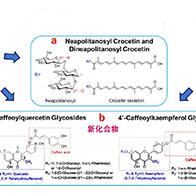
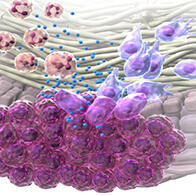
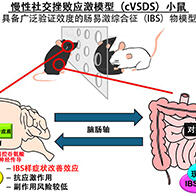
東京科學大學石野史敏名譽教授、藤岡慶史(研究當時為該大學研究生院卓越博士生,現為理化學研究所特別研究員)以及東海大學金児-石野知子客座教授的研究團隊,與山梨大學、日本國立研究開發法人理化學研究所共同發佈成果稱,發現逆轉錄病毒衍生基因Rtl8a、Rtl8b與成體期肥胖、運動能力下降、社交能力降低及抑鬱樣症狀存在關聯。該結論是通過分析雙基因剔除(KO)小鼠而得到的。鑑於該小鼠的症狀與普拉德-威利症候群(PWS)的後期症狀特徵高度相似,該疾病致病區域的靶點為人類Rtl8a基因,所以通過將KO小鼠用作模型小鼠,有望推動PWS發病機製研究和治療藥物開發的進程。相關研究成果已發表於國際學術期刊《Open Biology》的1月29日刊上。
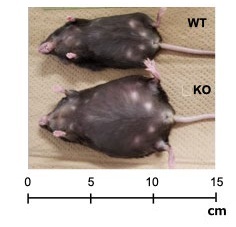
圖1:KO小鼠成體期出現的肥胖症狀。圖中為80周齡正常小鼠(上)與KO小鼠(下)(供圖:東京科學大學)
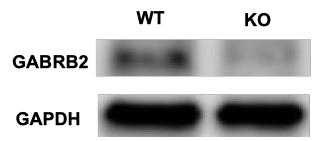
圖2:KO小鼠(右)前額葉皮層中的GABRB2蛋白質表達降低(供圖:東京科學大學)
哺乳動物基因體中含有在演化過程中哺乳類祖先感染的病毒為來源的基因。這些基因經過突變後可作為具有新功能的基因被利用,參與多種生理現象。
來源於逆轉錄病毒的Rtl8a、Rtl8b、Rtl8c是在X染色體上形成基因簇的三個功能相似的同源性基因,均為有胎盤哺乳動物的獨特性基因,但這些基因的功能此前並不明確。
研究團隊此前已發現,另一種病毒來源的哺乳動物獨特性基因PEG10具有胎盤形成的必需功能。此外,研究團隊還製備了Rtl8c敲除小鼠,但未觀察到顯著異常。
因此,此次研究團隊製備了Rtl8a、Rtl8b雙基因剔除小鼠(KO小鼠)並進一步進行解析。
結果顯示,雙基因剔除的KO小鼠自成體期開始出現肥胖症狀,並表現出活動能力下降、社交能力降低及抑鬱樣行為等異常現象。
Rtl8a、Rtl8b蛋白在大腦前額葉皮層與下視丘表達。研究認為KO小鼠的異常表現源於這些腦區的功能失調。
進一步對KO小鼠前額葉皮層進行基因分析發現,與神經疾病相關的抑制性神經傳導物γ-胺基丁酸(GABA)接受者GABRB2的表達水平降低。
PWS是日本政府指定的一種難治性疾病,多數病例為非遺傳性,其發病機製為15號染色體的特定區域形成了母源二倍體。初期表現為發育遲緩,後期則會引發肥胖及特徵性行為異常等。
近年,有研究顯示,天使症候群(AS)患者體內存在Rtl8蛋白的過剩表達。目前已知AS的致病染色體區域與PWS相同,其原因是父源二倍體化或UBE3A基因突變發生突變。
Rtl8蛋白是UBE3A的作用靶點,因此可預測出PWS患者體內的Rtl8表達會降低。
鑑於KO小鼠的症狀與PWS高度相似,而PWS的致病區域靶點為Rtl8a基因,因此KO小鼠有望作為PWS研究的模型小鼠使用。此前沒有兼具PWS研究條件的模型小鼠。
石野名譽教授指出:「此前沒有人考慮過Rtl8基因是人類PWS致病基因的可能性。但基於此次實驗,我們認為這種可能性較高。今後,我們計劃調查實際PWS患者體內是否存在Rtl8基因的突變或缺失。此外,那些曾被視為無用垃圾序列的病毒來源序列中,可能還存在其他與人類疾病相關的重要功能,我們期待展開進一步的探索。」
原文:《科學新聞》
翻譯:JST客觀日本編輯部
【論文資訊】
期刊:Open Biology
論文:Targeting of retrovirus-derived Rtl8a/8b causes late-onset obesity, reduced social response and increased apathy-like behaviour
DOI:10.1098/rsob.240279