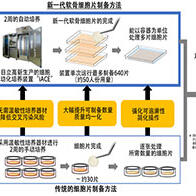
日本厚生勞動省於2026年3月6日有條件併附期限地對兩款使用人工多能性幹細胞(iPS細胞)的再生醫療產品發放了生產銷售許可。這兩款產品分別面向重症心力衰竭和巴金森氏症患者,是全球首次獲批的「日本產」iPS細胞治療產品。預計這兩款產品最早將在年內應用於臨床。
iPS細胞是通過向皮膚等體細胞人工導入數種基因,使其獲得分化為人體的多種細胞和組織的細胞。自2006年京都大學的山中伸彌教授等人宣佈在小鼠中成功製備出該細胞以來,已過去了約20年。日本率先使再生醫療成為常規療法,除此次實現臨床應用的疾病外,針對其他疾病的臨床試驗也在推進之中。對患者而言這意味著治療選擇的增加,同時也提升了人們對新型療法問世的期待。
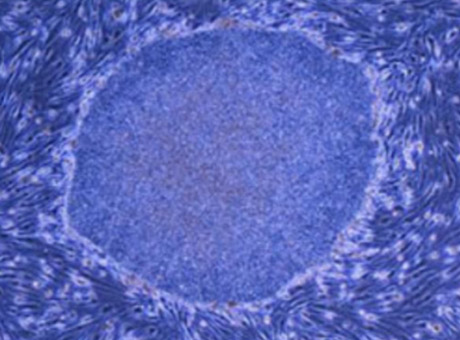
iPS細胞的顯微鏡圖像(山中伸彌/京都大學及日本科學技術振興機構提供)
大學初創企業與研髮型企業推動產品開發
日本厚生勞動省下屬的專家委員會於2月19日同意在滿足特定條件且設定期限的前提下同意兩項產品用於臨床,之後厚生勞動省正式批准了這兩款產品的上市。獲批產品包括:由大阪大學衍生的初創企業「CUORiPS」(東京)開發的「ReHeart」,以及住友化學集團旗下研髮型製藥企業「住友製藥」(大阪市)開發的「Amchepry」。
「ReHeart」主要用於治療因冠狀動脈狹窄或閉塞導致心肌缺血、心功能下降的「缺血性心肌病」所引發的重症心力衰竭。其原理是將來自他人iPS細胞培養得到的心肌細胞製成片狀,貼附於心臟表面,使其定植並促進其形成新的血管。在臨床試驗中,該產品已為8名患者實施移植,所有患者的症狀均有所緩解,心功能等指標也出現了改善。
「Amchepry」則用於治療巴金森氏症。該病由大腦中分泌神經遞質多巴胺的神經細胞減少所引發。治療方法同樣利用他人iPS細胞,誘導其分化為多巴胺神經前驅細胞後,移植至患者腦部。在臨床試驗中共有7人接受移植,其中6人確認能夠產生多巴胺。
鑒於兩款產品的臨床試驗樣本數量較少,日本厚生勞動省專家委員會依據「若能確認安全性並可推定有效性的前提下,則可設定附帶條件及期限,予以提前批准」的制度,做出了批准的決定。條件是在最長7年的批准期限內,通過實際臨床使用進一步確認其有效性,確認有效後,可轉為無條件許可。
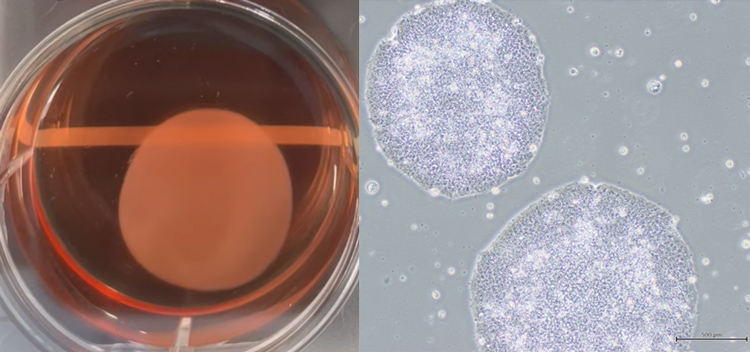
源自iPS細胞的心肌片(左圖,摘自CUORiPS的介紹視頻)與住友製藥培養的iPS細胞(右圖,由住友製藥提供)
多方科研努力跨越難關實現應用
憑藉榮獲2012年諾貝爾生理學或醫學獎的山中教授的劃時代研究成果,再生醫療產品得以在全球首次實現實用化,而這背後,離不開研究和相關開發人員為克服諸多難題所付出的非同尋常的努力。
關於利用iPS細胞的再生醫療,雖然從一開始就備受期待,但也有人指出其安全性方面的隱患。其中最具代表性的就是源自體細胞的組織可能發生癌變。在移植組織時,如果殘留了未分化的iPS細胞,就存在癌變的風險。雖然移植的細胞來自患者自身,不易發生排異反應,但仍需謹慎確認是否確實沒有發生排異反應。
針對癌變風險,日本厚生勞動省的研究團隊於2016年對iPS細胞基因組進行分析,並提出若發現了可能與致癌相關的基因突變,應避免進行移植。針對這些擔憂和課題,以山中教授所屬的京都大學iPS細胞研究所(CiRA)為首,日本國內許多大學和研究機構的研究人員持續開展研究並取得了諸多成果。
2014年,日本國立研究開發法人理化學研究所(簡稱,理研)等機構首次成功實施了將利用iPS細胞製備的視網膜細胞移植至患者體內的手術。此後,大阪大學和慶應義塾大學率先開展心臟疾病應用研究。2016年,信州大學等團隊宣佈,通過將細胞移植至患有心梗的模型猴體內,成功恢復了其心功能。
另一方面,在2016年,北海道大學與慶應義塾大學的研究團隊宣佈,利用不易患癌的裸鼴鼠,解析了抑制iPS細胞癌變的基因作用機制。2017年,京都大學又開發出可去除具有癌變風險細胞的方法。為實現「安全再生醫療的實用化」的目標,日本各大學和研究機構之間都在不斷加強合作。
即使移植到活體中也不會形成腫瘤的裸鼴鼠的iPS細胞(北海道大學等提供)
糖尿病、脊髓損傷、癌症之後的新挑戰
在多家研究機構穩步推進再生醫療實用化研究的背景下,CUORiPS於2025年4月、住友製藥於同年8月分別向日本厚生勞動省提交了上述兩款產品的生產銷售申請。
這兩款產品率先提交了申請並最終獲得批准,同時還有其他多種疾病的再生醫療研究同樣在穩步推進之中。
據日本厚生勞動省等機構介紹,目前以獲得再生醫療產品銷售許可為目標的臨床試驗及臨床研究正在多個領域展開,包括:加齡性黃斑變性(理研等)、1型糖尿病(京都大學)、再生障礙性貧血(京都大學)、外傷性脊髓損傷(慶應大學)、角膜上皮幹細胞缺損症(大阪大學等)。
此外,iPS細胞在癌症治療領域的應用也備受期待。日本千葉大學附屬醫院與理研於今年1月宣佈,利用iPS細胞製備出攻擊癌細胞的「自然殺傷T(NKT)細胞」,並在針對頭頸部癌症患者的臨床試驗中,8名患者中有2人獲得了腫瘤縮小的效果。此外,針對卵巢癌(CiRA與國立癌症研究中心東醫院)等多個癌症的治療研究也在進行中。
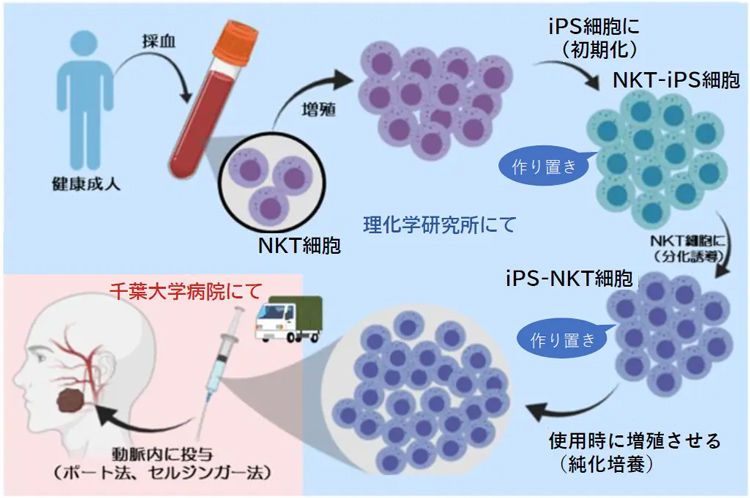
利用iPS細胞製備NKT細胞,然後應用於頭頸部癌症患者的流程圖(千葉大學病院/理化學研究所提供)
山中教授:「審慎的同時穩步推進」
日本厚生勞動大臣上野賢一郎在6日內閣會議後的記者會上談及此次批准的意義時表示「希望不僅能為日本,也能為全世界患者帶來福音」。不過,此次的批准畢竟還是附帶條件及期限的批准,需要在規定時間內收集更多數據,最終證明其療效,才能取得「正式批准」。

內閣會議後的記者會上的厚生勞動大臣上野賢一郎(3月6日、厚生勞動省提供)
今後,為了使利用iPS細胞製作的醫藥品能在更廣泛的醫療領域得到應用,對前兩例的安全性和療效進行嚴謹的驗證工作必不可少。目前擔任CiRA名譽所長的山中教授在厚生勞動省專家委員會批准該申請時發表瞭如下評論。
「在小鼠iPS細胞相關論文發表20周年的重要節點,能夠朝著社會應用邁出重要一步,我感到非常高興。然而,要將其確立為一種醫療手段,還需要通過更多病例驗證其安全性和有效性。我認為,重要的是不急不躁、科學上保持審慎態度,繼續一步一個腳印地穩步前進。」

在名古屋市某酒店進行演講的山中伸彌教授(2016年1月、筆者拍攝)
原文:內城喜貴/科學記者 JST Science Portal 編輯部
翻譯:JST客觀日本編輯部
【相關超連結】
厚生勞動省《上野大臣記者會見概要(2026年3月6日)》
文部科學省《關於使用iPS細胞的全球首個再生醫療等產品獲批「大臣談話」》
CUORiPS株式會社官網
CUORiPS《關於取得人類(同種)iPS細胞來源心肌細胞片附條件及附期限制造銷售批准》
住友製藥《關於在日本取得非自體iPS細胞來源多巴胺神經前驅細胞「Amsheplie」的製造銷售批准的通知》