京都大學醫生物學研究所統合生物過程領域的向山宙希研究員、渡邊仁美助教、近藤玄教授、廣田圭司副教授等人組成的研究團隊,發現了自體免疫性關節炎中引發慢性發炎和疼痛的新機制。研究團隊證實,從骨髓遷移來的炎性單核球在關節內分化為分別承擔「發炎」和「疼痛」功能的不同細胞群體。向山研究員表示:「在臨床中,就存在部分類風濕關節炎患者的發炎雖得到控制,但疼痛仍然持續存在的現象。通過將此次發現的巨噬細胞作為靶點,我們希望開發出不僅能抑制發炎,還可改善疼痛的治療方法」。相關成果已發表於《Science Advances》。

向山宙希研究員(供圖:科學新聞)
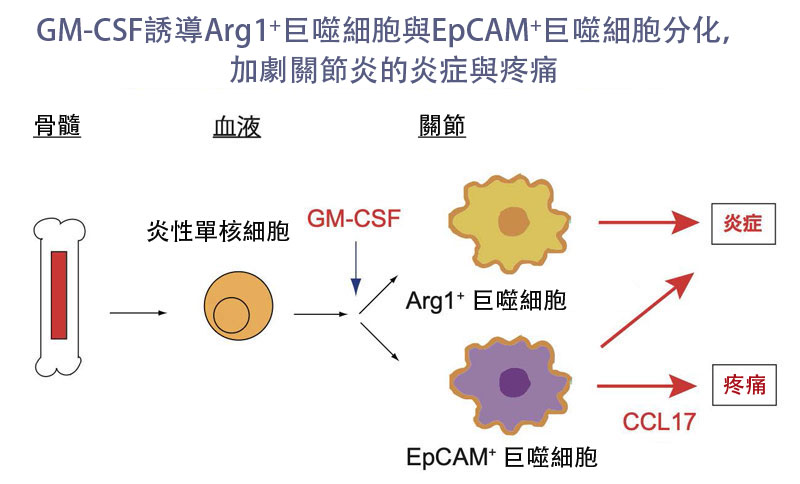
圖1 從骨髓經由血液遷移而來的炎性單核球進入關節後,在GM-CSF的作用下分化為Arg1⁺和EpCAM⁺巨噬細胞,加劇了關節炎症。特別是EpCAM⁺巨噬細胞通過CCL17還參與了疼痛過程。(供圖:京都大學向山宙希研究員)
類風濕關節炎是一種約佔人口1%的自體免疫性疾病,免疫細胞誘導發炎,引發關節疼痛與腫脹。巨噬細胞是腫瘤壞死因子(TNF)等炎性細胞介素的主要來源,在病情加重與病態持續中發揮著核心作用,近年研究發現其還與疼痛相關。
小鼠模型和臨床試驗已表明,作為細胞介素之一的顆粒球-巨噬細胞集落刺激因子(GM-CSF)深度參與關節炎的病理形成。然而,GM-CSF具體作用於哪些細胞、通過何種方式引發發炎,此前一直未明確。
研究團隊推測,GM-CSF可能通過作用於關節內的巨噬細胞來引發發炎和疼痛。
對此,研究顯示缺乏趨化因子接受者CCR2的SKG小鼠(呈現與人源類風濕關節炎類似病態的自體免疫性關節炎模型小鼠),其炎性單核球未遷移至關節,關節炎症狀明顯輕於野生型SKG小鼠,這表明炎性單核球在關節炎中起著重要作用。對關節巨噬細胞的產生和分化過程進行分析後發現,致病性巨噬細胞的主要前驅細胞並非組織常駐巨噬細胞,而是來自於從骨髓遷移而來的單核球。
於是,研究團隊將CCR2缺陷型SKG小鼠與GM-CSF受體缺陷型SKG小鼠相結合,阻斷炎性單核球和巨噬細胞中的GM-CSF信號後發現,小鼠幾乎不再發生關節炎,由此證實,GM-CSF信號對於炎性單核球和巨噬細胞的致病性至關重要。
此外,研究團隊使用混合移植了野生型SKG小鼠和GM-CSF受體缺陷SKG小鼠骨髓的嵌合小鼠,採集了發炎的關節組織,進行了單細胞RNA測序。通過對兩種小鼠來源的細胞分別進行標記,對能夠接收和無法接收GM-CSF信號的細胞進行了詳細的比較分析。結果顯示,在GM-CSF受體缺陷SKG小鼠來源的細胞中,Arg1陽性巨噬細胞和EpCAM陽性巨噬細胞缺失。這些巨噬細胞高表達炎性細胞介素,且EpCAM陽性巨噬細胞還特異性表達與疼痛相關的分子CCL17。
本研究首次揭示了GM-CSF對於具有特定功能的高致病性巨噬細胞群體的分化起著至關重要的作用。而此前,GM-CSF對關節巨噬細胞的具體作用一直不明確。
本次研究的成果有望推動類風濕關節炎全新療法的開發。迄今為止,尚無以巨噬細胞為靶點的類風濕關節炎的治療手段。若以本次發現的Arg1陽性巨噬細胞和EpCAM陽性巨噬細胞等致病性巨噬細胞為對象,就有望開發出既能抑制發炎又能緩解疼痛的治療方法。
研究團隊表示,今後將利用手術等採集的臨床樣本繼續推進研究。
原文:《科學新聞》
翻譯:JST客觀日本編輯部
【論文資訊】
期刊:Science Advances
論文:Pathogenic GM-CSF drives functional diversification of inflammatory macrophages in autoimmune arthritis
DOI:doi.org/10.1126/sciadv.aec0986