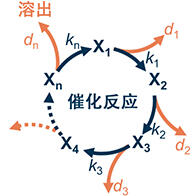
京都大學研究生院理學研究科的萩野浩一和前野悅輝兩位教授建立了「原子核」週期表(圖1)。
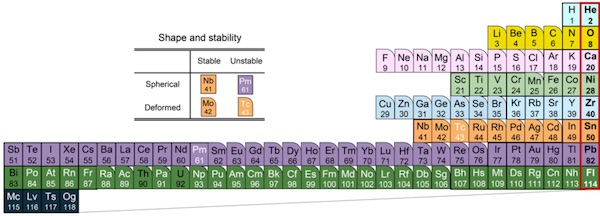
圖1:新建立的原子核週期表
中學化學就學過,構成元素的原子的中心是原子核,電子圍繞著原子核運動(圖2)。原子核中含有的質子數為「原子序」。「元素週期表」 的原子符號就是按原子序的順序排列的,性質相似的元素會排列在一起,這個排列體現了元素的週期性規律(圖3)。2019年是德米特里·門得列夫(Dmitri Mendeleev)建立元素週期表150週年(目前全球廣泛使用的元素週期表其實並不是門得列夫建立的「短週期表」,而是基於阿爾弗雷德·維爾納(Alfred Werner)建立的「長週期表」)。
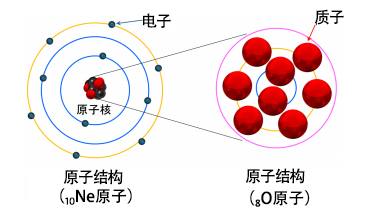
圖2:原子與原子核的結構圖。作為一例,圖中所示為鈍氣元素氖(Ne)的 軌域以及原子核具有魔數的氧(O)的質子軌道,圓代表軌道的殼層。
原子核由質子(圖中紅色)和中介子(圖中黑色)構成。原子核帶有與質子數成比例的正電。元素週期表體現了原子核周圍運行的電子從低能軌道開始依次填滿軌道殼層的情況。
在原子核中,可以認為構成原子核的質子和中介子也有類似的運動軌道,原子核的中心並沒有其他的「核」。不過,在質子和中介子的相輔作用下(湯川秀樹提出的名為「核力」的強相輔作用),原子核内部也會形成像電子一樣分成幾個殼層的軌道,並從低能軌道開始依次填滿殼層。這被稱為原子核殼層模型(Shell Model)。魔數的原子核是殼層正好被填滿的原子核,對應鈍氣。不過,如圖2所示,由於電子與質子和中介子的環境(位能)不同,原子與原子核的各殼層所能容納的最大數量大不相同。原子在電子數為2、10、18、36、54和86時,原子核在質子數為2、8、50、82和114時會填滿軌道殼層,這時候性質變得穩定。另外,質子數為40時,雖然程度比較小,但也會顯示同樣的性質。中介子也有同樣的魔數,除114變成126外,其他與質子相同。
圖3的不同顏色表示軌道的差異。最右一列的氦和氖等鈍氣,由於電子正好填滿了軌道的外殼,因此性質非常穩定,是不容易發生化學反應的元素。
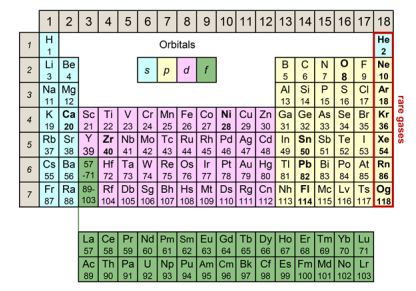
圖3:元素週期表(維爾納的長週期表)
那麼,能否建立一個原子核週期表呢? 原子核中除質子外還含有中介子,即使是相同質子數量的元素,也存在中子數不同的同位素。而且,中子數會大大影響原子核的穩定性。雖然有涵蓋所有元素的核素圖,但一直未發現其與元素週期表的對應關係。
對此,萩野浩一和前野悅輝教授通過選擇各元素最具代表性的同位素,建立了圖1所示與元素週期表對應的原子核週期表。該表右端排列的是與鈍氣元素相對應,質子數為魔數的元素。以前從未有人提出過這種原子核週期表。
圖4仿照元素週期表(圖3)用不同顏色對質子的軌道殼層進行了區分,原子魔數與原子核魔數的差異也變得一目瞭然。藍色背景色表示呈圓形擴散的s軌道(圖2的藍色圓圈),直到第12號元素鎂(Mg)其第三個3s軌道構成的殼層在電子中才被填滿,而在質子軌道中則被第70號元素鐿(Yb)填滿,這樣就反映出了軌域與質子軌道在性質上的顯著差異。
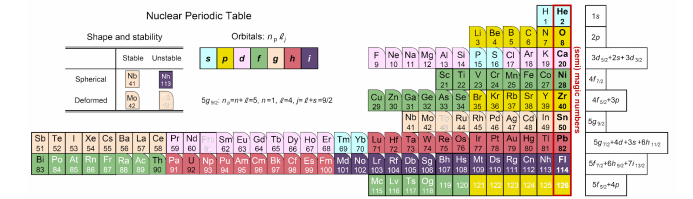
圖4:用不同顏色對質子軌道進行了區分的原子核週期表
從該週期表來看,滿足魔數的穩定原子核的形狀接近球形。而離魔數越遠,原子核形狀就越接近橄欖球形,另外還出現了即使原子序比鉛(Pb)小也會自然放射衰變的不穩定原子核(白字元素)。在新的原子核週期表中,不僅是殼層結構,各元素的原子核變形和穩定性也一目瞭然。
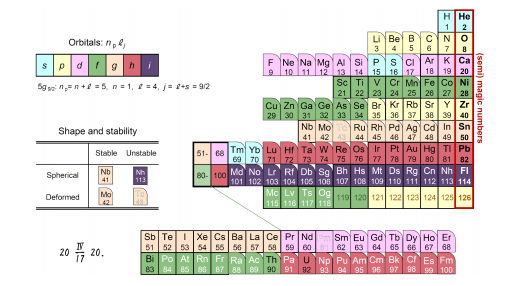
圖5:形狀與元素週期表(圖3)類似的原子核週期表
圖5的原子核週期表形狀看上去與常用的元素週期表(圖3)類似,但有一個很大的區別需要注意。在元素週期表中,正如屬於同一列(族)的元素用相同的顏色表示一樣,這些元素都擁有軌道性質相同的電子,因此在性質方面具有相似性。但在原子核週期表中,雖然上述魔數附近的性質具有週期性,不過從顏色差異上便可以看出,同一列元素的原子核擁有軌道不同的質子,因此在性質方面並無相似性。
這種能與元素週期表進行比較的原子核週期表,包括魔數在内,可以形成學習原子核性質的新指標。今後,大學的教科書等估計將採納原子核週期表進行教學。
原子核週期表還可以做成立體的。將圖1列印,用剪刀和透明膠帶可輕鬆製作出下圖(圖6)中的模型。關於立體元素週期表,前野教授約20年前設計過「Elementouch」,並且還作為京都大學的商品銷售,此次原子核立體週期表被命名為「Nucletouch」。

圖6:原子核的立體週期表Nucletouch
論文資訊
題目:A Nuclear Periodic Table
期刊:《Foundations of Chemistry》
DOI:https://doi.org/10.1007/s10698-020-09365-5
文:JST客觀日本編輯部