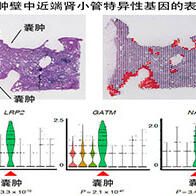
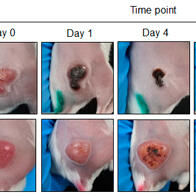
日本三洋化成工業株式會社(代表董事長:樋口章憲)與廣島大學研究生院醫系科學研究科整形外科學的安達伸生教授、香川大學醫學部的石川正和教授(研究當時為廣島大學)等人組成的研究團隊於10月31日宣佈,已針對半月板損傷患者啟動了驗證「絲彈性蛋白」的有效性與安全性的企業臨床試驗。今後將開始招募志願患者,並在廣島大學醫院等7家醫療機構實施試驗。目標是在2027年度內通過藥品審批,並在2028年度內實現納入醫保和上市銷售。該技術有望對預防膝關節病灶並延長健康壽命做出貢獻。

圖1 左起樋口社長、安達教授、川端慎吾(三洋化成工業Siela Project項目負責人)(供圖:廣島大學)
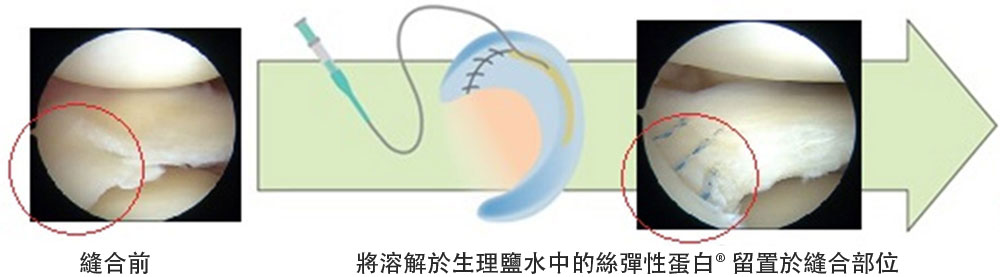
圖2 半月板中放置絲彈性蛋白® 的示意圖(供圖:三洋化成工業)
膝關節病灶是由於老化或運動導致膝關節軟骨及半月板受損而引起的。據估計,日本膝關節病灶患者約有3000萬人,其中伴有疼痛或行走困難等症狀者約為1000萬人。膝關節病灶是導致需要護理的首要誘因,對健康壽命造成嚴重影響,其經濟損失估算每年約5萬億日元。
半月板在膝關節中起到緩衝作用,並幫助膝關節平穩運動。半月板損傷通常採取縫合術或切除半月板本體的切除術。半月板損傷多見於老年人,另外由運動引起的外傷性損傷在年輕人中也較為常見。
然而,縫合術中有30%至40%的病例需要再次手術,而切除術則容易因膝關節功能障礙而引發或加速膝關節病灶的發生與進一步發展。
半月板由外側和內側兩層構成,縫合術的成功與血流密切相關,對內側無血流白區的損傷並不適用。因此,白區的治療一直是實現癒合的關鍵課題。
針對這一問題,此次臨床試驗在對白區損傷實施了縫合術並在斷裂部位留置絲彈性蛋白。
絲彈性蛋白是將絲素蛋白(來源於絲的蛋白質)與彈性蛋白(存在於人體皮膚中的彈性蛋白)的重複序列導入大腸桿菌中,通過生物合成製得的基因重組蛋白。該產品已於今年4月作為難治性皮膚潰瘍的創傷癒合材料獲得藥物批准,計畫於明年春季開始銷售。
經提取和精製獲得的絲彈性蛋白呈棉絮狀。
既往的基礎研究已確認其促進細胞遷移能力活化、增強膠原蛋白生成等特徵,且由於並非來源於動物,安全性較高。
本次臨床試驗將在關節鏡下實施縫合術,並注入和放置絲彈性蛋白水溶液。絲彈性蛋白在體內轉變為凝膠狀,作為促進細胞增殖的支架,幫助半月板癒合。
雙方自2017年起開展共同研究,並自2018年起在AMED支持下持續推進研究。
此前已完成小動物與大動物的臨床前試驗,並於2022年以8名患者為對象實施了醫生主導的臨床試驗。其中6例成功實現通過縫合保留半月板,在傳統治療方法難以奏效的病例中也取得了良好結果。鑒於其安全性與有效性得到確認,本次決定開展企業臨床試驗。
本次企業臨床試驗的對象為8歲以上、取得同意、MRI圖像顯示包含白區,且被診斷為單獨發生或伴隨前十字韌帶損傷的半月板損傷的患者,存在由半月板損傷引起的機械性損傷症狀,且經運動療法及鎮痛藥等保守治療後疼痛仍未改善,IKDC評分在55分以下者。
排除標準包括BMI在50公斤/m²以上等。
本試驗自實施縫合術及絲彈性蛋白注入與放置起,設定365天為觀察期,並在第1周、第2周、第12周、第24周進行關節鏡檢查,以評估癒合狀態。
主要評價指標設定為IKDC評分達到69分以上,同時將時間變化及是否需要再次手術等作為次要評價指標。
試驗預計於2027年3月結束。爭取在日本獲得藥物批准和FDA批准。在全球範圍內對半月板保留治療的幹技術頗受期待。
試驗實施機構包括日本廣島大學醫院、香川大學醫學部附屬醫院、關東勞災醫院、甲府醫院、JCHO大阪醫院、弘前大學醫學部附屬醫院、札幌圓山整形外科醫院、兵庫縣立復健中央醫院。試驗協調醫師由安達教授擔任。
原文:《科學新聞》
翻譯:JST客觀日本編輯部
【論文資訊】
期刊:Scientific Reports
論文:First-in-human exploratory trial assessing safety, feasibility, and efficacy of artificial protein (silk-elastin) in promoting healing in patients with meniscus injuries
DOI:10.1038/s41598-025-88616-x