清除老化細胞的相關研究正在全球範圍內積極開展,並正處於快速發展階段。其中,將老化細胞本身予以清除的做法被稱為「Senolysis(老化細胞清除)」,而僅去除老化細胞的部分特徵(例如慢性發炎)的做法則被稱為「Senostatics(老化表型抑制)」。
京都大學研究生院醫學研究科的近藤祥司副教授、三河拓己研究員、龜田雅博特定助教等人組成的研究團隊發現了一種可用於清除老化細胞的候選治療藥物。研究團隊發現,在老化細胞中,糖酵解酶PGAM與信號傳導激酶Chk1出現異常增強的蛋白結合,導致糖酵解代謝水平升高,並提高老化細胞的存活性。當研究人員抑制小鼠體內PGAM與Chk1的結合後,可以選擇性地誘導老化細胞發生程式性細胞死亡,從而減少慢性發炎並改善老化症狀。此外,在作為難治性年齡相關疾病之一的肺纖維化模型小鼠中,研究團隊同樣通過抑制PGAM與Chk1的結合成功清除老化細胞,觀察到了症狀改善的效果,表明其可成為年齡相關疾病的有效新型治療方法。相關成果已發表在《Signal Transduction and Targeted Therapy》上。
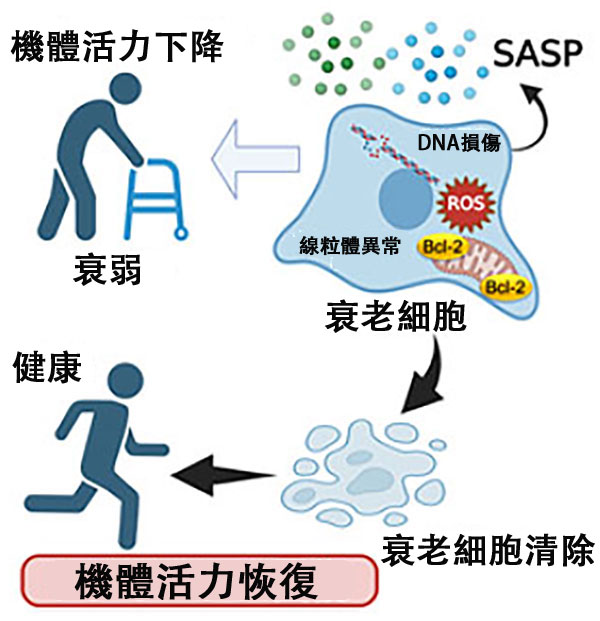
圖1 老化細胞引發的慢性發炎會導致機體恢復能力下降。清除老化細胞(Senolysis)有助於恢復機體活力。(供圖:京都大學,由BioRender製作)
近藤副教授表示:「2004年,羅氏公司在研究抗癌藥候選物時發現的Natarin,其光學異構物具有清除老化細胞的作用。團隊今後將繼續推進最優結構設計等研究工作,努力早日讓該成果惠及患者。」
近藤副教授團隊從老化研究的視角,長期聚焦糖酵解酶PGAM進行研究。通過最新的NanoBit技術,研究團隊成功將細胞內PGAM–Chk1激酶的結合過程視覺化。藉助該技術發現,老化細胞與癌細胞在代謝上具有共同特徵:由於PGAM–Chk1激酶結合增強,糖酵解代謝隨之升高。當研究人員向小鼠施用可抑制PGAM–Chk1結合的抑制劑後,老化小鼠的肌力出現改善,肝臟和腎臟也呈現功能改善的效果。
另一方面,Natarin最初作為p53―Mdm2結合抑制劑所開發的抗癌藥物,包含Natarin3a及其光學異構物Natarin3b,並證實只有Natarin3a具備抑制p53―Mdm2結合的作用。並且,Natarin3a的副作用較為明顯,所以該藥物最終未能實現臨床應用。
研究團隊發現,Natarin具有抑制PGAM–Chk1結合的能力。近藤副教授表示:「最初的實驗結果顯示無法抑制這種結合,但在調整解析方法後,確認到Natarin確實具備這種抑制作用。」
Natarin3a與3b的差異僅體現在是否具有抑制p53―Mdm2結合的能力,而兩者均具備抑制PGAM–Chk1結合的作用。因此,Natarin3b有望在不引發明顯副作用的情況下清除老化細胞。事實上,當分別將Natarin3b作用於年輕細胞和老化細胞時,僅在老化細胞中誘導了程式性細胞死亡,相比Natarin3a對年輕細胞和老化細胞均表現出毒性。
此外,研究團隊證實轉錄因子FOXM1是PGAM–Chk1結合的作用靶點。研究結果表明,在老化細胞中,FOXM1會抑制促凋亡基因BIM的表達。當施用Natarin3b時,FOXM1的活性受到抑制。
在解析老化內臟組織中FOXM1的表達模式後,發現FOXM1在肝臟、肺、腎髒和肌肉等多個組織中處於活化狀態。因此,當研究團隊將Natarin3b用於加齡性疾病之一的肺纖維化模型小鼠時,纖維化標誌物的表達以及纖維化面積均出現下降,並顯示出有效的治療效果。
近藤副教授表示:「30多年來,我作為一名綜合內科醫生接診過許多老年患者,至今仍能記得每位患者的情況。雖然此次的研究成果未能讓他們受益,但希望在既往經驗的基礎上,未來能將研究成果應用於老年醫學領域。」
原文:《科學新聞》
翻譯:JST客觀日本編輯部
【論文資訊】
期刊:Signal Transduction and Targeted Therapy
論文:Abrogation of aberrant glycolytic interactions eliminates senescent cells and alleviates agingrelated dysfunctions
DOI:10.1038/s41392-025-02502-6