老年癡呆的進程大都是從認知功能尚未下降的前期階段進展到輕度認知障礙(MCI),最終發展為認知功能全面下降的癡呆症的。如果能在臨床前期階段進行預防性干預,就能延緩癡呆症發病,進而提升生活品質、降低醫療費用。近年來,雖然已有大量診斷生物標誌物,日本國立研究開發法人量子科學技術研究開發機構(QST)與大阪公立大學的研究團隊正在合作開發更簡便、更低成本的診斷方法。

左起依次為飯田琢也教授、樋口真人中心主任、高畑圭輔主任研究員(照片:科學新聞社)
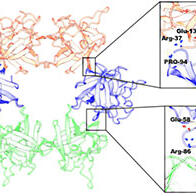
針對三大癡呆症(阿茲海默症、額顳葉變性症、路易體癡呆症),以澱粉樣β、tau蛋白、TDP-43、α-突觸核蛋白為靶點的診斷生物標誌物已被大量開發出來。這歸功於QST等機構開發的PET藥劑,使人們得以瞭解腦内靶分子的積累狀況,進而能夠特定外周血中的生物標誌物。然而,由於血液中標誌物分子濃度極低,必須使用裝置和試劑等價格昂貴的高靈敏度檢測方法,因而難以在一般診所或健康體檢中應用。
大阪公立大學飯田琢也教授團隊開發的LAC-SYS(光誘導加速系統),通過利用雷射光壓及產生的流動,能夠捕集溶液中的特定物質;通過使用附著抗體的微珠,僅收集目標生物分子;通過將其與免疫層析或PCR等分析技術組合,可以將檢測靈敏度提高約100倍。例如,在ELISA檢測中,不僅檢測靈敏度較以往提高了100倍,檢測速度也提升至原來的60倍左右,用時僅約5分鐘。該技術只需要與傳統方法結合即可實現,低成本檢測是其一大優勢。
目前,研究團隊已使用筆記本大小的實體模型,從微升級血液中成功檢測出了癌症、癡呆症、感染症標誌物。飯田教授表示:「我們正在推進與企業的合作研究,同時力爭實現實用化。未來,我們希望實現只需在手掌大小的檢測裝置上安裝卡盒,就能在家中輕鬆判斷是否處於疾病前期階段。」
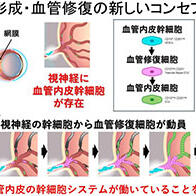
另一方面,若不對癡呆症本身進行更深入的理解,就無法推動治療方法的開發。侖卡奈單抗等澱粉樣β抗體藥物雖能將澱粉樣β的蓄積抑制八成,但對認知功能障礙的抑制效果僅有三成。因此,小膠質細胞受到學界關注。小膠質細胞負責腦內的免疫功能,感知到病原體或損傷時,會吞噬死細胞、釋放細胞介素等。但研究逐步發現,在阿茲海默症患者體內,小膠質細胞的過度活化反而使神經細胞受損。
QST腦功能成像研究中心主任樋口真人表示:「在人體內,老化細胞表面會出現孔洞,從中釋放出促炎物質,接連引發周圍細胞的發炎和老化。這一過程同樣發生在腦內。我們認為,蛋白質沉積(蛋白質老化)、膠質細胞衰老、膠質細胞發炎三位一體、相互交織的腦內老化發炎,正是癡呆症發病的本質。為找出調控這一腦內老化發炎的關鍵物質,我們正在開展研究。」
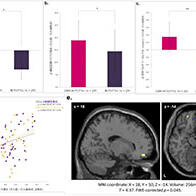
此外,還有與普通癡呆症不同、以精神症狀為首發症狀的癡呆症。其中之一是衝撞運動引發的慢性創傷性腦病。曾有研究報告指出知名摔跤手及橄欖球運動員等在退役後罹患精神病疾患並自殺的案例,對其死後的腦部進行檢查後發現,有大量tau蛋白蓄積。QST對退役的各類接觸性運動選手進行了tau PET成像,發現曾罹患各類精神病疾患的前選手腦中存在tau病灶。此前的研究已證實,tau病灶會隨時間推移而進展,使得以往難以實現的tau蓄積進展精細評估成為可能。目前已知,中高齡發病的精神障礙易出現重症化,且後續會發展為癡呆症。研究發現,約半數中高齡發病的情緒障礙患者,在認知功能下降開始前就已出現tau病灶。
QST主任研究員高畑圭輔表示:「我們證實了精神障礙背後與癡呆症致病蛋白存在關聯。癡呆症生物標誌物技術的進展,也將為以往難以客觀診斷的精神病疾患及精神醫學領域帶來巨大變革。我們需要搭建推進生物標誌物技術在臨床中實用化的框架與平台。」
通過開設新中心加速社會應用
大阪公立大學與QST將於明年5月開設大阪健康長壽醫科學中心。該中心將主導基於LAC-SYS的血液檢測臨床衡鑑。此外,中心將與樋口主任擔任項目負責人(PM)的「登月型(Moonshot)」目標開展合作,加速推進癡呆症預防與治療的社會應用。
原文:《科學新聞》
翻譯:JST客觀日本編輯部