日本千葉大學研究生院醫學研究院的本橋新一郎教授和千葉大學醫學部附屬醫院耳鼻咽喉與頭頸外科的飯沼智久講師,與日本國立研究開發法人理化學研究所(簡稱「理研」)生命醫科學研究中心合作,於1月16日宣佈,在將iPS細胞製備的免疫細胞「iPS-NKT細胞」直接施用於頭頸部鱗狀細胞癌的Ⅰ期醫生主導臨床試驗中,確認了免疫細胞的安全性,以及治療取得效果的跡象。研究確認,預製的異體iPS-NKT細胞可實現細胞的穩定供給,有望推動使用iPS-NKT細胞的治療方法的開發。相關研究成果已於12月30日發表在期刊《Nature Communications》上。
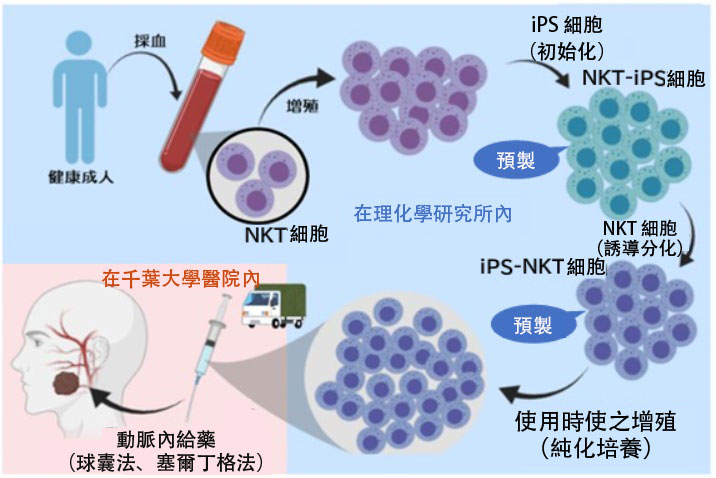
圖1 iPS-NKT細胞從製備到投用的流程
將冷凍保存的iPS-NKT細胞根據施用時機進行擴增後使用(供圖:千葉大學)
NKT細胞是一種具有NK細胞與T細胞特徵的T細胞,儘管其在血液中僅佔比0.01%,卻能通過樹突狀細胞等抗原呈遞細胞發揮強效的抗腫瘤作用。目前已知,NKT細胞本身既會直接攻擊癌細胞,還能產生IFN-γ來激活T細胞與NK細胞,使之對癌細胞發起攻擊。
此前,在千葉大學研究團隊針對頭頸部癌症進行了體內NKT細胞激活、體外培養並回輸的臨床研究。研究中暴露出了需使用患者的自體細胞、培養結果存在偏差、為個體定製治療會導致成本高昂等一系列問題。
為此,本次研究著眼於iPS細胞的高增殖能力,旨在開發出使用異體NKT-iPS細胞來源「NKT細胞(iPS-NKT細胞)」的治療方法。
2013年起,研究團隊在理化學研究所生命醫科學研究中心啟動了旨在建設主細胞庫的研究,並構建了一套從健康成人來源的NKT細胞中取得iPS細胞(NKT-iPS細胞),經冷凍保存實現預製,按需解凍後誘導分化為NKT細胞,經增殖後再給藥至患者的體制。由此,逐步實現了性能得到保障的細胞穩定供給。
上面的臨床試驗於2020年10月至2023年8月開展,針對已完成標準治療後復發或進展期頭頸部鱗狀細胞癌的患者給藥「iPS-NKT細胞」,並評估「iPS-NKT細胞」經腫瘤營養動脈給藥的耐性、安全性與有效性。
試驗對象為12例受試者,經篩選後10例正式參與。「iPS-NKT細胞」經腹股溝導管給藥,給藥頻次為1~3次(最多3次),給藥間隔2周。給藥劑量設定為第一劑量(3×10⁷cells/m²)與第二劑量(1×10⁸cells/m²),其中3例接受第一劑量,7例接受第二劑量。所有受試者在首次給藥前及給藥後第42天接受CT影像拍攝,研究對8例受試者的首次給藥前及給藥後第42天的情況進行對比評估。
研究結果顯示,在安全性方面,無法排除與給藥相關的不良反應有貧血、發熱、蕁麻疹、全身皮疹;最嚴重不良反應為1例接受第二劑量的受試者出現全身皮疹,但經類固醇治療後症狀快速消退。由此判定,第二劑量為最大耐受劑量。
在有效性方面,經CT影像評估:5例受試者腫瘤大小穩定(增大率±10%以內),其中2例觀察到腫瘤縮小(-10%)。3例受試者確認病情進一步發展,腫瘤增大率超20%。
針對1例腫瘤縮小的受試者,檢測其外周血中PD1陽性CD8+T細胞(攻擊細菌與癌細胞的免疫細胞)後發現,該細胞在給藥8天後被激活。單細胞分析中給藥8天後表達上調的基因組,被認為是受iPS-NKT細胞釋放的IFN-γ的影響而激活的。
研究進一步對腫瘤增大最顯著的1例、腫瘤縮小的2例受試者,開展給藥前至給藥後第21天的CD8T細胞時序性對比,發現腫瘤縮小的2例受試者體內CD8T細胞出現增殖,而腫瘤增大的1例受試者該細胞未有增加。
此外,對腫瘤縮小的2例受試者進行細胞毒性T細胞特性檢測後,確認具備既往抗原刺激記憶、或已擁有強細胞毒性的T細胞數量出現增加。
飯沼講師表示:「基於這一結果,我們認為該技術作為一種癌症免疫細胞療法開闢了免疫細胞可預製使用的道路。但效果還不足夠,目前千葉大學醫院正在開展/招募聯合使用擁有NKT細胞活化劑的樹突狀細胞與iPS-NKT細胞的臨床試驗。受試對象為所有頭頸部癌症及頸部復發病例。結合試驗成果,今後將繼續研究利用NKT細胞的癌症免疫細胞療法。」
原文:《科學新聞》
翻譯:JST客觀日本編輯部
【論文資訊】
期刊:Nature Communications
論文:Allogeneic iPSC-derived iNKT cells in recurrent head and neck cancer: a phase 1 trial
DOI:10.1038/s41467-025-66801-w