鈴木 勉
東京大學 研究生院工學系研究科 教授
2020年起任ERATO研究總負責人
核糖核酸(RNA)一般被認為是在DNA遺傳資訊合成蛋白質的過程中起中介作用的分子。但近年來的研究表明,它還直接參與維持生命機能、誘發疾病等多種生命現象。東京大學研究生院工學系研究科的鈴木勉教授致力於探究RNA被其他分子附加的「RNA修飾」機制,闡明RNA修飾調控生命機能的原理,並通過調控RNA修飾,為建立服務於新藥研發和疾病治療的技術基礎貢獻力量。
類似三葉草的結構
單一位點的甲基化引發性質劇變
生物的遺傳資訊被寫入細胞核內的去氧核糖核酸(DNA)中。DNA資訊被轉錄到傳訊RNA(mRNA)後輸送至細胞核外,之後,核糖體根據mRNA的鹼基序列連接氨基酸,合成構成生物體的蛋白質。在這一過程中,轉運RNA(tRNA)負責按照遺傳資訊連接氨基酸(圖1-左)。tRNA具有類似三葉草葉片的結構,其上結合著與mRNA的三聯鹼基序列相對應的氨基酸。
一個分子與糖或甲基等基團結合的現象被稱之為「修飾」,在化學領域,這也是製備擁有特定性質分子的常用方法。轉錄後的RNA在細胞內也會發生同類反應,20世紀後半葉,研究人員發現tRNA能夠接受結合甲基的甲基化、結合乙醯基的乙醯化等多種修飾(圖1-右),這些被被統稱為「RNA修飾」。
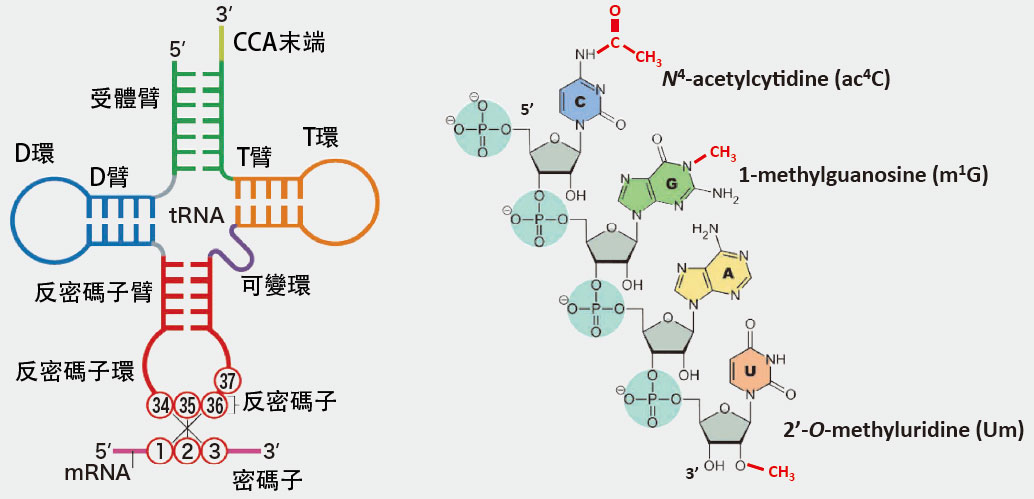
圖1 tRNA的結構(左)。tRNA摺疊形成L型立體結構,3'末端結合氨基酸,第34、35、36位的反密碼子與mRNA上被稱為密碼子的三聯鹼基序列互補結合。右表徵圖紅部分為RNA修飾的實例。上方兩處為鹼基發生的修飾,下方一處為核糖發生的修飾。
東京大學的鈴木勉教授正是被RNA修飾所吸引的學者之一。約30年前,他還是東京工業大學(現東京科學大學)的學生時,進行tRNA相關研究的他發現tRNA存在大量修飾並深受觸動,之後便開始了對RNA修飾的研究。他回憶道:「僅單一位點的甲基化,就能引發性質劇變,這一發現令我十分震驚。」
已發現超150種修飾,新「面孔」不斷湧現
2020年開始在ERATO啟動研究
與RNA同為核酸分子的DNA也會接受修飾,但人體的DNA修飾幾乎僅限於胞嘧啶這種鹼基的甲基化,其他類型僅發現數種。與之相比,RNA修飾已發現超過150種,且新的修飾類型還在不斷發現之中。在21世紀發現的23種RNA修飾中,鈴木教授的研究團隊發現了13種,據稱還有約20種尚未發表的新發現。
鈴木教授作為2020年啟動的日本國立研究開發法人科學技術振興機構(JST)的ERATO「鈴木RNA修飾生命機能項目」的研究總負責人,解析DNA遺傳資訊轉錄後的基因表現調控機制。為闡明RNA修飾所擔負的機能以及與生命現象的普遍性關聯,研究團隊按照「發現」「解析」「操控」三大方向研究RNA修飾(圖2)。項目由4個研究團隊構成,不僅探索新型RNA修飾並解析其功能,還開發革新性RNA修飾分析技術與機能操控技術,力求闡明疾病成因以及構築新藥研發和疾病治療的技術基礎。
| 子項目 | 研究概要與目標 |
| 「發現」 | ⚫解析從包括人類在內的多種生物中分離純化的RNA分子,探索新型RNA修飾並確定其化學結構。 ⚫運用高靈敏度質譜分析法,鑑定RNA修飾的種類與位點,闡明RNA修飾的機能。 ⚫利用奈米孔測序與深度學習技術,開發單分子水平的RNA修飾定量分析技術。 |
| 「解析」 | ⚫鑑定RNA修飾酶及其對應基因,闡明RNA修飾的生物合成與機能。 ⚫針對各類RNA修飾酶,構建合成酶基因剔除的小鼠模型,通過小鼠的表型探究RNA修飾的生理功能。 ⚫闡明由RNA修飾異常引發的疾病的發病機製。 |
| 「操控」 | ⚫通過對RNA修飾酶進行工程化改造,治療由RNA修飾異常引發的疾病(RNA修飾病)。 ⚫研發RNA修飾酶抑制劑,推動新藥研發。 ⚫開發通過照射特定波長紅外光激發RNA、從而激活或干擾RNA修飾功能的技術。 |
圖2 鈴木RNA修飾生命機能項目概要
支撐生物耐熱性的「掛鎖」
明確可逆性磷酸化修飾
「鈴木RNA修飾生命機能項目」目前已發表了超80篇研究論文。2022年發表於《Nature》期刊的《發現支撐生物耐熱性的「鎖」》是「發現」方向的重要研究成果。該研究在tRNA中發現可逆的磷酸化修飾,並闡明這一修飾能賦予tRNA耐熱性和抗RNA降解酶的特性,從而提升生物的耐熱能力。
磷酸基結合的磷酸化修飾在蛋白質中十分常見,但在RNA中發現該修飾尚屬鈴木教授團隊首創。鈴木教授研究室的大平高之助教在研究耐高溫古菌的tRNA時,發現鹼基第47位點的尿苷發生了磷酸化修飾(圖3-左)。進一步研究發現,無法產生該修飾酶的突變株,在高溫環境下的生存率會下降(圖3-右)。
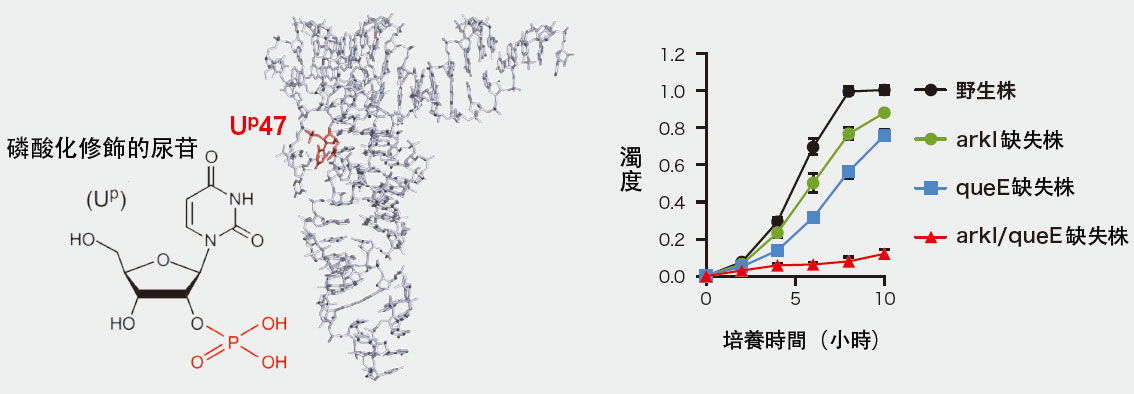
圖3 左圖為發生磷酸化修飾的尿苷(Up)的結構及其在tRNA中的位點(Up47)。右圖為研究87℃條件下古菌耐熱性的實驗結果。縱軸單位是以波長660奈米(1奈米為十億分之一米)光測量的濁度。同時缺失產生Up的修飾酶基因(arkI)和賦予tRNA結構剛性的基因(queE)的菌株,在高溫下的生存率顯著降低。
為闡明這種修飾為何與耐熱性有關,鈴木教授團隊與東京大學研究生院新領域創成科學研究科的富田耕造教授團隊合作,進行了X射線晶體結構解析。tRNA摺疊形成L型立體結構時,疏水性鹼基聚集在內部,使立體結構趨於穩定,但在高溫環境下,其立體結構會發生崩潰,由於這種熱變性而喪失機能。而磷酸基具有親水性,它會在立體結構中朝向溶劑側,即外側,從而能夠有效阻止高溫下的結構崩潰,起到穩定結構的作用。
鈴木教授比喻道:「這種磷酸化修飾並非將立體結構完全固定,而是在賦予立體結構一定柔韌性的同時防止熱變性。就像掛鎖一樣,允許一定程度的活動餘量,同時又能維繫住立體結構。」
從菠菜中獲得重要成果
發現「環境響應型開關」
2025年,鈴木教授的團隊發現了一種普遍存在於植物的葉綠體、粒線體,以及霍亂弧菌、綠膿桿菌等部分致病性細菌中的新型tRNA修飾。為了開展研究,團隊在學校附近的超市採購了40kg菠菜,並使用自主研發的用於純化微量tRNA的「全自動往復循環層析圖儀」(圖4),從菠菜中純化出了3.3毫克tRNA。

圖4 為純化微量RNA自主研發的全自動往復循環層析圖儀系統,從中可見研究團隊為推進RNA修飾研究做出的技術創新。
此外,研究團隊還證實,此次發現的修飾在蛋白質合成過程中起到了不可或缺的作用。鈴木教授笑著說:「有人可能會覺得,40公斤材料只能提取3.3毫克的tRNA嗎?但其實這種材料利用率已經算好的了。」上述通過調控tRNA功能的重要研究成果,將有助於植物的培育以及對病原菌感染性疾病的治療。
同年12月,研究團隊在全球首次發現,在低氧環境下,大腸桿菌的核糖體RNA(rRNA)中「RNA骨架」會發生甲基化修飾。這種新型的骨架甲基化能微調控核糖體的結構與活性,提高低氧環境下的翻譯效率,起到促進生長的「環境響應型開關」作用。該成果揭示了RNA修飾感知生長環境、調控蛋白質合成的全新機制,同時也有望為無細胞蛋白質合成以及合成生物學研究提供重要的技術基礎。
鑑定出兩種「加糖」的酶
對生物健康成長不可或缺
作為「解析」方向的研究成果之一,鈴木教授團隊於2023年在《Cell》雜誌上發表了「tRNA的糖修飾調控蛋白質合成速度」。該研究鑑定出了兩種分別將半乳糖和甘露糖這兩種糖添加到tRNA上的酶,並闡明瞭其分子基礎構造。此外,研究還表明,這些修飾能夠調控蛋白質合成速度,通過小型熱帶魚斑馬魚的實驗證實,其對生物的健康成長至關重要。
部分tRNA的第34位鹼基發生了特殊修飾,修飾後的鹼基還會進一步添加半乳糖或甘露糖。這一現象早在1976年就被發現,但其詳細機制和功能此前一直不明。鈴木教授研究室的兩名研究生分別發現了向該修飾鹼基添加半乳糖的酶「QTGAL」和添加甘露糖的酶「QTMAN」,細胞實驗證實,若缺乏這些酶,mRNA合成蛋白質的翻譯速度會加快,且新生蛋白質無法正確摺疊。也就是說,tRNA的糖基化修飾通過調控蛋白質合成速度,維持適當的翻譯速度,從而有助於維持蛋白質的質量和機能。
此外,通過斑馬魚實驗發現,無法遺傳繼承這些酶的個體,出生後的生長速度會變慢,體長也會變短。翻譯速度並非越快越好,通過添加糖來適當調控翻譯速度,是生物健康生長的必要條件。
目前,研究團隊正在製備缺失引起該修飾的基因小鼠模型,以便研究這些酶的功能。此前,已有實驗結果顯示,缺失QTGAL的小鼠表現出在明亮環境中活動時間減少的焦慮傾向,而缺失QTMAN的雌性小鼠的活動量則出現增加。此外,缺失QTMAN的小鼠會呈現肥胖體型,鈴木教授的團隊目前正在詳細研究這些表型為何會因tRNA修飾缺失而產生。他表示:「這些酶可能與人類的疾病相關,比如精神病疾患、癌症等,我們希望進一步闡明其中的關聯。」
為治療粒線體病帶來新希望
開發使用奈米孔的全面檢測技術
「操控」方向的研究也取得了初步成果。鈴木團隊發現,由粒線體DNA突變引發的「粒線體腦肌病(MELAS病)」患者,其tRNA未發生牛磺酸修飾,並且,在使用MELAS病患者細胞進行的實驗中,成功恢復了tRNA的功能。
健康人群中,一種名為MTO1的酶會使tRNA的尿苷發生牛磺酸修飾。但在MELAS病患者中,由於tRNA中本應是腺嘌呤的鹼基變成了鳥嘌呤,導致MTO1無法識別tRNA,尿苷無法發生牛磺酸修飾。鈴木教授等通過過量表達MTO1使其在細胞內大量產生,成功恢復了tRNA的牛磺酸修飾,同時顯著提升了細胞的蛋白質合成及呼吸活性(圖5)。
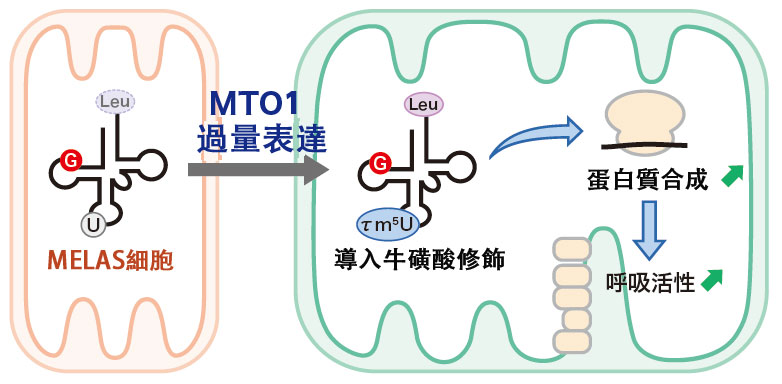
圖5 鈴木教授的團隊通過過量表達MTO1,成功將本應存在的牛磺酸修飾(τm5U)導入tRNA,恢復了粒線體功能。白胺酸(Leu)是構成蛋白質的20種氨基酸之一。
MELAS病是一種類似腦卒中發作的疑難病症,此前一直缺乏有效療法,預後效果較差。鈴木團隊目前正與東京大學醫科學研究所的岡田尚巳教授合作,研究使用腺相關病毒的MELAS病基因療法,這一研究為難以通過基因組編輯治療的粒線體病帶來了新的治療希望。
在進行上述研究的同時,鈴木教授團隊還在推進開發RNA修飾的檢測技術。其中一項重要技術是使用名為「奈米孔測序儀」的裝置進行tRNA修飾的單分子解析。在奈米孔測序儀解析中,將RNA拉伸成單鏈狀態,使其通過由膜蛋白構成的被稱為奈米孔的微孔,通過此時電流的變化來解析鹼基序列。
鈴木教授團隊注意到,RNA修飾在通過奈米孔時會表現出特徵性電流值。通過機器學習各tRNA通過時產生的特徵性電流波形模式,不僅能解析鹼基序列,還能在單分子水平上檢測tRNA修飾的存在與否及修飾比例。全面檢測tRNA修飾,將為闡明疾病成因、開展疾病診斷提供重要依據。
中心法則中RNA的作用,是高中教材中也會講解的基礎知識點。但教材中幾乎未提及RNA修飾這一靈活的調控機制,也未介紹RNA修飾異常與疾病的關聯,可以說,這是一個全新的研究領域。相信在本項目結束後,通過深入推進RNA修飾的研究,將進一步推動對生命現象的理解和醫療應用。(TEXT:島田祥輔 PHOTO:上樂博之)

原文:JSTnews 2026年2月號
翻譯:JST客觀日本編輯部