日本國立研究開發法人量子科學技術研究開發機構(QST)量子醫科學研究所先進核醫學基礎研究部的張明榮部長、謝琳主幹研究員等成功研發出了以癌細胞表面代謝型麩胺酸1型接受者(mGluR1)為靶點的診療一體化藥劑。這是一種將診斷(Diagnosis)與治療(Therapy)一體化的新型醫療技術,不僅可在治療前預測療效,還能利用α射線與β射線從實體層面強力殺傷癌細胞。該成果有望成為可應對多種癌症、強效且安全的個性化醫療方案。相關研究成果已發表在《Molecular Therapy》的3月11日刊上。
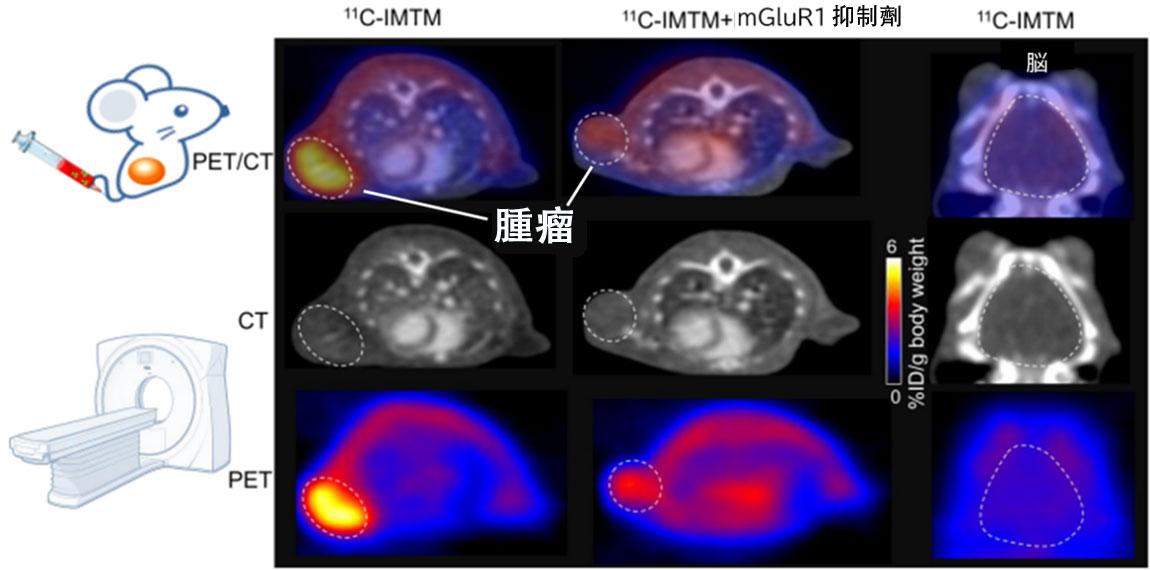
圖1 給惡性黑色素瘤小鼠模型注射11C-IMTM後拍攝的PET圖像(供圖:量子科學技術研究開發機構(QST))
診療一體化是將診斷與治療相結合的新型醫療技術。應用於核醫學領域的放射性診療一體化技術,使用可靶向聚集於癌細胞表面分子的抗體或藥物(分子靶向藥),並結合γ射線核素或PET(正電子發射斷層顯像)核素製成的診斷藥物,進行影像檢查,隨後將藥物結合的核素替換為α射線或β射線核素進行治療。
PET是一種通過向受檢者注射藥物,檢測藥物釋放的正電子所產生的γ射線,從而對體內深部生物物質的分佈與量等進行成像的診斷方法。由於可以確認癌症狀態及藥物的聚集程度,因此可在治療前預測療效。
α射線和β射線能夠以強大的能量損傷癌細胞的DNA,從而殺傷癌細胞。通過同一種藥物實現上述兩種功能,研究團隊開發出可同時完成診斷與治療的配對藥物——PET診斷藥物「11C-IMTM」與α射線靶向同位素治療藥物「211At-AMTM」。
當將該藥物投放至皮下移植了小鼠來源惡性黑色素瘤的模型小鼠並進行PET成像後,發現藥物高度聚集於腫瘤部位,證實其可用於診斷。同時藥物在與機體毒性密切相關的腦部和血液中聚集量較低,未發現安全性問題。
隨後,當給小鼠注射211At-AMTM後,確認到所有個體的腫瘤增殖均受到抑制,效果持續了10天。α射線靶向同位素治療藥物不僅對原發竈有效,也有望用於轉移竈治療。
為此,研究團隊製備了肺轉移小鼠模型並進行評估,結果顯示PET成像可清晰顯示肺轉移竈,且生存期延長了約2倍。此外,在對難治性癌症胰腺癌的評估中,也顯示出顯著的腫瘤增殖抑制效果,15隻小鼠中有7隻腫瘤消失。
治療藥物中使用的砹(At)是一種鹵素元素,由於可通過迴旋加速器製備,因此成本較低且可在日本國內製造。單次照射就能確認到治療效果,對身體的負擔也較小。今後,研究團隊將力爭開展人體臨床試驗。
原文:《科學新聞》
翻譯:JST客觀日本編輯部
【論文資訊】
期刊:Molecular Therapy
論文:A mGluR1-targeted radiotheranostic strAtegy visualizes lesions and potentiAtes antitumor efficacy in melanoma and pancreAtic cancer
DOI:doi.org/10.1016/j.ymthe.2026.02.032