以胰腺癌、膽管癌等為代表的難治性癌症的特徵之一是在被稱為「間質」的癌細胞以外的區域,會出現數量超過癌細胞的癌症相關纖維母細胞(cancer-associated fibroblast:CAF)的反應性增生。在這類癌症中,可觀察到CAF圍繞癌細胞巢增生的表現。CAF是一類在膠原蛋白等細胞外基質的產生方面能力出眾的細胞,這些細胞外基質的沉積會誘導間質纖維化。已知纖維化引發的癌組織硬化會激活癌細胞,提升其增殖能力及侵襲能力。此外,還已知癌組織的纖維化及硬化會誘導腫瘤血管塌陷、缺血性微環境形成、藥物遞送效率下降以及免疫抑制性微環境的形成。

圖1 名古屋大學研究生院醫學系研究科的榎本篤教授(供圖:名古屋大學)
儘管過去此前曾嘗試開發抑制CAF增生、或是殺傷CAF的治療方法,但臨床試驗及臨床研究均未取得成功,因此殺傷及抑制CAF的戰略已到了重新審視的時期。我們轉變以往思路,旨在開發出一種新型治療方法,以自主鑑定的CAF標誌物分子為靶點的抗體藥物偶聯物(antibody-drug conjugates:ADC)向胰腺癌細胞高效遞送抗癌藥物。
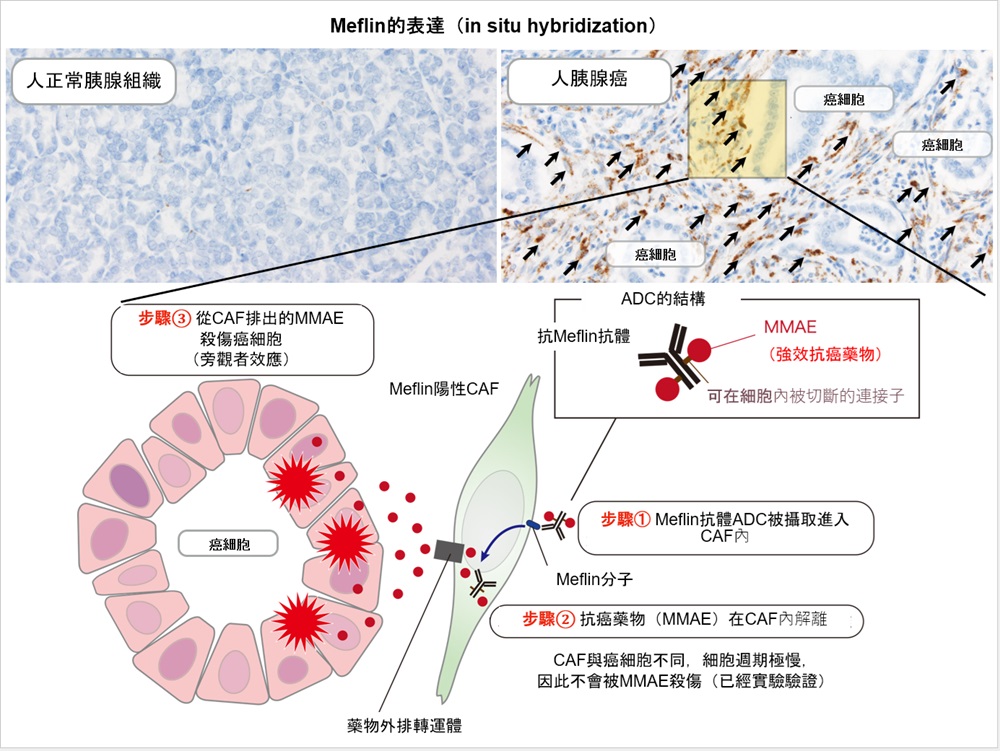
圖2 Meflin在人胰腺癌CAF中的表達及抗Meflin-ADC的藥效機制(供圖:名古屋大學)
本圖模式化地展示了本次研究課題旨在開發的抗Meflin-ADC的藥效機制。抗Meflin-ADC被Meflin陽性CAF攝取後,在CAF內釋放的酬載被排出至細胞外,進而殺傷周圍的癌細胞(旁觀者效應)。
我們於2019年,將胞外結構域帶有富白胺酸重複序列的GPI定錨型分子Meflin,鑑定為CAF最具特異性的膜分子標誌物。通過基因修飾小鼠、自發性癌症小鼠模型、人類病理組織樣本等開展的驗證,已逐步闡明Meflin陽性CAF極敏銳地聚集於癌細胞周圍,在轉移竈的CAF中也有表達,且與其他CAF膜標誌物分子相比,顯示出較高的mRNA表達水平。除胰腺癌外,我們已確認該分子在膽管癌、大腸癌、肺癌、乳腺癌、尿路上皮癌、腎癌等多種伴隨間質纖維化反應的癌症中,均特異性表達於CAF。同時我們也證實,Meflin雖在正常組織的間質細胞中也有表達,但其表達水平遠低於CAF。
迄今為止,我們已獲得多株抗Meflin單源抗體,並製備了通過連接子在這些抗體上偶聯酬載的ADC(以下簡稱抗Meflin-ADC)。截至目前,我們已在多個荷瘤小鼠模型中發現,抗Meflin-ADC具有顯著的抗腫瘤效果。
我們預期,抗Meflin-ADC的藥效機制,是ADC被攝取進入CAF細胞後,經蛋白酶從ADC上釋放的酬載通過藥物外排轉運體被排出至細胞外、進而殺傷鄰近癌細胞的「旁觀者(Bystander)效應」。此時CAF不會被殺傷,這一點已在採用培養細胞的實驗體系中得到確認。
基於上述驗證結果,我們設定的目標為:驗證抗Meflin-ADC療法相較於現有細胞毒性抗癌藥物的優勢,以及旁觀者效應的詳細藥理機制;開展采用GMP級ADC的安全性試驗法,以及啟動針對不可切除進展期胰腺癌患者的I期臨床試驗。
現已證實,Meflin陽性CAF在絕大多數伴隨間質纖維化反應的癌症中均可觀察到。此外,與伴隨抗癌治療的擇汰壓力力或病程進展,不斷獲得治療抗藥性或積累基因突變的癌細胞不同,已知CAF的表型十分穩定。我們期待未來有一天,抗Meflin-ADC能夠廣泛應用於上述多種癌症,或是已對其他治療藥物產生抗藥性的癌症。
原文:《科學新聞》
翻譯:JST客觀日本編輯部