日本九州大學研究生院醫學研究院的今井猛主幹教授、稻垣成矩助教與鹿兒島大學、山梨大學等組成的研究團隊,在全球首次成功實現了小鼠大腦的活體透明化,並在保持生物功能的前提下實現了反復觀察。今井主幹教授表示:「十幾年前,我們對小鼠死後標本進行透明化處理時,常被問及何時能實現活體透明化,如今終於成功了。這種方法可以在不影響大腦功能的情況下實現觀察,希望該技術今後能廣泛應用於各類研究。」相關成果已發表在《Nature Methods》上。
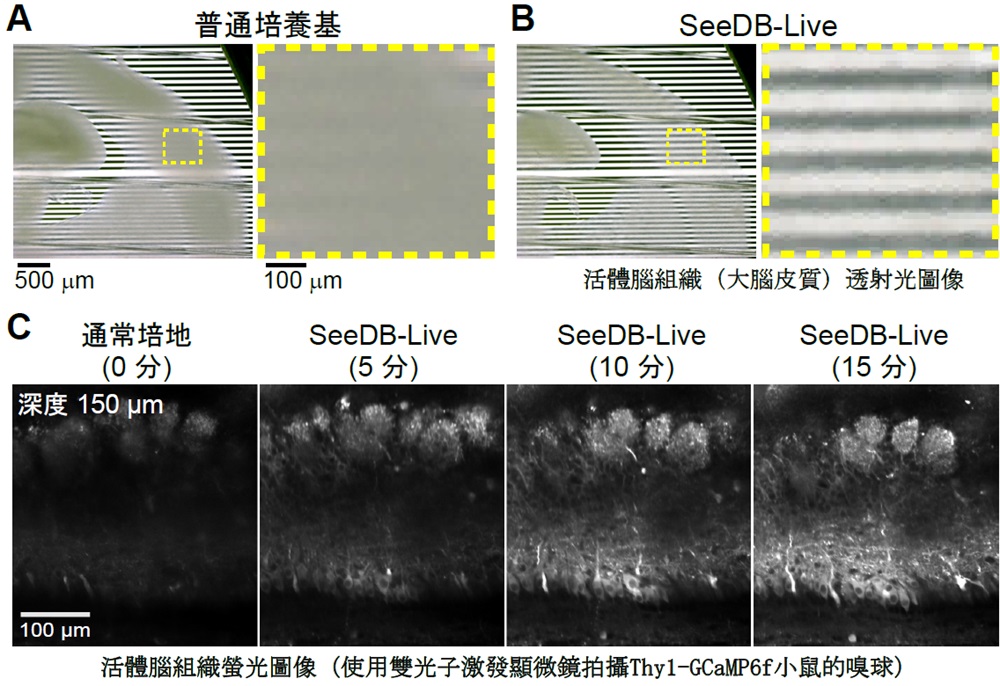
圖1 活體腦組織的透明化(供圖:九州大學稻垣成矩助教、今井猛教授)
(A, B)為活體腦組織(厚度300微米的剖切)的透明化。出生後第5天小鼠的大腦皮質分別浸入普通培養基(人工腦脊髓液)(A)和SeeDB-Live(B)中約1小時後的活體腦組織的透射光圖像。透明化後的腦組織可清晰地觀察到標本下方的條紋圖案;(C)為活體腦組織(出生9天小鼠的嗅球)的螢光鈣檢測。研究人員使用雙光子激發顯微鏡,對神經細胞中表達螢光鈣感測器GCaMP6f的轉基因小鼠Thy1-GCaMP6f的腦剖切進行了螢光檢測。將普通培養基更換為SeeDB-Live後,腦組織逐漸透明化,能夠觀測到深部神經細胞的熒燈火信號。
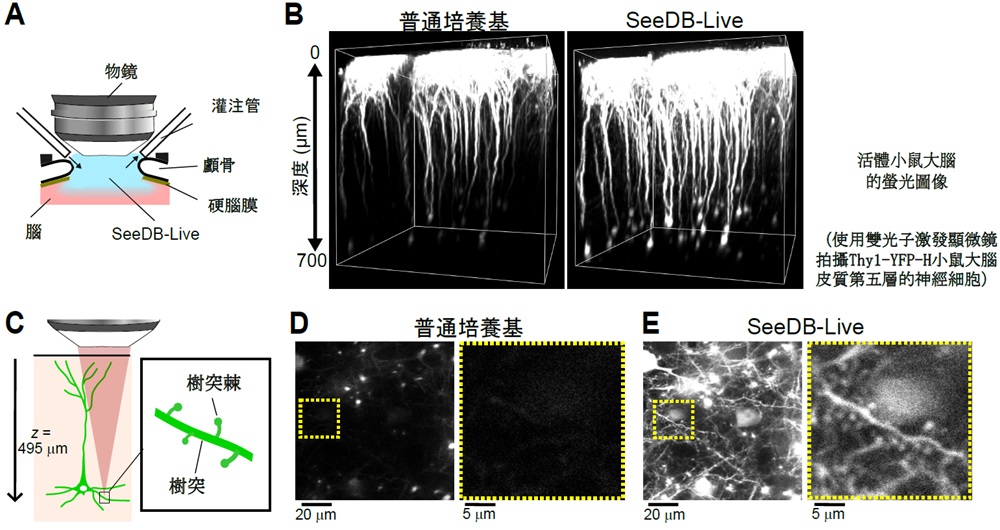
圖6 活體動物大腦的透明化(供圖:九州大學稻垣成矩助教、今井猛教授)
(A)活體小鼠大腦透明化。在感覺缺失狀態下的小鼠腦表面持續灌注SeeDB-Live 1小時,使其滲透,進行透明化處理;(B)大腦皮質第五層神經細胞的三維螢光圖像。使用雙光子激發顯微鏡,對神經細胞中表達螢光蛋白的(Thy1-EYFP-H)小鼠進行拍攝。與透明化前相比,透明化後腦深部熒光度顯著提升;(C-E)大腦皮質第五層神經細胞樹突及樹突棘(C);與透明化前(D)相比,透明化後(E)熒光度提升,能夠更清晰地觀察到樹突和樹突棘的螢光圖像。
活體組織呈現不透明的主要原因,是光線在細胞內外發生折射與散射,無法直線傳播所致。以往的透明化試劑濃度較高,會因滲透壓導致細胞脫水死亡。
研究團隊使用多種分子篩選最佳透明化試劑。結果發現,在細胞外液中添加白蛋白,可抑制光的折射與散射,實現對活體組織的非侵入性透明化。白蛋白幾乎不改變細胞外液的離子組成,也沒有細胞毒性。由此,研究團隊全球首次實現了在組織透明化狀態下,並使用螢光顯微鏡觀察組織內細胞的正常功能。
稻垣助教表示:「我們從2021年左右著手研究,數月後便發現球狀聚合體效果較好。但候選分子會對細胞功能產生不良影響,研究因此停滯了約一年。某天深夜獨自做實驗時,想著反正沒人,就試用了純度高的昂貴白蛋白試劑,最終取得了成功。」
經過活細胞等實驗驗證,研究團隊將研發的透明化試劑SeeDB-Live導入活體小鼠大腦,成功通過螢光顯微鏡觀察至大腦第五層。大腦透明化的小鼠在歷經4個月以上的反復實驗後仍保持健康。研究團隊表示,未來將通過優化滲透方式,實現對大腦更深水層次的觀察。
原文:《科學新聞》
翻譯:JST客觀日本編輯部
【論文資訊】
期刊:Nature Methods
論文:Isotonic and minimally invasive optical clearing media for live cell imaging ex vivo and in vivo
DOI:10.1038/s41592-026-03023-y













