片桐 秀樹
東北大學 研究生院醫學系研究科 教授
2020年起擔任登月型研究開發事業目標2 項目主管
糖尿病是一種病程在無自覺症狀的狀態下持續進展,一旦惡化便會引發並發症的嚴重疾病。目前的治療主要通過持續注射胰島素、口服藥物控制血糖水平,至今還沒有根本性的治療方法。因此,早期發現與預防至關重要。日本東北大學研究生院醫學系研究科的片桐秀樹教授統籌負責一項聚焦由腦和神經所介導的「器官間網路」、旨在攻克糖尿病的項目。為實現「即便不採血檢查也能在超早期檢出糖尿病,並可從源頭預防發病的社會」, 片桐教授的團隊正朝著這個目標努力。
日本國內患者與前期人群約2000萬人
一旦發病,就很難治癒
糖尿病是一種血液中葡萄糖濃度慢性升高的疾病。人體內由胰腺中散在分佈的島狀細胞聚集而成的「朗格漢斯島」β細胞,會分泌名為「胰島素」的激素調節血糖。然而,患上糖尿病後,就會出現無法合成足量的胰島素,或是胰島素效果無法正常發揮的情況。糖尿病目前尚無根本性療法,目前主要的治療手段是只能通過飲食、運動、服藥等方式控制血糖,使血糖值接近正常範圍。在日本,以生活習慣為主要誘因的2型糖尿病佔糖尿病總體病例的九成以上。
據估算,日本國內的糖尿病患者,與血糖水平略高於正常值、糖尿病發病風險較高的「糖尿病前期人群」合計約達2000萬人。多數情況下,該病在無自覺症狀的狀態下持續進展,一旦病情惡化便會引發失明、腎衰竭等並發症,以及心力衰竭等嚴重疾病。其結果不僅會縮短患者的健康壽命、降低生活品質,還會因醫療費用增長、護理需求增加,給整個社會造成巨大損失。
針對這一問題,東北大學教授片桐秀樹作為JST(日本國立研究開發法人科學技術振興機構)登月型研究開發事業目標2「2050年建成可實現疾病超早期預測與預防的社會」中所包含的研究項目之一「通過對恆常性的理解與調控來攻克糖尿病及其伴發疾病」的項目主管,正在推進糖尿病超早期發現與發病預防的相關研究。本文將對該項目取得的成果進行介紹。
同時與醫學以外的多元領域開展合作
聚焦於腦和神經的獨特視角
片桐教授研究團隊的最終目標,是實現即便不反復採血檢查,也能夠獲取糖尿病及其並發症的相關資訊,進而能夠對糖尿病做到超早期發現,或是採取預防發病的相關措施。為此,研究團隊不僅與醫學界的各領域開展合作,還正與藥學、資訊科學、工學、數學等各領域的研究學者合作推進項目。其實項目成員中包括片桐教授在內的專科醫生僅數人。「為攻克僅憑糖尿病研究者無法解決的課題,我們邀請了其他掌握必要技術與知識的人士參與其中。通過引入醫療專業以外的視角,研討也變得活躍起來」,片桐教授闡述了多元性的重要性。
片桐教授申報登月型研究開發事業的理由之一,是認為該項目能夠充分應用自己長年以來一直倡導的「器官間網路」的研究成果。所謂器官間網路,是一種「大腦收集全身臟器與器官的資訊並發出指令,以此維持代謝平衡」的構想。由於這類資訊也可經由神經進行交互,因此聚焦神經系統、闡明糖尿病病理機制、開發超早期預測與預防方法,便成為了該項目的獨特視角。
片桐教授一直關注於對維持機體內環境恆定的「恆常性」,並將糖尿病解釋為「代謝發生了極其微小變化的狀態」。據悉,健康人群空腹狀態下,全身血液中的葡萄糖含量約為4克,降至3克即為低血糖,超過6克則可診斷為糖尿病。片桐教授談及研究契機時表示:「我的研究始於闡明對葡萄糖進行精密控制的這類代謝機制的想法。」
藉助AI與心電圖預測心力衰竭
實現並發症的居家管理
糖尿病並發症包括高血壓、心臟泵血功能下降的心力衰竭等。心力衰竭是危及生命的疾病,連同糖尿病在內,這些並發症的早期發現也是重要的研究課題。片桐教授團隊正在推進使用人工智慧(AI),利用即便在家中也可使用的測量設備來捕捉並發症前兆的研究。
心力衰竭的惡化大多發生於家中。針對這一問題,項目成員之一、東京大學研究生院醫學系研究科及東京科學大學難治性疾病研究所的藤生克仁特任教授等人,活用學習超過9500例心電圖數據的AI模型,開發出了可對心力衰竭嚴重程度進行分類的、名為「HF指數」的指標。團隊證實,當基於可在家中使用的攜帶型心電圖儀或腕錶型器件所測得的心電圖計算出HF指數時,便能夠高精度地診斷心力衰竭的惡化與發病。
臨床一般通過血液檢查測定「腦性(B型)鈉利尿肽(BNP)」作為心力衰竭的指標。但研究表明,HF指數能夠達到BNP的同等水平,甚至更為靈敏地檢測出心力衰竭(圖1)。通過應用該系統,有望實現心力衰竭的居家早期發現,並推動遠端醫療的發展。
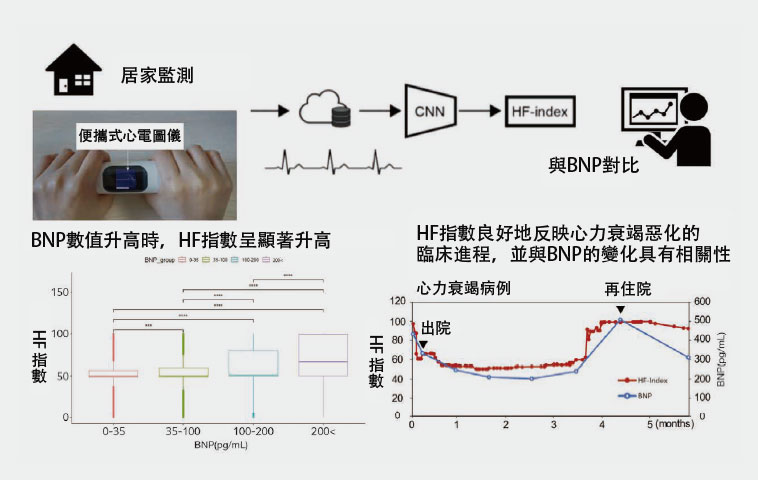
圖1 研究證實,基於心力衰竭數據計算得到的原創指標HF指數,可比BNP濃度上升更早地檢測出心力衰竭的惡化,可有效用於心力衰竭的居家管理。
受該研究啟發,東京科學大學研究生院醫齒學綜合研究科的山田哲也教授,成功開發出一種能夠通過可在家裏使用的攜帶型·腕錶型心電圖儀,高靈敏度檢測出糖尿病超早期階段。
此外,藤生教授還利用一種名為目標光譜相機的特殊相機,開發出僅需拍攝臉部與手掌5秒即可檢測出高血壓的AI模型。該模型通過測定皮膚的反射光譜,以AI分析高血壓的特徵性波長數據,從而以非侵入式方式實現健康狀態的數值化與視覺化。在對該模型進行優化升級後,團隊也成功實現了超早期階段糖尿病狀態的檢測。該成果曾在2025年的大阪・關西世博會上展出,參觀者實際體驗了非接觸式健康診斷(圖2)。上述所有成果,均有助於在日常生活中實現糖尿病及其伴發疾病發病的早期檢出。

圖2 大阪·關西世博會上展出的「來體驗融入日常街頭的未來健康診斷」展項(左)。只需將臉部對準安裝在反射面型數字標示牌(右)上的相機數秒,即可檢測出心跳、血壓乃至糖尿病的狀態。
刺激迷走神經增加胰島素分泌
將在癲癇患者中開展驗證
即便能夠檢測,若不能預防,其意義也是受到很大限制。片桐教授在圍繞胰腺β細胞增加法作為糖尿病預防治療方法的研究中,取得了劃時代的成果。他此前通過小鼠實驗,闡明瞭由肝臟-腦-胰腺這一神經系統構成的器官間網路對胰腺β細胞數量的調節機制。該機制具體而言就是,當血糖值上升時,肝臟中一種稱為細胞外信號調節激酶的酶會被激活,該信號通過神經傳遞至大腦,來自大腦的資訊再通過名為迷走神經的自律神經傳遞至胰腺,從而促進β細胞的增加。
在本次項目中,研究團隊更進一步,嘗試開展了以糖尿病預防為預設的實驗。首先,團隊製備了經基因改造、可通過藍光刺激激活從大腦延伸至胰腺的迷走神經的小鼠,並對其進行修飾,使其在受到近紅外光光照射時胰腺會呈現藍色。對該小鼠照射近紅外光光並給予葡萄糖後,發現其胰島素分泌量增加,血糖上升得到抑制。此外研究還發現,若持續進行光刺激兩周,β細胞的數量會增加至兩倍以上(圖3)。這表明,通過僅刺激與胰腺相連的迷走神經,能夠在質和量兩方面激活β細胞,進而增加血液中的胰島素含量。
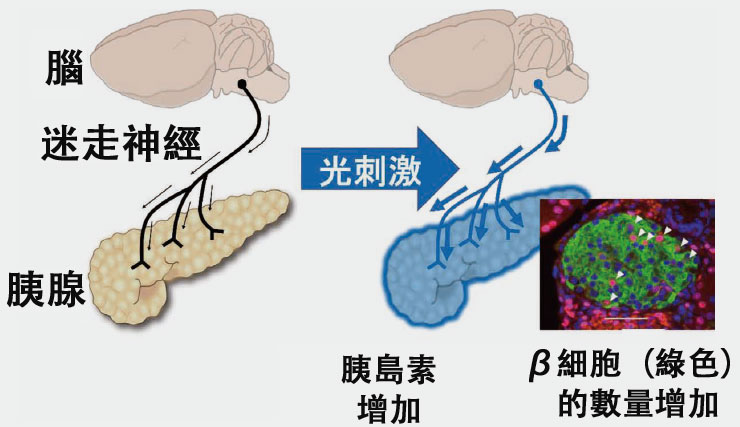
圖3 對基因改造小鼠照射近紅外光光使胰腺呈現藍色後,連接胰腺的迷走神經被激活,β細胞數量增加。白色箭尖所指粉色部分為增多的β細胞核。
上述實驗由於進行了基因改造,因此無法直接用在實際的患者身上。另一方面,一部分癲癇患者為治療已植入迷走神經電刺激裝置。研究團隊已尋求此類患者的協助,開展一項通過名為「升糖素負荷試驗」的檢測方法測定β細胞數量的臨床研究,進而確認在人體中,迷走神經刺激是否真的能讓β細胞增多。
與此同時,研究團隊還在研發增加β細胞的口服劑和營養補充劑作為更簡便的方法。片桐教授等人表示,目前已找到幾種候選化合物。
長達40年的追蹤調查證實
抑制餐後血糖可降低風險
目前糖尿病的診斷,均依據空腹攝入75克葡萄糖並測定一定時間後血糖值的「葡萄糖負荷試驗」所對應的標準值開展。然而,即便處於糖尿病發病前被認定為「正常」的血糖範圍內,是否仍存在能進一步降低死亡風險的區間,此前尚不明確。為此,片桐教授等人運用自1986年以來持續針對岩手縣大迫町(現花捲市)普通居民實施的追蹤調查數據開展了長期探討。該追蹤調查圍繞高血壓及循環系統疾病展開,以4年一次的頻率進行葡萄糖負荷試驗。研究以糖耐量正常、平均年齡62歲的地區居民為對象,分析葡萄糖負荷試驗中血糖值與壽命的關聯。結果顯示,葡萄糖攝入1小時後血糖值超過每分升170毫克(mg/dL)的組,在後續20年間的死亡率顯著高於血糖值低於該數值的組(圖4)。研究還顯示,就死亡原因而言,動脈硬化與惡性腫瘤相關死亡亦有所增加。
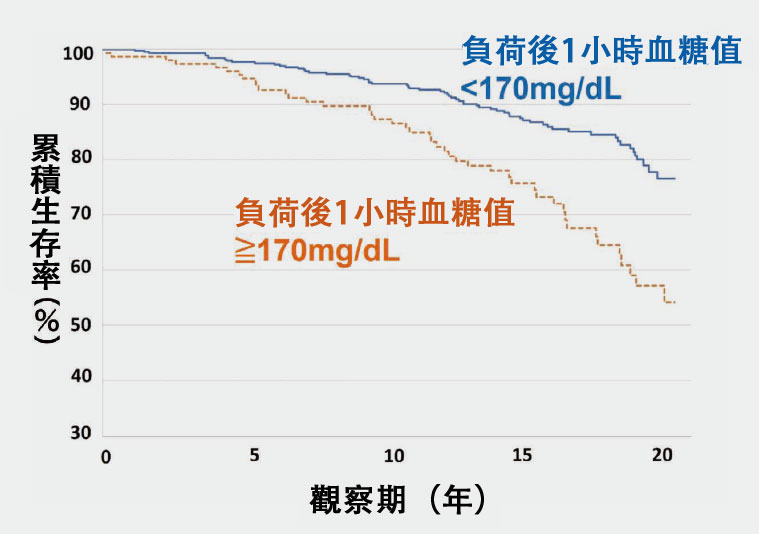
圖4 在調查開始時為健康者的人群當中,糖負荷試驗後1小時血糖值超過170mg/dL的人群,與未達該數值的人群相比,20年後的生存率顯著降低。
這個結果說明,餐後血糖值上升與動脈硬化及惡性腫瘤的發病之間可能存在共同機制,目前片桐教授等人正在研究以闡明該機制。此項研究有望為預防動脈硬化及惡性腫瘤、延長健康壽命提供支持,據信將帶來巨大影響。
中年發福的原因之一或為神經細胞
運動中的能量來源機制也已闡明
除此之外,片桐教授的項目還逐步揭示了多種體內臟器和器官互利共生並調節代謝平衡的現象。隨著年齡增長而感到難以瘦下來的人想必不在少數。其原因之一,或許就在於大腦神經細胞延伸出的突起長度。
在生物體內,存在一套「當體內脂肪蓄積時,脂肪細胞會分泌一種名為瘦素的激素來提升代謝量與脂肪燃燒量,並抑制食慾」的機制。瘦素作用於大腦下視丘的神經細胞後,該神經細胞會分泌一種名為黑皮質素的分子,該分子被其他神經細胞上的黑皮質素4型接受者(MC4R)蛋白接收後,便會起到促進代謝、抑制食慾的作用。
MC4R並非分佈在整個神經細胞上,僅存在於神經細胞像天線一樣向外延伸的「初級纖毛」表面。對此,名古屋大學研究生院醫學系研究科的中村和弘教授等人已發現,大鼠體內帶有MC4R的初級纖毛會隨年齡增長逐漸縮短;通過基因編輯強制縮短初級纖毛後,大鼠的攝食量增加,體重與體脂率也有所增加(圖5)。目前,團隊正推進相關研究,探索能否通過給藥延長初級纖毛。
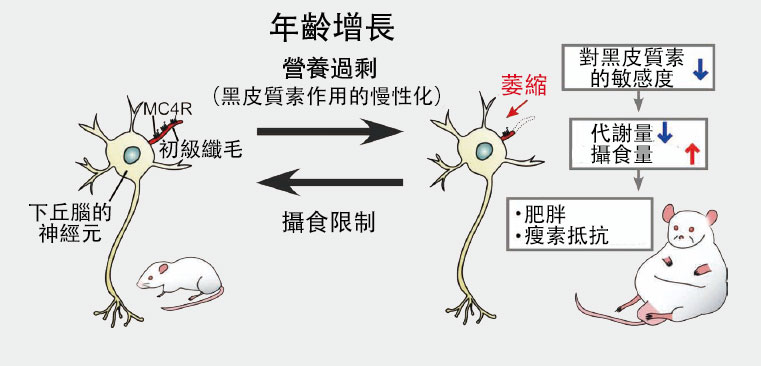
圖5 隨著年齡增長,神經細胞延伸出的初級纖毛會縮短,機體對黑皮質素的敏感度下降,進而導致代謝量降低,同時攝食量增加。
此外,儘管運動被認為對於改善肥胖有效,團隊還闡明瞭不同運動強度下機體對能量來源的差異化利用現象。肝臟內會發生一種從非碳水化合物物質中合成葡萄糖的「糖異生」反應。片桐教授等人通過小鼠實驗發現,在慢跑低強度運動中,機體以脂肪組織來源的甘油為糖異生的原料;而在快跑高強度運動中,機體則以肌肉來源的乳酸為糖異生的原料。對這一機制的調控,有望助力開發出提升運動能力、改善肥胖、預防肌少症的新方法。對於老年人而言,維持肌肉量至關重要,因此聚焦肝臟的糖異生現象,有望助力開發出在維持肌肉的同時高效燃燒脂肪的運動療法與運動輔助製劑。
迄今為止,片桐教授除了自己參與的合作研究之外,還作為項目主管充分施展了才幹。他回顧道:「能夠與日本頂尖研究學者組成的項目成員深入交流探討,我深感榮幸;我也始終懷著強烈的使命感推進合作,包括將不同領域研究者的成果對接為項目內的合作研究等事宜。」
如今,為期10年的項目已過半,片桐教授充滿幹勁地表示,將在後半段的5年中活用這些合作,進一步完善AI與數理模型解析工作。「例如,我們正在開發糖負荷試驗及血液循環的模擬器,目標是能夠準確預測血糖值和胰島素濃度的變化,並評估各臟器的代謝狀態。」此外,著眼於研究的傳承,他已任命3名項目參與者擔任子項目主管。目前團隊正舉全員之力,為確保最終目標——「2050年實現糖尿病及伴發疾病的超早期發現與預防」——的實現,穩步推進各項工作。
(TEXT:島田祥輔、PHOTO:島本繪梨佳)

原文:JSTnews 2026年4月號
翻譯:JST客觀日本編輯部