東京大學研究生院新領域創成科學研究科的鈴木邦律教授與北海道大學基因病控制研究所的野田展生教授等人組成的研究團隊,首次在活細胞中明確了橋狀脂質轉運蛋白Atg2在細胞內胞器之間雙向轉運脂質的過程。相關研究成果已發表在期刊《Journal of Cell Biology》上。
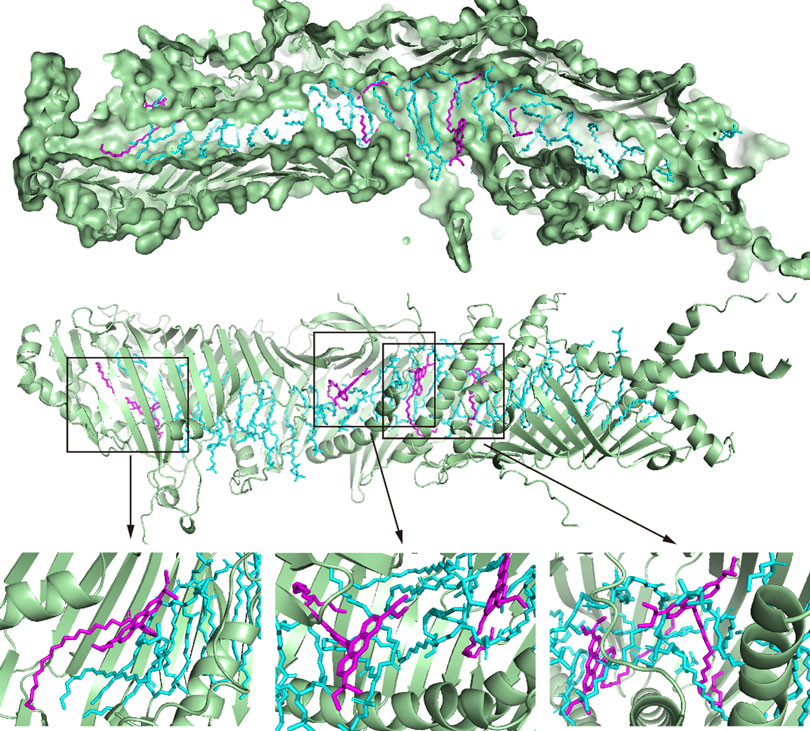
圖1 含磷脂的Atg2結構預測
研究團隊使用AlphaFold3預測了包含磷脂的Atg2三維結構。Atg2(綠色)、磷脂(青色)、R18(紫紅色)。(供圖:東京大學)
細胞內部存在大量承擔特定功能的胞器,它們被由脂質構成的膜所包裹。當細胞面臨營養飢餓等壓力時,膜會包裹並分解胞器的一部分,作為營養物質重新利用,這被稱作自噬過程。在此過程中,細胞內會形成一種名為隔離膜(自噬體)的新生膜,該膜呈片狀延展,包裹細胞內的代謝廢物。要擴大這層膜,需要大量的脂質,但由於此前缺乏能在活細胞中追蹤脂質動態的合適標記(探針),脂質究竟從何處、以何種方式被轉運而來一直不清楚,是此前學術界的重大未解課題。
研究團隊採用一種結構與脂質高度相似的螢光染料——十八烷基玫瑰紅B(R18),首次將其導入活酵母細胞與哺乳動物細胞,並即時觀測了細胞內脂質的運動情況。結果發現,將R18加入細胞培養液後,其會先吸附於細胞表面,隨後被翻轉進入細胞膜,再被轉運至內質網,最終轉移到各級自噬相關膜結構上。
研究人員將R18作為追蹤脂質轉運的發光標記物,通過特殊顯微成像觀察證實,Atg2蛋白在內質網與隔離膜之間起著橋樑作用,高效介導脂質從內質網向隔離膜的轉運。此外,研究還發現當向細胞重新供給營養、人為終止自噬進程時,脂質轉運方向就會發生逆轉。停止擴張的隔離膜中的脂質,會通過Atg2這座「橋」被運回原來的內質網。
此前人們普遍認為Atg2僅能單向轉運脂質,而本次研究證實:Atg2可根據細胞所處環境(飢餓狀態或營養狀態),靈活實現「內質網向隔離膜」或「隔離膜向內質網」的脂質雙向轉運。這一成果有助於理解細胞如何在需要的時候將脂質運送到需要的地方,從而維持自身穩定狀態這一生命的基礎機制。該成果今後有望助力闡明與自噬異常相關的疾病機制,推動醫學與生物學研究實現進一步發展。
原文:《科學新聞》
翻譯:JST客觀日本編輯部
【論文資訊】
期刊:Journal of Cell Biology
論文:Reversible One-way Lipid Transfer at ER-Autophagosome Membrane Contact Sites via Atg2
DOI:10.1083/jcb.202506039