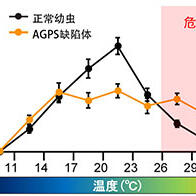
國立研究開發法人日本醫療研究開發機構(AMED)正在實施一項從2024年起為期5年的「智慧生物製藥研究支援事業」。為了從日本國內創製出革新性生物藥品,該項目以實現「向臨床試驗進階」為目標,共有19個項目正在推進之中,我們將針對這些「生物藥品的璞玉」採訪各個項目的負責人,為大家做系列報導。

鹿兒島大學研究生院理工學研究科教授伊東祐二(供圖:鹿兒島大學)
腦部及中樞症狀嚴重的遺傳性疾病,屬於醫療領域中最難治療的領域之一。即便是致病基因已經明確的疾病,由於按照常規給藥的方法,治療藥物難以充分抵達腦部,因此無法實現根治的病例不在少數。而橫亙於醫生面前的巨大障礙,就是存在於血液與大腦之間的「血腦障壁(BBB)」。
近年來,可抑制特定基因表現的核酸藥物作為腦遺傳性疾病頗具前景的治療手段受到關注。然而,核酸藥物若採取常規的靜脈注射,藥物難以穿透BBB向腦內移行,因此現階段採用的是蛛網膜下腔內給藥等對患者身體負擔較重的給藥方法。要攻克這一難題,高水平的藥物遞送技術(DDS)不可或缺。針對上述課題,我們在「智慧生物製藥研究支援事業」項目框架下推進研發的,正是「基於使用組織移行性抗體Accum Body的高功能性DDS的生物新藥研發」。
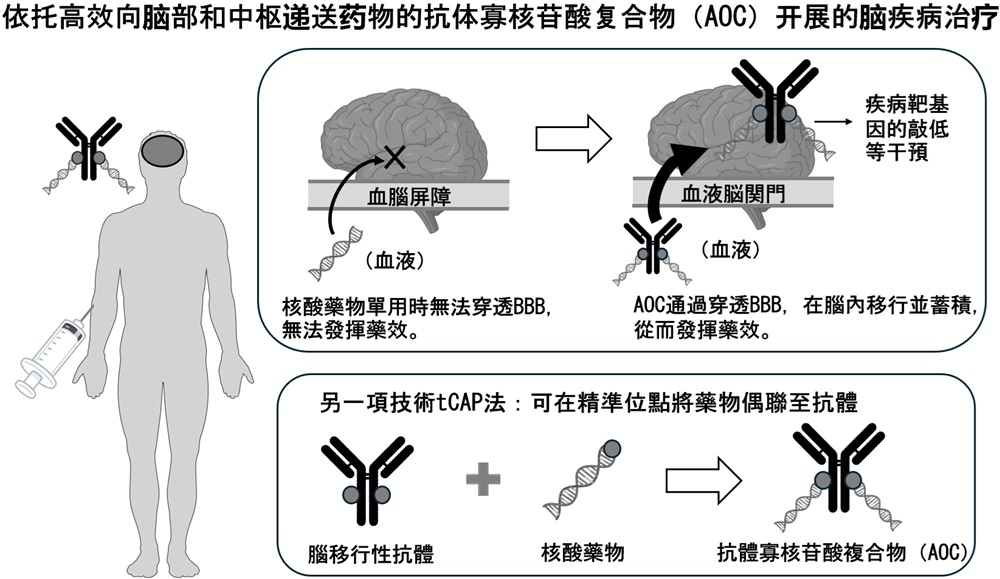
圖1研究概要圖(供圖:鹿兒島大學)
本研究的核心在於,開發出可將選擇性向腦部移行的抗體與具有治療效果的核酸藥物偶聯而得的「抗體寡核苷酸化合物(AOC)」,並由此開發出針對遺傳性腦疾病的新型治療藥物。研究思路的一大特徵是不將抗體作為‘藥物本身’,而是使其發揮「向腦部遞送核酸藥物的載體」的功能。本研究的基礎技術,是一種被稱作「腦Accum Body」的腦移行性抗體。腦Accum Body具備從血液中選擇性移行至腦組織、並在腦內高濃度蓄積的特性。AOC治療藥物通過將核酸藥物與腦Accum Body抗體結合,便可實現將核酸藥物高效地遞送至腦內,並對靶基因表現加以抑制。此外,本項目還成功開發出腦Accum Body的升級技術「腦Trans Accum Body」。腦Accum Body雖表現出較高的腦內蓄積性,但從血液向腦部移行的速度仍可以優化。為此,我們通過利用抗轉鐵蛋白接受者抗體穿透血腦障壁機制的抗體技術,提高了腦Accum Body從血液向腦內移行的效率,由此獲得的技術成果便是腦Trans Accum Body。藉助該項技術,有望將核酸藥物「更快、更多」地送至腦部,進一步提升治療效果。
支撐AOC技術實現的另一關鍵要素,則在於抗體與核酸藥物的偶聯技術。傳統方法會讓核酸隨機偶聯至抗體氨基或巰基,因此面臨性能參差不齊、抗體功能下降等問題。本研究攜手多肽研究所,合作開發出了一種僅針對抗體特定修飾位點(IgG抗體Fc區Lys248位點)的、被稱作「tCAP法」的位點特異性偶聯技術。tCAP法能夠在不損傷抗體功能的既定位置的條件下,以既定數量(1個或2個)偶聯核酸藥物,從而製備出品質均一、重現性高的AOC。
本研究以特定的腦遺傳性疾病為靶點,通過推進AOC藥物研發揭示上述技術於臨床中的有用性。本研究所採用的技術為可以拓展至各類疾病的「新藥研發平台」,為推進其產業化,我們已成立初創企業Accum Cap Technology,以腦Accum Body及腦Trans Accum Body為基礎的技術作為日本原創的革新性DDS,蘊藏著大幅改變未來腦疾病生物藥物研發模式的潛力。為直面腦疾病這一全球性課題,本項目希望助力日本原創高功能生物藥創製的實務舉措,戰略性地、紮實地推進現有研發種子進入臨床試驗的工作。
原文:《科學新聞》
翻譯:JST客觀日本編輯部