東京醫科齒科大學通過與東京大學的聯合研究發現,在部分惡性黑色素瘤(罕見且難治癒癌症)患者體內高度表達的白血球介素13接受者α2(IL13Rα2)會誘導形成癌細胞繁殖所需的新血管,由此加速腫瘤的形成。相關研究成果已於2月24日發布在國際學術雜誌《Scientific Reports》的網路版上。
【研究背景】
惡性黑色素瘤為皮膚癌的一種,被認為是體內負責產生黑色素的色料細胞和痣細胞發生癌變所致。惡性黑色素瘤的惡性程度非常高,發病早期就存在浸潤和轉移的現象,是難以治癒癌症的代表之一。主流治療方法是採用針對癌細胞繁殖性的抗癌藥物進行化療等,但問題是很多抗癌藥物都有副作用。惡性黑色素瘤領域也在推進分子靶向治療藥物的開發,以BRAF基因為靶點的維羅非尼(vemurafenib)等已投入使用,但也存在副作用。所以當務之急是確定新的靶向分子和查明癌症的惡化機制。不過,此前一直未確定在惡性黑色素瘤中進行獨特性表達並促進其惡化的細胞表面抗原。
【研究成果的概要】
研發小組為確定惡性黑色素瘤的新癌症抗原,此前探索了針對惡性黑色素瘤細胞A375的獨特性抗體,作為其抗原之一,鎖定了白血球介素13接受者α2(IL13Rα2)。另外,為研究IL13Rα2在惡性黑色素瘤患者體內的表達模式,利用組織微陣列和100多例病理標本進行了免疫組織染色,發現部分(約10%)患者的腫瘤組織内表達IL13Rα2(圖1)。此前已通過研究確認,在正常組織中,IL13Rα2隻在精巢中表達,而在惡性黑色素瘤中,IL13Rα2在癌細胞的細胞膜中表達,因此確定其為新型癌症標誌物。
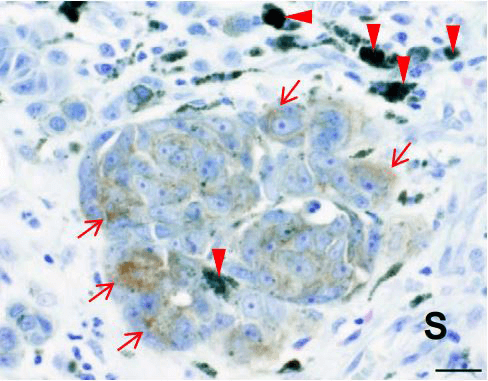
圖1:IL13Rα2在惡性黑色素瘤中的表達
採用惡性黑色素瘤組織對IL13Rα2進行免疫染色(褐色:紅色箭頭)。IL13Rα2僅在癌細胞中表達,未能在間質(S)中檢測出來 。紅色三角形箭頭:黑色素。比例尺:20μm
接下來,研發小組為了研究IL13Rα2在惡性黑色素瘤惡化過程中發揮的作用,使不表達IL13Rα2的惡性黑色素瘤細胞SK-MEL-28表達IL13Rα2(以下稱「IL13Rα2表達細胞」),然後將不表達IL13Rα2的SK-MEL28細胞作為控制細胞,比較了癌細胞的繁殖和腫瘤形成能力(圖2)。結果發現,在培養的細胞中,IL13Rα2表達細胞的繁殖速度比控制細胞低(圖2左),但對移植到免疫缺陷小鼠皮下後形成的腫瘤的尺寸進行比較發現,IL13Rα2表達細胞的腫瘤形成能力增強(圖2右)。另外,在表達IL13Rα2的惡性黑色素瘤細胞A375中,即使IL13Rα2基因缺失,也同樣觀察到了這種作用。
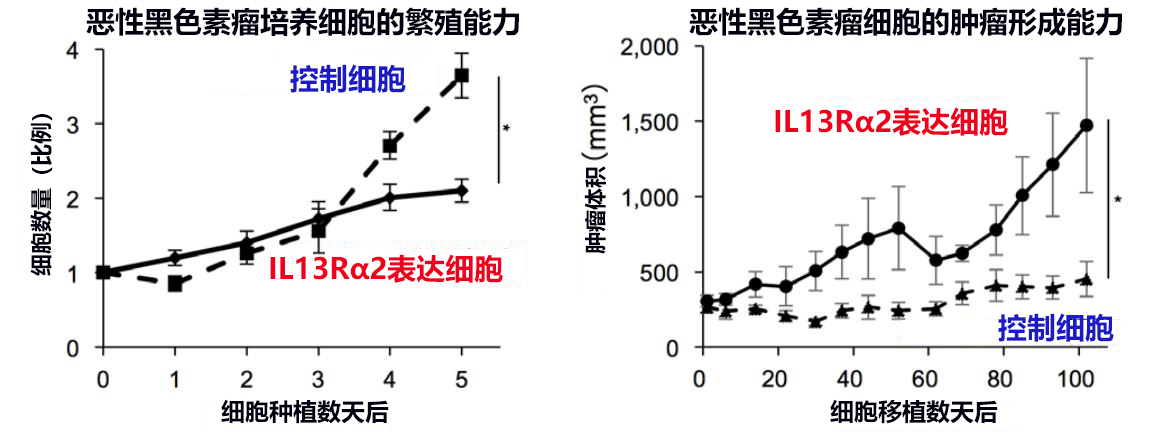
圖2:IL13Rα2在惡性黑色素瘤發展過程中發揮的作用
在癌症微環境中,除癌細胞外還存在血管和纖維母細胞等組成因子,這些組成因子具有促進腫瘤形成的作用。尤其是血管,通過為癌細胞提供繁殖所需的氧氣和營養,在腫瘤組織的生長中發揮著不可或缺的作用,研發小組為調查IL13Rα2通過新形成血管來促進腫瘤形成的可能性,利用針對血管內皮細胞標誌物PECAM-1的抗體,檢測了源自惡性黑色素瘤細胞的腫瘤組織中的血管形成情況。
檢測結果顯示,源自IL13Rα2表達細胞的腫瘤組織中的血管數量比源自控制細胞的腫瘤多。因此,研發小組綜合探索了通過表達IL13Rα2在惡性黑色素瘤細胞中誘導血管形成的因子,發現IL13Rα2會誘導表皮細胞成長因子(EGF)家族的Amphiregulin因子的表達。另外還發現,在惡性黑色素瘤細胞中,通過表達Amphiregulin,腫瘤形成能力和血管形成能力會增強,這表明,在惡性黑色素瘤細胞中,隨著血管形成因子Amphiregulin的表達增加,IL13Rα2會促進血管形成,從而加速腫瘤的形成(圖3)。
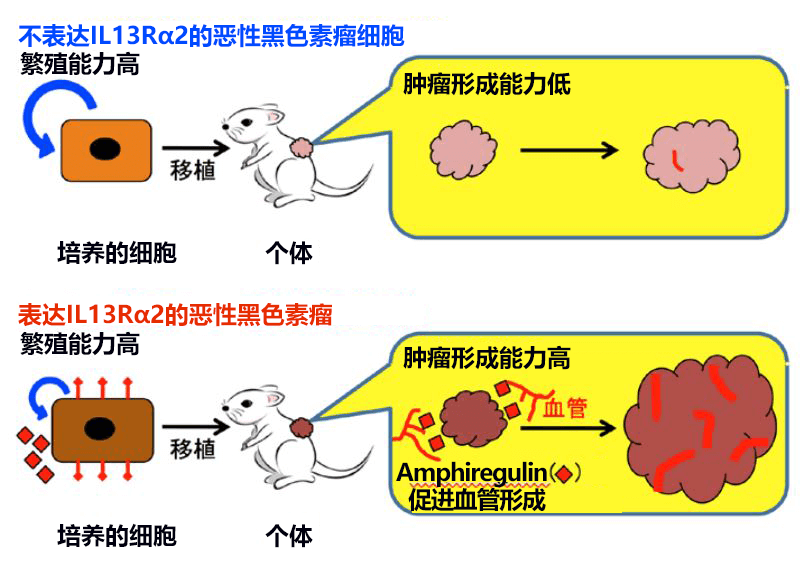
【研究成果的意義】
通過本次研究首次確認,IL13Rα2可作為惡性黑色素瘤的新型生物標誌物使用。在正常組織中,IL13Rα2隻在男性的生殖器官(精巢)中表達,而其他類型的癌症(惡性神經膠質瘤和胰腺癌等)中也未發現有IL13Rα2表達,所以被認為是表達量隨著細胞癌變而增加的癌症標誌物。由此,有望利用研發小組在本次研究之前確立的獨特性抗體等,開發以IL13Rα2為靶向的新型分子靶向療法。另外,此次還通過研究確認,在表達IL13Rα2的惡性黑色素瘤中,Amphiregulin等血管形成因子的表達增加會促進腫瘤形成,通過抑制IL13Rα2的作用,有望抑制惡性黑色素瘤的病情發展。
文 JST客觀日本編輯部














