2019年2月14日,國立大學法人東京醫科齒科大學(Tokyo Medical and Dental University, TMDU)發布新聞稿稱,該校大學院醫齒學綜合研究科的柿沼晴準教授、朝比奈靖浩教授、渡辺守教授等研究團隊,與東京大學、斯坦福大學、東海大學等共同研究建立了一個將人源iPS細胞誘導製備出肝星狀細胞的全新方法[1]。同時,該團隊發現iPS由來的肝星狀細胞有促進肝細胞成熟分化的功能,並詳細揭示了該功能的作用機制(圖1)。
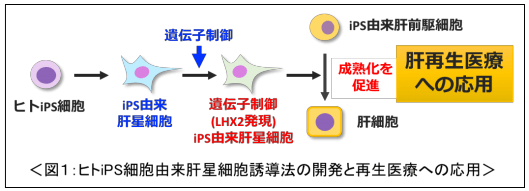
圖1 人源iPS細胞誘導成肝星狀細胞
該研究成果已線上發表於《Scientific Reports》(2019年2月14日)科學期刊上[文獻1]。
肝星狀細胞(hepatic stellate cells, HSCs),又稱貯脂細胞、伊東細胞,1956年由日本群馬大學醫學部伊東俊夫教授發現。星狀細胞位於肝臟的洞樣血管和幹細胞的竇周隙(Space of Disse)中,靜止期儲存身體絕大部分的維生素A和大量油脂。當肝臟創傷修復或慢性肝炎等發生時,星狀細胞被激活,是肝纖維化的主要成因(圖2)。肝纖維化和斑痕組織惡化,進而成為肝硬化。另外,星狀細胞與血栓性血小板減少性紫癜等疾病也關係密切。
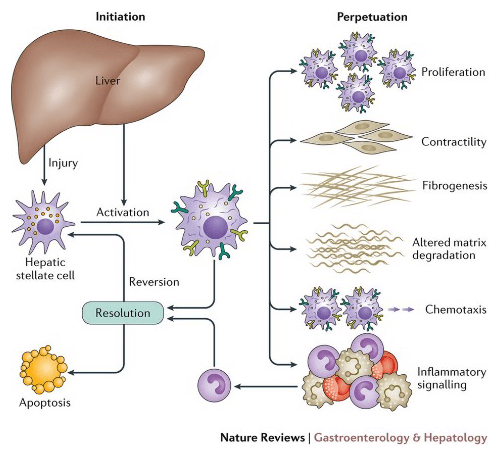
圖2 肝星狀細胞 (Nature Reviews)
研究團隊在人源iPS細胞培養過程中,通過添加特定成長因子和小分子化合物,成功誘導分化出了星狀細胞。在發炎刺激下,iPS細胞誘導而來的星狀細胞展現出人體天然星狀細胞類似的性能,轉化成了能最終導致肝硬化的肌纖維母細胞。當把星狀細胞與未成熟的iPS由來肝祖細胞共同培養時,成功促進了後者的機能成熟化進程。該發現將iPS細胞向肝臟再生醫療又推進了一步。
肝硬化患者因肝臟長期受到傷害最後導致機能失落,通常早期症狀不明顯,後期引起下肢水腫、皮膚泛黃、易淤青、蜘蛛痣、腹水等。據《柳葉刀》上的文獻數據顯示,2013年全球因肝硬化導致的死亡人數為120萬。其中,由於酒精、B型肝炎和C型肝炎造成的肝硬化死亡人數分別為38.4萬、31.7萬和35.8萬。目前對於進行性肝硬化和肝功能耗竭,除了肝臟移植,還沒有其他根治的方法。但和其他器官移植面臨的困境類似,供體的嚴重不足一直是難以解決的問題。
iPS細胞在再生醫學各領域嶄露頭角,儼然成為再生器官移植的重要出路。但是人源iPS細胞分化成的肝細胞,與人體原有的肝細胞相比較,在代謝機能等方面都表現出不成熟性。這也是iPS來源肝細胞走向臨床應用面臨的重要挑戰之一。
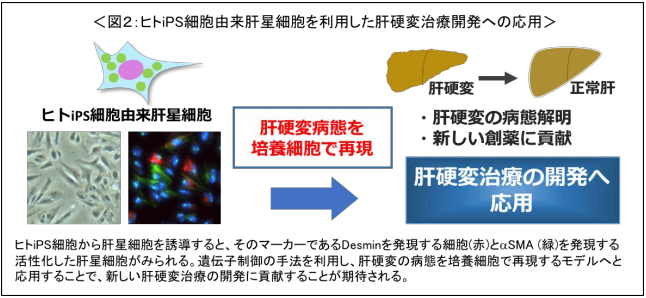
圖3 iPS細胞由來的肝星狀細胞用於肝硬化新藥研發
關於如何讓iPS細胞分化而來的肝細胞能夠進一步成熟化,研究團隊認為人體器官内各類細胞間的相輔作用極為重要。所以研究人員最終決定從肝臟間充質細胞之一的星狀細胞入手。不僅順利構建了星狀細胞製備的全新技術,同時如願發現了星狀細胞促進iPS細胞由來的肝細胞成熟化的機制。
本研究成果,不僅有助於應用iPS細胞的肝臟再生醫療的發展,而且有望通過各類iPS細胞誘導成的星狀細胞,加快針對肝硬化等疾病的新藥研發(圖3)。
供稿 宋傑 東京大學博士
編輯修改 JST客觀日本編輯部
參考文獻:
1 Masato Miyoshi, Sei Kakinuma, et al. LIM homeobox 2 promotes interaction between human iPS-derived hepatic progenitors and iPS-derived hepatic stellate-like cells. Scientific Reports. 9, Article number: 2072 (2019)
相關鏈結:
1. 東京醫科齒科大學新聞稿













