日本名古屋大學的研發小組與臺灣中央研究院和日本鳥取大學合作,共同查明瞭不同糖鏈控制神經軸突生長的分子機制。尤其是名為硫酸軟骨素(CS)的糖鏈,在發生脊髓傷害等外傷或腦梗塞等供血不足時,CS會在受損的軸突尖端誘導出名為Dystrophic endball(營養不良的端球)的異常球狀結構,並阻礙受損的神經軸突再生,這是全球首次在分子和細胞水平查明這種機制。
稱為神經細胞軸突的部位在人體內發揮著「輸電線」的作用,通過電信號傳遞各種資訊。輸電線有時會被「颱風」等刮斷,神經軸突也一樣,有時會因外傷等斷裂。斷裂了的輸電線能立即重新接上,但神經軸突無法二次再生。因為CS經由神經細胞接受者PTPRσ,將原本具備再生能力的軸突變成了名為Dystrophic endball的異常球狀結構,此部分為阻斷了其再生能力。
本次研究發現,PTPRσ會使名為Cortactin的分子去磷化,並抑制自噬流動,這是形成Dystrophic endball的主要原因。
相關研究成果已於2019年5月6日發布在英國科學期刊《自然-化學生物學》(Nature Chemical Biology)的網路版上。
人類的神經廻路連接成直線的話長達50萬公里,形成神經廻路的就是神經細胞的軸突。
神經廻路很容易因外傷等斷裂,比如脊髓傷害等。斷裂後神經細胞最遠的尖端會發生沃勒變性,但較近的尖端(細胞體側)仍然存活,因此神經軸突會嘗試重新向遠端延伸。但中樞神經系統的神經軸突會蠻力阻止這種再生(圖1)。
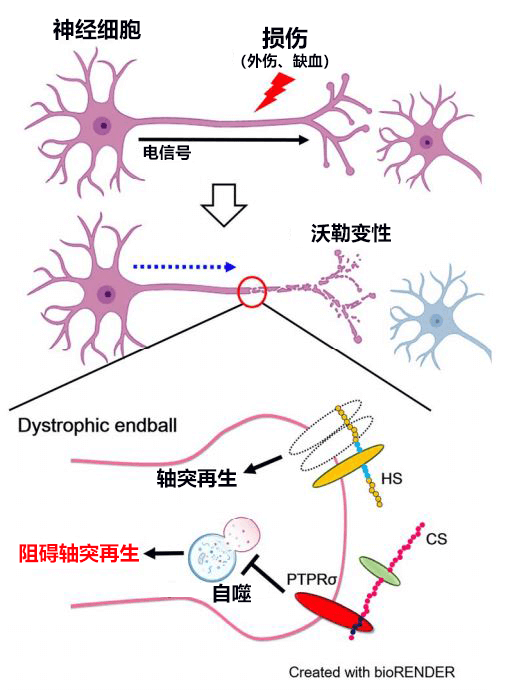
圖1:阻礙神經軸突再生
這樣神經廻路就會被永久切斷,導致患者出現麻痹等後遺症。罪魁禍首就是名為硫酸軟骨素(CS)的糖鏈。
因為CS會與神經細胞接受者PTPRδ結合,在神經尖端部分誘導名為Dystrophic endball的異常球狀結構。另一方面,名為硫酸乙酰肝素(HS)的糖鏈負責軸突生長,奇妙的是,CS與HS的結構非常相似,都會與同一個接受者PTPRδ結合。不過,長期以來一直不清楚這兩種十分相似的糖鏈是如何發揮完全相反的作用的。
研發小組首先化學合成了結構和長度各不相同的一系列HS和CS。對其進行解析發現,HS能夠與大量PTPRδ同時結合,因此該接受者為多聚體,而CS只能與一個或極少量的PTPRδ同時結合,因此接受者為單體。PTPRδ的這種狀態差異向神經細胞發送了完全相反的命令。
研發小組還發現,CS會提高PTPRδ的酶活性,使細胞内的Cortactin分子脫磷酸作用。而磷酸化的Cortactin是完成自噬必不可少的分子。因此,軸突内的自噬被中斷,由此抑制軸突生長,在軸突末端形成球狀物Dystrophic endball,這是受損軸突的特徵之一。
該發現的重要之處在於,查清了通過CS-PTPRδ-cortactin-autophagy這一路徑阻礙軸突生長的機制。由此明確了有效治療神經傷害的靶向分子。例如,HS低聚糖和PTPRδ抑制劑等有望成為候選藥物。另一個重點是,該發現還有望用來查明巴金森氏症和阿茲海默症等神經退行性疾病的發病機製。因為在這些疾病中也經常發現自噬中斷的現象。(日文發布全文)
文:JST客觀日本編輯部














