日本北海道大學研究生院藥學研究院的市川聰教授與美國杜克大學的Seok-Yong Lee副教授等人組成的聯合研究小組,全面解析了對耐藥菌也有效的天然有機化合物與靶酶的復合體結構。
用於治療細菌感染的抗生素迄今為止挽救了無數生命。不過,使用抗生素會出現對抗生素產生耐受力的耐藥菌,因此新藥開發的歷史可以說是藥物與耐藥菌之間的「道高一尺魔高一丈」。耐藥菌的傳播已經成為全球性的嚴重問題,當務之急是開發對耐藥菌也有效的抗生素,這是抵抗耐藥菌的「最後堡壘」。
在對抗耐藥菌的新型抗生素開發中,與細菌細胞壁的主要成分肽聚糖的生物合成有關的酶MraY受到了關注,目前已經從自然界中分離出了幾種能蠻力抑制MraY的天然有機化合物。
此次,市川教授等人組成的聯合研究小組對化學合成的天然產物衍生物群與MraY結合形成的復合體進行三維結構解析,由此提出了「條碼系統」,能為抑制MraY的化合物提供合乎邏輯和常理的設計指南。這樣就可以根據復合體結構進行藥物設計,有望開發出能對抗耐藥菌的抗生素,作為抑制耐藥菌的「最後堡壘」。
相關研究成果已發布在2019年7月2日(週二)公開的《自然-通訊》(Nature Communications)雜誌上。
【研究背景】
已知細菌細胞壁的主要成分肽聚糖是開發抗生素的優良靶標,此前已經開發出了青黴素等β-內醯胺類抗生素和萬古黴素等。但現在又出現了對這些抗生素產生耐受力的耐藥菌,成為了嚴重的世界性問題,在全球有數百萬人因為耐藥菌而死亡。為對抗耐藥菌,當務之急是開發具有新的作用機制的抗生素。近年來,合成肽聚糖前驅體——脂質I(Lipid I)的酶MraY(所有細菌生長必不可少的酶)作為開發抗生素的新靶標備受期待。
目前已經從自然界中分離出幾種能蠻力抑制MraY的天然有機化合物。這些化合物的尿苷部分擁有相同的結構,其他結構則有較大差異。
此前一直不清楚這些化合物是如何與MraY相輔作用的,以及今後該如何進行分子變換才能進一步「發揮藥效」。
【研究方法】
為分析此前化學合成的3種抑制MraY的天然有機化合物(或其衍生物)是如何抑制MraY的,研究小組對復合體結構進行了綜合解析。雖然難以對跨膜酶MraY進行X射線晶體結構解析,但此前市川教授等人組成的聯合研究小組全球首次對Muraymycin D2(MRY D2)與源自嗜熱菌Aquifex aeolicus的MraY形成的復合體成功地進行了X射線晶體結構解析(Nature 2016, 533, 557)。此次試著在相同的條件下獲得其他復合體的晶體,但很遺憾未能實現。
因此,聯合研究小組向大羊駝(Llama、Lama、Glama)施用MraYAA,通過對生成的多種MraY的單鏈抗體(奈米抗體)進行解析,獲得了約60種奈米抗體。利用其中3種適合結晶的奈米抗體,成功與3種抑制MraY的天然有機化合物進行了共結晶,並對獲得的晶體實施了X射線晶體結構解析(圖1左)。
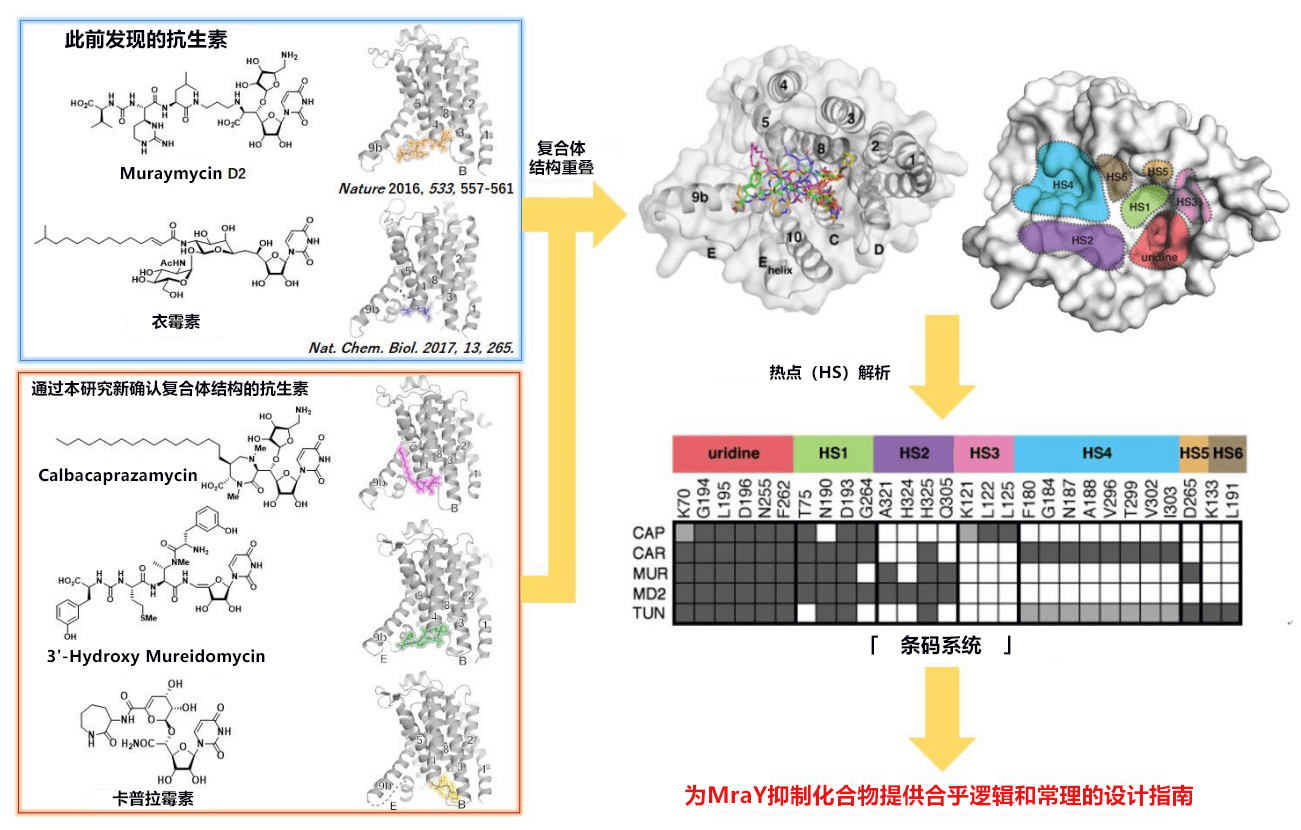
圖1.
(左)對成功實現共結晶的MraY抑制天然有機化合物晶體進行X射線晶體結構解析的結果。
(右)可以為MraY抑制化合物提供合乎邏輯和常理的設計指南的「條碼系統」。
【研究成果】
通過結構解析發現,所有化合物共同存在的尿苷部均與同一個結合口袋結合,但其他位點形成了不同的相輔作用。聯合研究小組將這些特徵位點分別定義為熱點(HS),把尿苷周圍、TM9b /Loop E、己內醯胺結合、疎水性、Mg2+結合及衣黴素結合口袋分別命名為HS1-HS6。另外,通過分析化合物與包含6個HS在内的殘基形成的相輔作用,提出了能為MraY抑制化合物提供合乎邏輯和常理的設計指南的「條碼系統」(圖1右)。
分析發現,除了與HS1結合外,各種抑制劑必須與至少2個HS相輔作用。例如,雖然卡普拉黴素(Capuramycin)屬於例外,與HS1及HS3進行結合,但衣黴素與HS4和HS5結合,並在其他化合物不具備的HS6中形成氫鍵,表明衣黴素擁有與其他化合物不同的HS結合譜。
聯合研究小組通過對抑制MraY的天然有機化合物全面實施結構解析,首次發現了以上現象。
【未來展望】
通過利用為MraY抑制化合物提供合乎邏輯和常理的設計指南的「條碼系統」,可以根據復合體結構實施藥物設計,有望開發出新的抗生素,作為對抗耐藥菌的「最後堡壘」。
(日文新聞發布全文)
文:JST客觀日本編輯部翻譯整理














