東京大學研究生院工學系研究科化學系統工學杉山弘和副教授的研究組,用於生物醫藥製劑無菌灌裝工藝選擇的線上工具「TECHoice」的原型版本(Prototype Version)現已公開[1]。作為一款線上軟體,計算和介面功能已經部署到伺服器。包括大小生物醫藥企業、醫藥生產合同外包組織(contract manufacturing organization,CMO;contract development and manufacturing organization,CDMO)等在内的眾多客戶都可以免費訪問使用(圖1)。TECHoice的網路位址[2]及示範業已公佈於7月15日的《Processes》雜誌上[文獻1]。
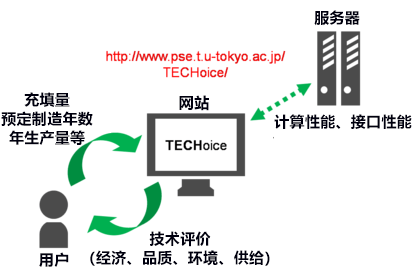
圖1 TECHoice使用流程示意圖
以單源抗體藥為代表的生物製藥市場在全球範圍内急速擴張,迫切需要對生產製造工藝進行最適化提高。一般來說,生物製藥的製造工程包括原料藥(Active Pharmaceutical Ingredients,API,又稱活性藥物成份,比如單抗藥品中的有效成分--單抗)的製造和最終藥品製劑(比如注射液等最終的藥品使用形態)的製造。本次TECHoice解決方案面向的無菌灌裝(圖2),即對原料藥的濾過性滅菌後灌裝到西林瓶、注射器和安瓿瓶等最終使用容器並加塞等,是藥品製劑製造的重要一環。
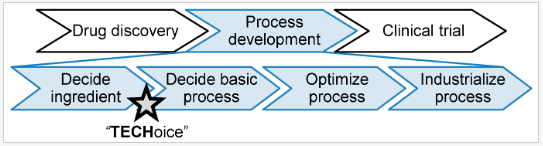
圖2 新藥研發過程中TECHoice可以應用的階段示意
生物製藥工業生產流水線中製劑最後灌裝模製是患者護理的第一道但也是最後一道防線,所以要求生產過程性能穩定,製造設備絕對清潔無菌,防止微生物和微粒污染,保證生物製劑的醫藥活性。生物藥製劑無菌灌裝過去主要走重複利用(Multi-Use Technology,MUT)的技術路線,採用不鏽鋼製發酵槽和管道設備,在不同批次間進行清洗和滅菌處理,以防交叉感染。後期引入的預先清潔和滅菌處理的一次性樹脂裝置(Single-Use Technology,SUT),
省時省力但提高了後期生產成本。儘管一次性路線和重複利用路線在成本等各方面存在差異(圖3),但目前為止尚未能確立一個在何種情形下選用哪個技術路線的綜合評估體系。
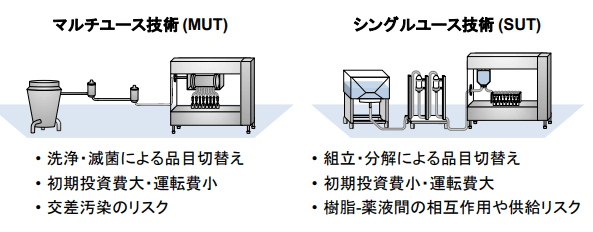
圖3 MUT與SUT兩種不同技術路線的比較
研究組此次開發的線上工具TECHoice,可以從經濟性、環境衝擊、產品品質和供應穩定性等方面綜合考慮,對生物製劑無菌灌裝工藝中是採取何種工藝路線做出直觀性的分析比對並給出最優選擇建議。目前所有客戶都可以自由訪問原型版本,便於數據輸入和結果輸出的介面也已基於Type Script、Java Script和Hypertext Markup Language等程式設計語言構建,並已部署到Web伺服器上(圖4),運算功能主要在負責存儲計算執行文件的MATLAB Production ServerTM上展開。
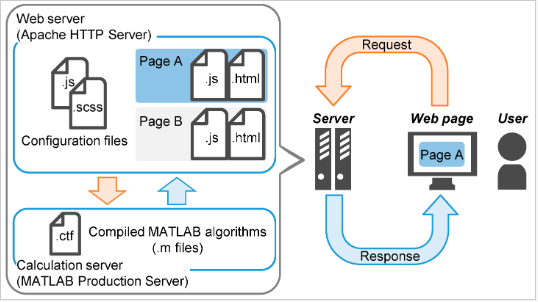
圖4 基於Hypertext Transfer Protocol (HTTP)協議的線上工具結構示意圖 (圖出自文獻1)
TECHoice對SUT、MUT以及二者融合混用而成的雜合路線(Hybrid Technology:HYB),從淨成本、生命週期内二氧化碳排放量、產品品質影響、供應穩定性四個方面進行綜合評估。通過輸入填充量、年產量、預計生產年數等初始參數,和藥劑化學性質、設備尺寸、設備價格等預設參數計算比較得出上述四個層面的定量評估值。另外還可以根據各項加權因數的敏感度不同給測評人員一個可選擇性的結論(圖5)。這些分析對新藥研發中的工藝設計,尤其在大量生產工廠開工建設前綜合取捨:權衡投資方向尤為關鍵。
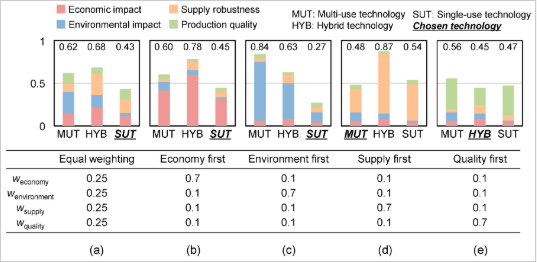
圖5 不同應用場景下不同路線各指標權重結果直觀性示例 (圖出自文獻1)
值得特別強調的是,TECHoice並非是科學家們在實驗室裏閉門造車的產物。其從構想階段伊始就一直是客戶導向,採用了質量源於設計(Quality by Design, QbD)的理念。其整個開發過程,是國際製藥工程學會(International Society of Pharmaceutical Engineering:ISPE)日本總部成立的特別研究小組在考察了行業具體需求和應用有效性的前提下負責推進的。杉山副教授領導的該研究小組包括了製藥企業、設備製造商、機械工程公司等成員,從TECHoice概念提出到功能設計、結構規畫、可操作性與有用性等各個方面都收到了來自下游行業客戶的大量建議和意見。研究組計劃後續會對原型版進行功能擴充和升級改造,進一步提高實用性。
供稿 宋傑 東京大學博士
圖除特別註釋外均取自日文新聞發布稿
編輯修改JST客觀日本編輯部
參考文獻
1. Haruku Shirahata, Sara Badr, Yuki Shinno, Shuta Hagimori, Hirokazu Sugiyama. Online decision-support tool 「TECHoice」 for the equipment technology choice in sterile filling processes of biopharmaceuticals. Processes 2019, 7(7), 448; https://doi.org/10.3390/pr7070448
相關鏈結
1. 東京大學官方新聞稿
2. TECHoice網路位址













