東京大學附屬醫院的前川洋醫生與東京大學研究生院醫學系研究科的特聘教授稻城玲子等人,查明瞭急性腎傷害(Acute Kidney Injury,AKI)的粒線體功能異常伴發炎發生的機制。
此前已知AKI伴隨腎小管粒線體傷害和發炎反應誘導兩種現象。本項成果表明二者都是由粒線體DNA激活先天免疫系統的引起的,該發現具有劃時代的意義。另外小鼠實驗顯示,通過遺傳學及藥理學上抑制該機制的靶分子——干擾素基因刺激蛋白(Stimulator of Interferon genes,STING),可以達到改善AKI的效果。
住院患者罹患AKI的比例很高,同時重症患者必須透析、死亡率攀升,此次的研究成果有望開發出新的AKI治療方法,進而改善AKI患者的預後。
<研究背景>
急性腎傷害(Acute Kidney Injury:AKI)是指由各種原因引起的腎功能快速惡化的疾病。發生AKI後無法正常產生尿液,本來應該通過尿液排出的各種物質不斷在體內累積,最終引起心力耗竭和電解質異常等尿毒症症狀。嚴重的話需要進行透析治療。另外,住院患者很多都會罹患AKI,進而導致死亡率上升。研究發現,即使腎功能一時得到改善,將來也極有可能發展成腎功不可逆降低的慢性腎病或者完全失落腎臟機能的腎耗竭晚期。
腎臟是由多類細胞形成三維複雜器官。已知罹患AKI後,腎臟近端小管細胞會發生粒線體傷害並誘發發炎反應。另外,近年來發現了識別細胞質内DNA並引起先天免疫反應的cyclic GMP-AMP synthase(cGAS)- stimulator of interferon genes(STING)通路。因此,研究人員研究了患AKI後近端小管細胞發生的粒線體傷害及相繼誘發的發炎反應與cGAS-STING通路之間的關係。
<研究内容>
本次研究使用小鼠常用抗癌藥---順鉑(Cisplatin,CDDP)來建立AKI模型。施用順鉑後,小鼠患上AKI的同時,腎臟内的cGAS-STING通路被激活,發炎細胞介素表達增加。另外, AKI患者的腎組織標本也顯示cGAS-STING通路被激活。
接下來,利用抑制了STING表達的STING基因剔除小鼠確認,和使用STING抑制劑得到同樣的效果,施用順鉑後造成的腎功能傷害和發炎反應得到了改善。當向近端小管細胞添加順鉑後,利用細胞膜外能量代謝分析儀和流式細胞分析技術測定,粒線體功能出現傷害,粒線體外膜電位下降。
進一步研究發現,在施加順鉑的近端腎小管細胞中,粒線體DNA洩漏到細胞質中,激活了cGAS-STING通路,並誘發了發炎。粒線體DNA推測是通過粒線體外膜上與程式性細胞死亡有關的BAX洩漏的(圖 1)。
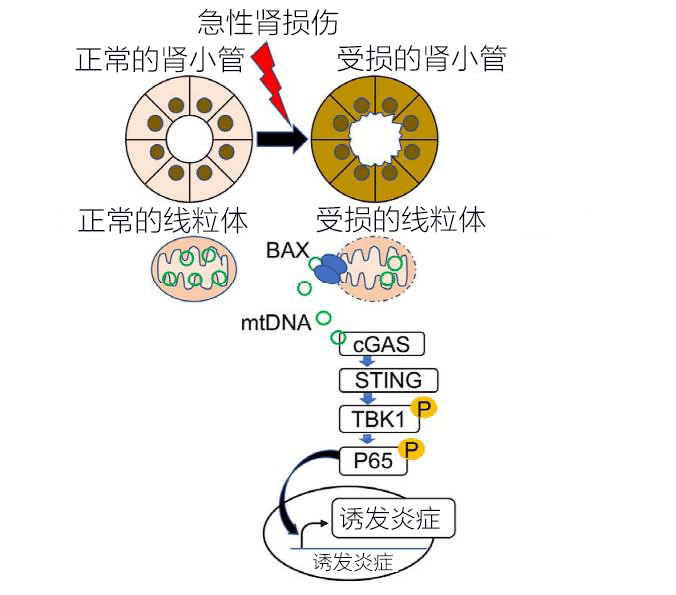
圖1:在急性腎傷害中,腎小管細胞會發生粒線體傷害,並經由BAX發生粒線體DNA(mtDNA)洩漏,從而通過cGAS-STING通路引起發炎反應。
論文題目:Mitochondrial damage causes inflammation via cGAS-STING signaling in acute kidney injury.
期刊名稱:《Cell Reports》(網路版:10月29日)
DOI編號:10.1016/j.celrep.2019.09.050
文:JST客觀日本編輯部翻譯整理














