原京都大學研究生鈴木大助(現為千葉大學醫學部本科生)、京都大學iPS細胞研究所(CiRA)講師杉本直志和堀田秋津,以及京都大學CiRA的教授江藤浩之(兼千葉大學再生治療學研究中心主任)等人合作,利用基因編輯技術,通過iPS細胞製作了HLA-I缺失的巨核細胞系(imMKCL),成功製造出HLA缺失血小板。HLA缺失的iPS血小板是可以向任何亞型HLA-I進行輸血法的廣譜製劑(圖1)。
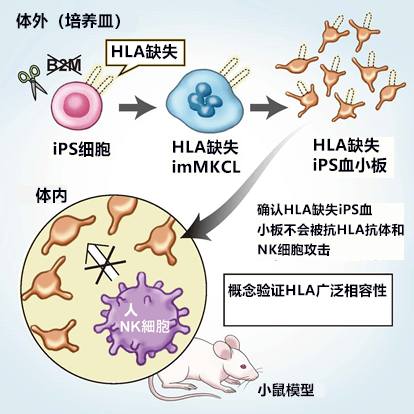
圖1:研究概要圖
利用基因體編輯技術,通過iPS細胞製作了HLA-I缺失的巨核細胞系,成功製造了血小板。經驗證,這種血小板在培養皿内沒有被NK細胞攻擊,而且在新培育的小鼠模型中也順利實現循環。HLA-I缺失的iPS血小板有望成為可以為無數人輸血法的「通用」製劑。
血小板輸注患者有5%左右會出現與免疫反應有關的血小板輸注無效症。這種情況下,血小板的類型如果不配對分組就會產生排斥,因此導致可用捐血供體受限,血小板供應不足的風險升高。血小板輸注無效症的主要原因是在懷孕或血小板輸注時,產生了針對與自體不同的HLA-I分子的抗體。目前使用人類iPS細胞的血小板製作技術作為對供體依賴捐血的補充系統正在積極推進臨床研究。不過,因HLA-I不配對分組會引起血小板輸注無效症,所以需要使用與接受者HLA-I相配對分組的製劑。所以存在一個挑戰是,至少需要準備140種HLA-I亞型才能覆蓋約90%的日本人。
江藤教授和杉本講師等人組成的研究團隊2010年宣佈可以通過人類iPS細胞生產血小板。為了開發滿足臨床輸注所需的血小板大規模製備技術,研究團隊從產生血小板的巨核細胞著手進行了推進。2014年通過人iPS細胞誘導成功了可自我克隆的巨核細胞,並確立體外冷凍保存的永生化巨核細胞系(imMKCL)的製作方法(中村等2014)。2018年,發現「亂流」對利用巨核細胞產生血小板非常關鍵,並開發了可產生亂流的生物反應器,成功實現了優質血小板的高效規模化製備(伊東、中村等2018)。
通過人工基因操作使由imMKCL製作的血小板不表達HLA-I的話,可以製備出對血小板輸注無效症也有效的血小板製劑,且直接實現滿足臨床輸血法製劑規模的系統製備。另一方面,不僅是血小板,此前也沒有充分驗證通過輸血法或移植的方式導入HLA-I缺失的細胞是否會被NK細胞排斥攻擊。已知NK細胞會攻擊包括病毒感染細胞和腫瘤細胞等在内的HLA-I低表達細胞。擁有人類NK細胞並且HLA缺失細胞受到排斥的動物模型也一直沒建出來。
因此,研究團隊除了在培養皿内驗證了NK細胞的反應性外,還與熊本大學聯合建立了擁有包括NK細胞在内的人類血細胞系統的小鼠模型。實際確認,HLA-I缺失血小板可在體內順利循環,不會被免疫系統滅絕。
本次研究成功在臨床應用推進中的iPS血小板系統裏整合進HLA-I敲除技術,並利用含NK細胞的體外實驗和動物模型驗證了免疫反應,確認HLA缺失的iPS血小板不會受到抗HLA抗體和NK細胞攻擊。這項概念驗證(POC:proof-of-concept)成果,證實HLA缺失的iPS血小板可作為「通用」的HLA相容製劑使用。HLA缺失iPS血小板的臨床應用有望消除因HLA-I不配對分組而引起血小板輸注無效症的輸注風險,並降低之前需多亞型製備iPS血小板帶來的規模成本(圖2)。
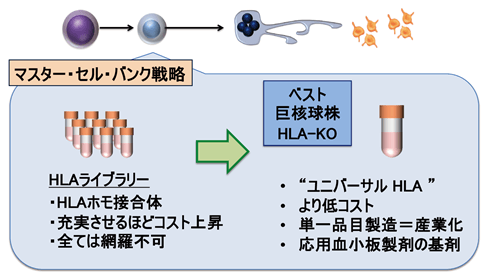
圖2:HLA缺失iPS血小板製劑的展望
在以往巨核細胞系的主細胞庫戰略中,要想配對分組HLA-I亞型,需要準備很多細胞庫。但如果是HLA缺失的iPS血小板,則可以利用最佳的細胞系,作為「通用」的單一製劑製造,有助於實現產業化。另外,均質製劑還利於血小板的醫療應用。
相關研究成果已於2019年12月26日發布在美國科學期刊《Stem Cell Reports》的網路版上。
論文資訊
題目:iPSC-derived platelets depleted of HLA class-I are inert to anti-HLA class-I and NK cell immunity
期刊:《Stem Cell Reports》
DOI: 10.1016/j.stemcr.2019.11.011.
文:JST客觀日本編輯部翻譯編輯














