3月18日,日本東京大學醫科學研究所亞洲傳染病研究基地的井上純一郎教授與山本瑞生助教宣佈,發現絲胺酸蛋白酶抑制劑「萘莫司他」(Nafamostat)能夠抑制新型冠狀病毒(SARS-CoV-2)感染人體細胞的膜融合。這一發現是利用能對病毒進入細胞的最初過程——病毒外膜與細胞膜的融合進行定量評估的膜融合測量系統發現的,絲胺酸蛋白酶抑制劑「萘莫司他」與此前發布的其他融合抑制劑相比,能以1/10以下的低濃度抑制病毒的膜融合。

東京大學於3月18日舉行記者會,宣佈「萘莫司他」有可能阻止新冠病毒感染人體(照片:共同社)
萘莫司他是日本治療胰腺炎的處方藥物,目前還沒有進行鍼對新型冠狀病毒感染症的臨床試驗。井上純一郎教授在記者發布會上表示希望能夠盡快通過臨床實驗驗證,獲得在人體內部也有效的數據。
東京大學教授井上純一希望能夠盡快獲得人體有效的結果(照片:NHK報導截屏)
SARS-CoV-2要想感染人體,需要與細胞表面存在的接受者蛋白(ACE2接受者)結合,然後使病毒外膜與細胞膜融合,這一過程至關重要。就冠狀病毒而言,Spike蛋白(S蛋白)與人體細胞膜的ACE2接受者結合後,會被蛋白質水解酶TMPRSS2切斷,激活S蛋白,活化的S蛋白對病毒外膜與細胞膜的融合是十分關鍵的環節。井上等人根據MERS冠狀病毒的研究結果調查了萘莫司他和卡莫司他(Camostat)的作用,發現萘莫司他以1-10nM的低濃度就可以顯著抑制病毒侵入。這表明,萘莫司他可能會非常有效地阻止SARS-CoV-2感染。
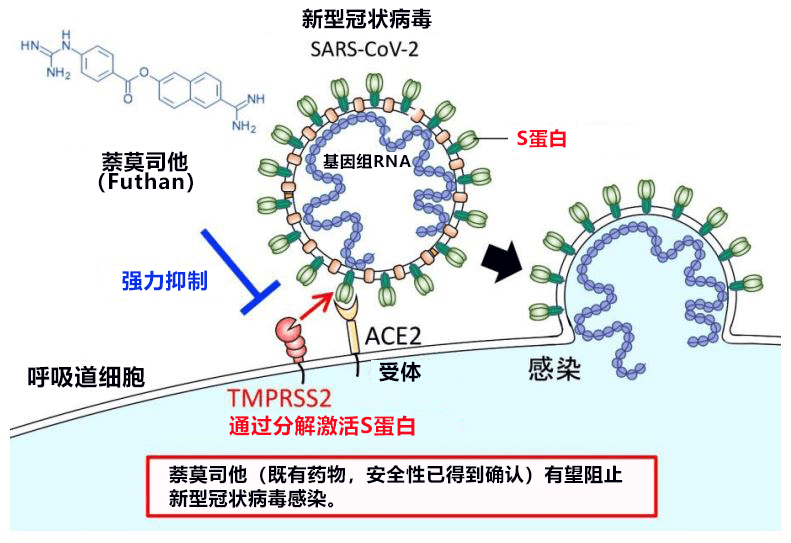
在SARS-CoV-2等冠狀病毒中,病毒基因體RNA被由脂雙層和外膜蛋白組成的病毒套膜(外膜)包圍著。SARS-CoV-2在病毒套膜上的Spike蛋白(S蛋白)與細胞膜接受者(ACE2接受者)結合後,開始侵入人體細胞。來自人體的細胞蛋白酶(蛋白質水解酶)——弗林蛋白酶(Furin)將S蛋白切割為S1和S2。然後,S1與接受者ACE2結合。而另一個片段S2被人體細胞表面的絲胺酸蛋白酶TMPRSS2切斷,由此出現病毒與細胞的膜融合。
Hoffmann等人發現,呼吸道細胞中有ACE2和TMPRSS2是感染SARS-CoV-2的必備條件(參考文獻1)。井上等人在2016年就發現,絲胺酸蛋白酶抑制劑萘莫司他利用依賴MERS-CoVS蛋白、接受者CD26和TMPRSS2的膜融合系統能有效抑制膜融合,可作為MERS-CoV感染抑制劑使用(參考文獻2)。
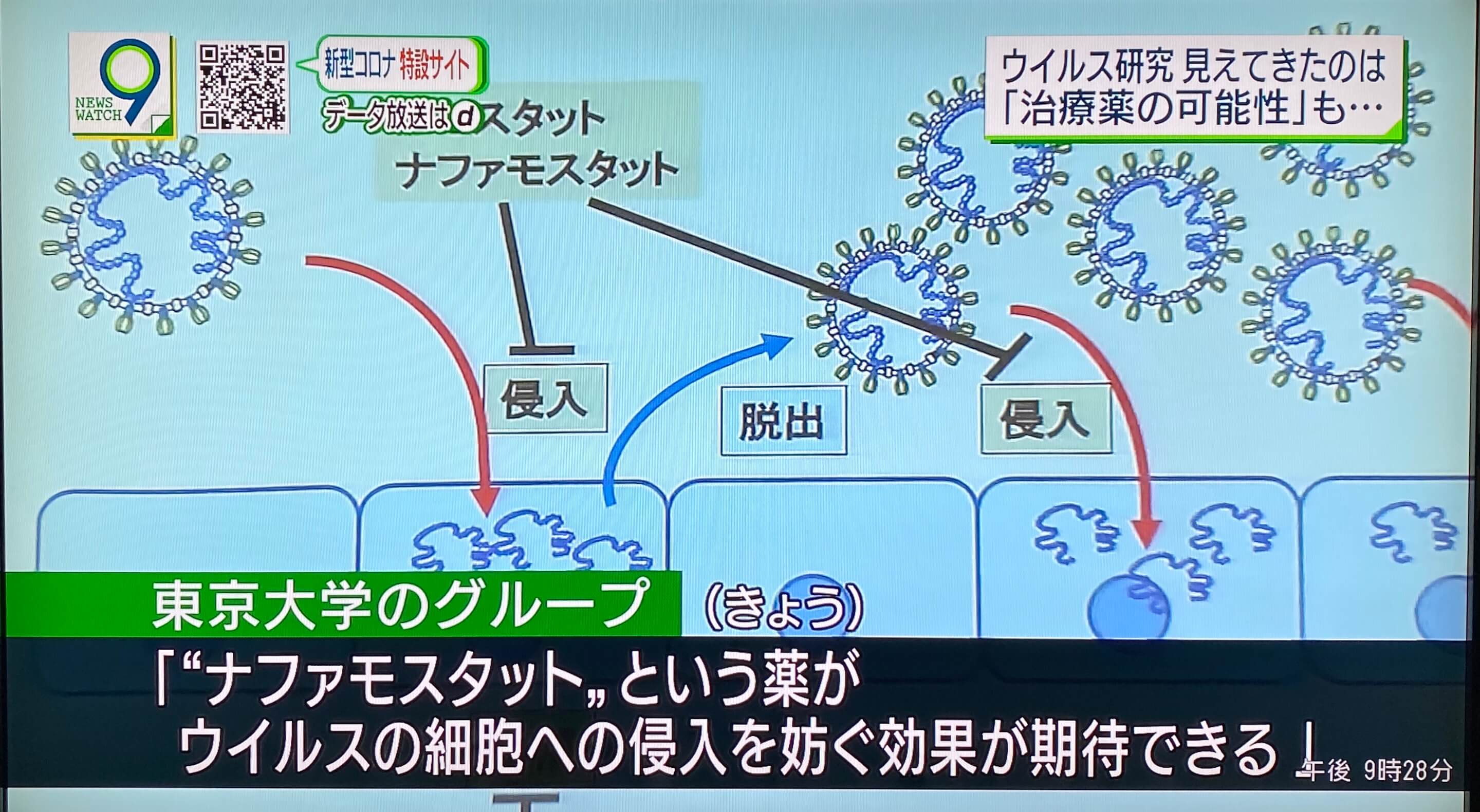
萘莫司他阻止新冠病毒侵入人體細胞的機制圖(照片:NHK報導截屏)
此次井上等人利用293FT細胞(源自人類胎兒腎臟)以及依賴SARS-CoV-2S蛋白、接受者ACE2和TMPRSS2的膜融合測量系統,研究了萘莫司他能否也抑制SARS-CoV-2S蛋白的膜融合。結果顯示,萘莫司他在10至1000nM的濃度範圍可以濃度依賴性地抑制膜融合。
接下來井上等人還利用内源性表達ACE2和TMPRSS2、呼吸道上皮細胞源Calu-3細胞(被認為是引起人類感染的重要感染細胞)實施了同樣的實驗,確認能以更低濃度的1-10nM濃度顯著抑制膜融合。這個濃度範圍與抑制MERS-CoVS蛋白膜融合的濃度範圍基本相同。另外,井上等人還比較了與萘莫司他相似的蛋白質水解抑制劑卡莫司他的效果,發現在SARS CoV-2S蛋白的融合中,萘莫司他能夠以卡莫司他約1/10的濃度顯示出抑制效果。
以上結果表明,在臨床使用的蛋白質水解抑制劑中,萘莫司他效果最好,有望阻止感染新型冠狀病毒感染症。萘莫司他和卡莫司他都是日本治療胰腺炎的藥物,在日本國内已經作為處方藥使用多年。萘莫司他在臨床上通過靜脈注射的方式給藥,據推測,給藥後的血中濃度將超過此次實驗得到的抑制SARS-CoV-2S蛋白膜融合的濃度,所以有望在臨床上抑制病毒進入人體細胞。卡莫司他為口服藥,服用後的血中濃度被認為會低於萘莫司他,但與其他新型冠狀病毒藥物合併使用也可能會獲得效果。
論文資訊
1.Hoffmann et al. Cell 181,1-10(2020)
2.Yamamoto et al. Antimicrob Agents Chemother 60,6532-6539(2016)
文:JST客觀日本編輯部














