日本理化學研究所(簡稱「理研」)生命機能科學研究中心計算分子設計研究團隊的小松輝久研究員、小山洋平研究員、衝本憲明高級研究員、森本元太郎技師、大野洋介高級技師和泰地真弘人組長組成的研究團隊,利用分子動力學(MD)模擬專用計算機「MDGRAPE-4A」,對新型冠狀病毒感染症(COVID-19)的致病病毒「SARS-CoV-2」的主蛋白酶結構動態進行了10微秒(1微秒為100萬分之1秒)的模擬。並於3月17日在存儲庫Mendeley Data中公開了原始數據,以供全球的新藥研究人員自由使用。
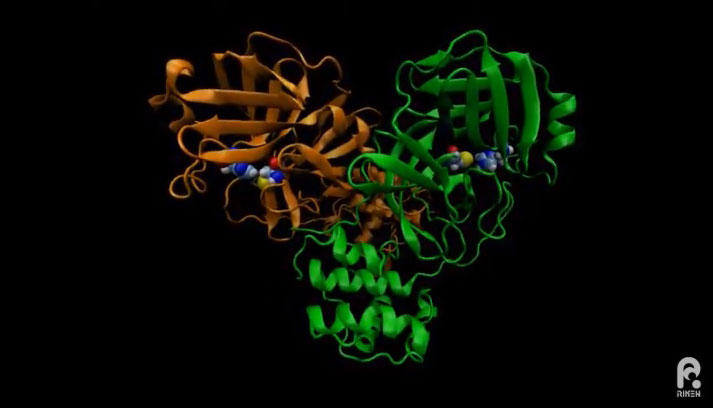
圖:MDGRAPE-4A超算模擬的SARS-CoV-2主蛋白酶結構。用顏色區分了構成二聚體的兩個次單元,用球形模型表示了位於蛋白酶活性中心的氨基酸位點。(理研公開影片截圖)
該數據有望用來開發有效抑制病毒繁殖所必需的蛋白酶活性的抑制劑,以及篩選候選分子等。
冠狀病毒的基因體為單鏈RNA,感染寄主細胞後,會通過RNA基因體翻譯出長蛋白(多聚蛋白)。隨著這種多聚蛋白被裂解,各片段會作為病毒繁殖所需的結構蛋白和酶發揮作用。在這些酶中,主要催化多聚蛋白裂解的是主蛋白酶。抑制主蛋白酶裂解活性的抗病毒藥物正在開發之中,已有多家研究機構報告了針對人類免疫不全症病毒(HIV)等現有病毒的蛋白酶抑制劑和SARS-CoV-2主蛋白酶復合體的空間結構(X射線晶體解析數據)。MD模擬是在近似於細胞内的環境下解析分子間相輔作用的手法,可用來獲取高精度推進新藥篩選(考慮水溶液中的分子動態和溶劑效果)的資訊。
研究團隊以最近報告的SARS-CoV-2主蛋白酶X射線晶體解析數據為基礎,利用MDGRAPE-4A模擬了蛋白酶二聚體在水溶液中的結構動態。
影片:利用MDGRAPE-4A模擬的SARS-CoV-2的主蛋白酶結構動態(理研公開影片)
研究背景
新型冠狀病毒感染症(COVID-19)自2019年在中國武漢首次報告病例以來,至今已擴散到世界各地,世界衛生組織(WHO)宣佈疫情進入全球大流行。這種新型病毒產生的社會影響已波及到全球,開發針對COVID-19的有效藥物成為非常緊急的國際事件。
冠狀病毒的基因體為單鏈RNA,感染寄主細胞後,會通過RNA基因體翻譯出長蛋白(多聚蛋白)。隨著這種多聚蛋白被裂解,各片段會作為病毒繁殖所需的結構蛋白和酶發揮作用。確定COVID-19的致病病毒為「SARS-CoV-2」後,很多研究機構都解析了病毒蛋白的空間結構,並不斷將成果錄入公共數據庫。
根據結構解析開發抗病毒藥物時,靶蛋白之一是主要催化多聚蛋白裂解的主蛋白酶。抑制主蛋白酶的裂解活性被認為是可以抑制病毒在感染細胞内的繁殖,所以科學家都在尋找與主蛋白酶結合的抑制性分子。實際上,現在已針對人類免疫不全症病毒(HIV)開發出了多種靶向主蛋白酶藥物,並顯示出了有效性。
在近年來的藥品開發中,利用超級計算機探索和評估針對靶蛋白的候選藥物分子的計算機模擬(In Silico)新藥開發備受關注。分子動力學(MD)模擬是在近似於細胞内的環境下解析分子間相輔作用的方法,可獲得用來高精度推進新藥篩選(考慮水溶液中的分子動態和溶劑效果)的資訊。
研究團隊開發了新藥開發專用超級計算機「MDGRAPE-4A」,從2019年11月開始實驗性運行。與普通計算機相比,MDGRAPE-4A擅長在短時間内模擬蛋白質的結構變化,因此對靶蛋白、候選藥物分子和水分子的動態結構進行採樣後,有望利用其結構數據進行高精度的結合親和性預測,並以現實的計算時間實現高精度的計算機模擬篩選。
研究方法與成果
研究團隊利用MDGRAPE-4A超算,以可以自由利用的形式公開了SARS-CoV-2主蛋白酶的MD模擬資料。用於模擬的SARS-CoV-2主蛋白酶的空間結構主要以Liu等人的報告為基礎,溶劑的水分子數量將近3萬個,系統的總原子數量將近10萬個。利用MDGRAPE-4A實施了約10天的計算,模擬了SARS-CoV-2主蛋白酶的10微秒(1微秒為100萬分之1秒)結構動態(圖1)。
一般認為,水溶液中的蛋白質與藥物的分子間相輔作用發生在亞毫秒(~100微秒)的時間尺度内,此次的數據應該可以作為推算藥物分子結合前的主蛋白酶結構動態的基礎數據。
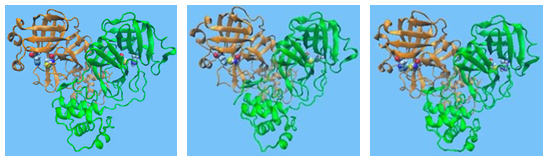
圖1:利用MDGRAPE-4A模擬的SARS-CoV-2的主蛋白酶結構動態。從圖中可以看出,主蛋白酶結構會隨著時間而產生變化。
未來展望
目前,作為候選的抗病毒藥物,已提出了幾種能夠與SARS-CoV-2主蛋白酶結合的分子,而且對其復合體實施了X射線晶體解析。雖然距離真正開發出新藥還有很長的路要走,還需要開展大量的研究,但利用此次公開的MD模擬資料可預測候選分子與主蛋白酶的結合強度等,有望加快國内外的新藥研究速度。
今後,研究團隊預定繼續模擬SARS-CoV-2的主蛋白酶,並廣泛研究結合狀態下的候選藥物分子的模擬、類似蛋白酶,以及在SARS-CoV-2中編碼的其他潛在新藥靶蛋白的模擬等。
文:JST客觀日本編輯部編譯














