日本橫濱市立大學研究生院醫學研究科梁明秀教授帶領的聯合研究團隊,成功開發出了可獨特性檢測新型冠狀病毒(SARS-CoV-2)抗原的單源抗體。此次製作的抗體不會與近緣的SARS冠狀病毒或引起感冒的人類冠狀病毒發生交叉反應,隻對新型冠狀病毒(SARS-CoV-2)起反應(圖1)。今後,利用該抗體可以簡便地開發出在短時間内準確檢測出新型冠狀病毒免疫層析試劑盒。
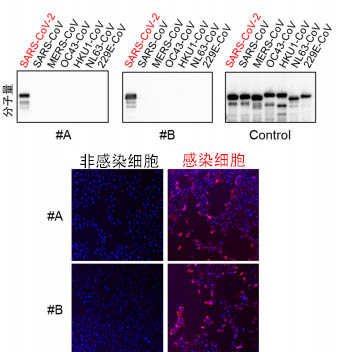
圖1:抗體的性能評估
(上)採用蛋白質記憶痕跡法的抗體獨特性解析。此次開發的抗體#A和#B隻檢測新型冠狀病毒,不與其他人類冠狀病毒發生交叉反應。
(下)感染新型冠狀病毒的Vero-E6/TMPRSS2細胞的螢光免疫染色圖像。抗體#A和#B均檢測出了感染細胞内的病毒抗原。藍色:細胞核,紅色:病毒抗原
研究背景
據報告,新型冠狀病毒感染症(COVID-19)的感染人數全球超過了200萬人,已造成16萬多人死亡,作為一個非常嚴重的全球性公眾衛生問題,亟需盡快採取對策。另外,日本的感染人數也超過了1萬例,今後疫情也可能繼續擴大。
目前,病原體檢測僅採用PCR法等病毒基因檢測法,但平均要4~6小時左右才能出結果,而且需要使用特殊設備,檢測數量有限。作為可在醫療現場使用的快速診斷法,研究人員雖然開發出了血清抗體檢測試劑盒,但目前尚無獲批作為體外診斷用藥品使用的試劑(或者產品),另外,該方法是確認對病原體的免疫反應(抗體)的試驗法,因此不適合感染初期的檢測。
要想掌握新型冠狀病毒的實態,並提供適當的防控對策和妥善的治療,必須盡快開發一種能在感染初期即可迅速進行診斷的簡易診斷法。另一方面,要想開發檢測試劑盒,必須開發能準確識別新型冠狀病毒抗原的單源抗體。現在使用的很多抗體與SARS冠狀病毒和其他相關人類冠狀病毒等的交叉反應尚未得到充分驗證,準確檢測新型冠狀病毒的高性能單源抗體目前還沒有實用化。
研究内容
以梁明秀教授為中心組成的聯合研究團隊首先利用病原體蛋白合成法大量製備了構成新型冠狀病毒的核衣殼蛋白(NP),該方法應用了梁教授擁有的技術小麥胚芽無細胞法(圖2)。接下來,通過以NP為免疫原為小鼠接種,成功確立了144株產生抗NP單源抗體的融合瘤。從中篩選哪些融合瘤會產生僅獨特性識別新型冠狀病毒抗原的抗體時發現,其中20株產生了僅檢測新型冠狀病毒的單源抗體。
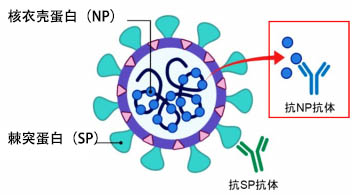
圖2:新型冠狀病毒的結構和此次開發的抗體的靶標
另外研究團隊還查清了這些抗體識別的位點,並確認在各國分離的新型冠狀病毒毒株間也存在這些位點。這表明,此次獲得的抗體具有可全面檢測新型冠狀病毒的優異特性。此外還發現,該識別位點與近緣冠狀病毒的相似性比較低,實際上,該抗體完全不會與其他人類冠狀病毒發生反應,隻對新型冠狀病毒有反應。聯合研究團隊利用生物膜干涉技術解析了抗原抗體的相輔作用,發現這些抗體對抗原蛋白NP有很高的親和性。另外還發現,這些抗體中有6株是可用於免疫染色和ELISA法等的高品質抗體。
未來展望
採用免疫學方法的檢測試劑盒開發取決於該試劑盒使用的抗體能否準確識別病原體。雖然目前還沒有開發這種試劑盒,但今後有望利用這種高性能抗體,開發可以簡單快速地僅檢測新型冠狀病毒的免疫層析試劑盒。如果能開發出檢測病毒抗原蛋白的簡易免疫層析試劑盒,那麼無需使用特殊設備,在門診或病牀邊就可以通過簡單的操作快速檢測出病毒。今後能確立快速診斷法,並提高診斷精度,在與PCR檢測比較靈敏度後,有望作為實施PCR檢測前的篩檢手段。
文:JST客觀日本編輯部














