本文根據大阪大學研究成果發布資料翻譯整理而成
新型冠狀病毒病感染症(COVID-19)肆虐全球,至今仍未找到有效的治療方法,需要盡快開發治療藥物和疫苗。
京都府立醫科大學循環器内科學的星野溫助教、大阪大學蛋白質研究所的高木淳一教授及微生物病研究所的岡本徹教授等人組成的研究團隊,成功地將新冠病毒的接受者——ACE2蛋白的病毒結合力提高了100倍以上。新冠病毒通過與人體細胞ACE2蛋白結合來完成感染,而利用提高了結合力的高親和性修飾型ACE2蛋白,有望抑制病毒感染人體細胞。
今後將與Life Science Institute公司共同開發採用該高親和性修飾型ACE2蛋白的病毒中和蛋白製劑。
背景
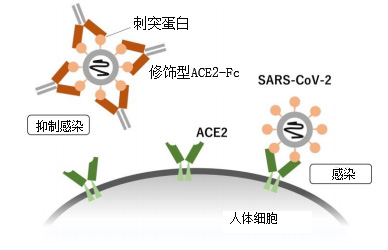
新型冠狀病毒(SARS-CoV-2,簡稱「新冠病毒」)引起的新型冠狀病毒感染症(COVID-19)已在全球造成5000多萬人感染,130多萬人死亡。新冠病毒通過使病毒顆粒表面的刺突蛋白與人體細胞表面的ACE2蛋白結合來完成感染。因此,治療時可採用阻斷並中和刺突蛋白的方法,作為中和製劑,業界目前正在大力開發抗體製劑。不過,使用抗體製劑的話可能會發生逃逸突變,即因病毒發生基因突變,刺突蛋白的形狀改變,導致抗體無法與其結合。為解決這個問題,研究團隊著眼於新冠病毒接受者——ACE2蛋白,開發通過提高ACE2蛋白與病毒的結合力來實現高中和活性的蛋白製劑。
研究方法與成果
研究團隊採用了定向進化法,即在試管内演化ACE2蛋白,使其更容易與病毒結合。首先,在容易出錯的條件下擴增ACE2基因,製作擁有約10萬種ACE2突變體的基因池。然後在細胞表面分別表達這些突變體,從中回收能與病毒的刺突蛋白充分結合的類型。之後繼續向回收的ACE2突變體中導入突變,以同樣的流程回收能進一步與刺突蛋白結合的突變體。通過重複這個步驟,最終成功地將ACE2與病毒刺突蛋白的結合力提高到了100倍以上(圖1)。作為結合力指標的解離常數(KD值)方面,野生型為41.4nM ,而修飾型ACE2為0.37nM,實現了比抗體製劑更高的結合力。
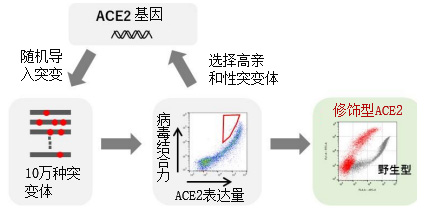
圖1:利用定向進化法開發高親和性ACE2的概要
接下來,研究團隊合成了使抗體的Fc區域與該高親和性修飾型ACE2結合的蛋白製劑,並評估了功能。通過結合Fc,有望穩定在體內的藥代動力學特性,以及變成二聚體提高中和活性。在針對偽病毒的中和實驗中,野生型的感染半抑制濃度(IC50)為12.6μg/mL,而修飾型為0.055μg/mL,有效性約達到200倍。另外,在針對新冠病毒的中和實驗中,修飾型ACE2-Fc在普通抗體製劑的血液濃度範圍内表現出良好的病毒中和活性(圖2)。
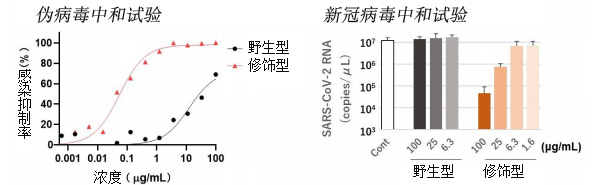
圖2:修飾型ACE2-Fc製劑的病毒中和試驗
在偽病毒中和試驗中,研究團隊使不同濃度的ACE2-Fc和病毒分別與293T/ACE2細胞反應1個小時,48小時後利用螢光酵素檢驗法評估了感染率(左側)。而在新冠病毒中和試驗中,使不同濃度的ACE2-Fc和病毒分別與Vero6/TMPRSS2細胞反應2個小時,24小時後利用即時PCR法評估了分泌到培養基中的病毒拷貝數(右側)。
未來展望
今後將利用此次研究開發的高親和性修飾型ACE2蛋白,與Life Science Institute公司共同開發具備高病毒中和活性、且不會因病毒基因發生突變而產生抗藥性的新型治療藥物。另外,如果該製劑能安全地用於人體並實現普及,則有望終結這場肆虐全球的COVID-19疫情。
論文資訊
題目:High affinity modified ACE2 receptors prevent SARS-CoV-2 infection
期刊:bioRxiv
URL:10.1101/2020.09.16.299891
日語發布原文
編譯:JST客觀日本編輯部














