本文根據慶應義塾大學成果發布編譯整理而成
慶應義塾大學醫學部整形外科學教室的鐮田泰裕(博士課程4年級學生)和生理學教室的神山淳副教授等人組成的研究團隊,通過與大日本住友製藥公司再生和細胞醫藥神戶中心的磯田美帆博士等人進行聯合研究,開發出了將臨床用人iPS細胞有效分化為膠質細胞(寡樹突膠細胞(注1)等)的誘導方法,通過臨床用於脊髓傷害模型動物的脊髓後確認,運動功能得到了改善。
作為通過神經幹細胞移植恢復受損脊髓功能的機制之一,移植細胞的再髓鞘化至關重要。髓鞘通過覆蓋從神經細胞延伸出來的軸突,像絕緣片一樣發揮作用,可使脊髓内實現非常快速的神經傳遞。此前也有利用人iPS細胞源移植細胞進行再髓鞘化的報告,但移植細胞均使用研究用iPS細胞,未報告過採用臨床用人iPS細胞的分化誘導法以及使用模型動物的驗證成果。
此次,研究團隊利用擁有不易發生排斥反應的HLA型組合的人iPS細胞培養了容易分化成膠質細胞的神經幹細胞並進行移植,確認運動功能得到明顯的改善,因此該成果有望實現從基礎到臨床的無縫銜接,有力推動臨床應用。
此次開發利用了京都大學iPS細胞研究所(CiRA)培養的臨床用iPS細胞誘導膠質細胞指向性神經幹細胞(Neural Stem/Progenitor Cells(NS/PCs) with gliogenic competence from clinically relevant feeder-free human iPSCs:以下簡稱「ffiPSC-gNS/PCs」),通過向脊髓傷害模型小鼠移植ffiPSC-gNS/PCs,驗證了其安全性和有效性(下圖)。
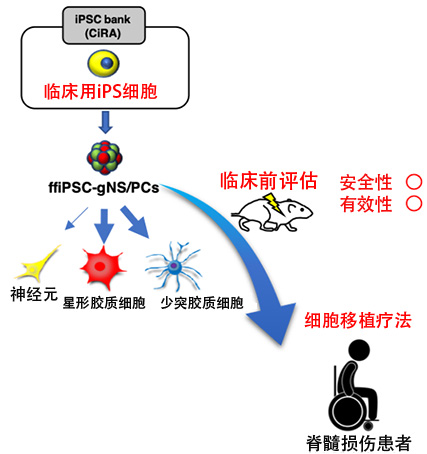
圖:研究概略圖
研究成果
(1)通過免疫染色和基因表現分析確認培養的細胞具有較高的膠質細胞分化指向性
通過免疫染色確認,利用此次開發的新誘導法培養的神經幹細胞高度表達未分化細胞分化為膠質細胞時所須的轉錄因子NFIA和OLIG2。另外,基因表現分析也同樣確認膠質細胞相關的基因表現升高。
(2)經確認,移植的細胞大多都分化為寡樹突膠細胞,並實現再髓鞘化
移植的ffiPSC-gNS/PCs在移植12周後的小鼠傷害脊髓内分化成了神經元、星狀神經膠細胞和成熟的寡樹突膠細胞。另外,通過電子顯微鏡確認,多數細胞都針對由來自移植細胞的寡樹突膠細胞構成的殘存軸突實現了再髓鞘化。
(3)實施細胞移植的小鼠因脊髓傷害而降低的運動功能得到改善
針對脊髓傷害後移植了ffiPSC-gNS/PCs的小鼠和僅注入磷酸鹽緩衝溶液的小鼠,評估了後肢運動功能,確認細胞移植小鼠的運動功能明顯得到改善。另外,在轉棒上的行走時間和在平地上行走時的步幅也得到改善。此外還發現,移植了ffiPSC-gNS/PCs的小鼠,後肢的髖關節、膝關節和踝關節可以更順暢地運動。
(注1)寡樹突膠細胞
中樞神經内的膠質細胞之一,會形成包圍細神經的脂質層——髓鞘,具有加快神經信號傳遞速度的功能。
論文資訊
題目:A robust culture system to generate neural progenitors with gliogenic competence from clinically relevant induced pluripotent stem cells for treatment of spinal cord injury
期刊:STEM CELLS Translational Medicine線上版
DOI:10.1002/sctm.20-0269
日語發布資料
編譯:JST客觀日本編輯部














