日本產業技術綜合研究所的中村真紀主任研究員與信州大學的齋藤直人教授等人,開發出了治療骨轉移癌的奈米顆粒。顆粒中含有抑制破骨細胞功能的藥物,可以將藥物遞送到細胞中,有助於實現副作用較小的治療。
在健康的骨骼中,形成骨骼的細胞和破壞並吸收骨骼的細胞會均衡地發揮作用。癌細胞轉移到骨骼後,會激活破骨細胞,破骨溶解出來的蛋白質則會促進癌細胞增殖,形成惡性循環。
骨轉移在無法通過手術徹底切除癌細胞時等,一般使用抑制破骨細胞功能的藥物「雙膦酸鹽」進行治療。雙膦酸鹽會附著在骨骼的磷酸鈣成分上被吸收,從而抑制破骨細胞工作。由於是通過靜脈注射的方式給藥,副作用比較強。需要開發一種向破骨細胞遞送藥物的方法。
研究團隊此次開發出了直徑約為100奈米(奈米為10億分之1米),尺寸容易被細胞吸收的奈米顆粒。奈米顆粒是碳片的集合體,看起來像海膽。藥物被放在相當於海膽刺的部分。

新開發的奈米顆粒可遞送抑制破骨細胞功能的藥物=圖片由產業技術綜合研究所提供
抑制破骨細胞功能的藥物與骨骼的主要成分磷酸鈣親和性比較高,容易附著上去。磷酸鈣與碳片也容易粘附在一起。這些物質在水溶液中混合後,聚集在一起形成了一個顆粒。
新開發的顆粒設想在發生癌細胞轉移的骨骼附近局部給藥。被破骨細胞吸收的顆粒首先收歛集在細胞中的消化器官——溶體中。 由於溶體内部呈弱酸性,顆粒中含有的磷酸鈣會溶解出來並釋放藥物。
在實驗中,研究團隊向來自小鼠的破骨細胞中加入新開發的奈米顆粒後發現,顆粒被細胞吸收。還以相同的濃度分別加入新開發的顆粒和單獨的藥物進行了比較。單純加入藥物時,細胞幾乎都能存活,而加入新開發的顆粒時,存活率約為50%。單純加入藥物時除非濃度達到此次給藥量的100倍左右,否則無法攻擊破骨細胞。
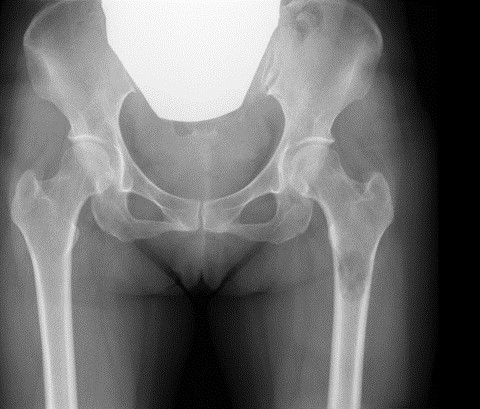
轉移到左側大腿骨的癌細胞(陰影部分)。會引起疼痛並導致骨骼變脆=圖片由信州大學醫學部附屬醫院提供
研究團隊預定利用小鼠等驗證新開發的顆粒的效果。目標是繼續進行改良,以使其易於被破骨細胞吸收,還將開發少量給藥即可取得效果的治療方法,力爭盡快開始臨床試驗。
據報告,死於癌症的人約有30%發生了癌細胞骨轉移。乳房癌、前列腺癌和肺癌等發生骨轉移的情況尤其多。發生骨轉移後,骨骼會變脆,從而導致骨折和疼痛。患者的生活品質(QOL)會明顯降低。
日文:下野谷涼子、《日經產業新聞》、2021年1月25日
中文:JST客觀日本編輯部













