大阪大學研究生院理學研究科博士後期課程的學生野村幸汰(日本學術振興會特別研究員DC)與真木勇太助教、岡本亮講師、梶原康宏教授及岡山大學健康系統綜合科學研究科的佐藤Aya副教授等人組成的研究團隊,通過以硫代酸為關鍵物質,開發出了完全不同於以往的醣蛋白合成方法,由此實現了在免疫過程中至關重要的細胞介素——糖鏈結模具組裝C-C基序趨化因子配體1(CCL1)及白血球介素3(IL3)的化學合成。另外,研究團隊還通過細胞實驗分析了造血細胞上的IL3接受者與通過該合成法合成的IL3結合形成復合體時糖鏈所發揮的功能。由於可以將糖鏈自由嵌入蛋白質中,探究糖鏈在醣蛋白中功能的研究有望取得進展。此外,醣蛋白和醣肽製劑等聚合物~中分子藥品的合成效率也有望提高。相關研究成果已發布在《Journal of the American Chemical Society》上。
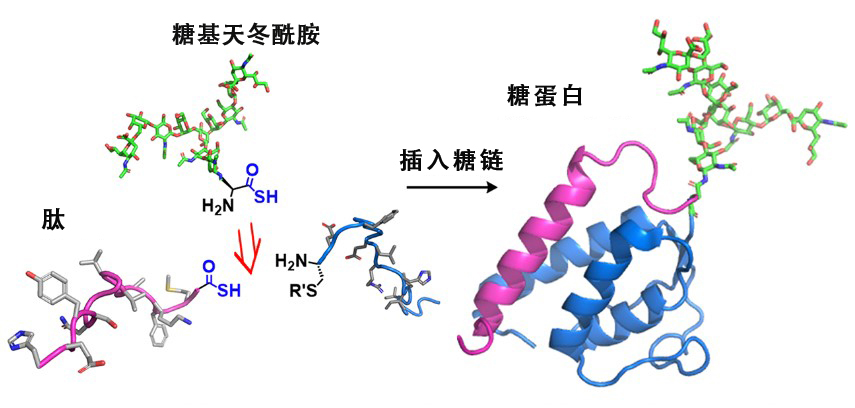
新的醣蛋白合成方法。通過以化學方法將糖基天冬醯胺酸嵌入到蛋白質中實現了醣蛋白的快速合成(圖片:大阪大學提供)
醣蛋白具有對病毒產生免疫反應和發炎反應,以及向細胞傳遞信號等多種功能,但與體內的蛋白質結合的糖鏈有多種結構,很難確定哪種結構的糖鏈比較重要。另外,利用生物技術獲得高純度的醣蛋白也非常困難。
解決這個問題的對策之一是可以自由改變糖鏈結構,且能獲得高純度醣蛋白的化學合成法。但是以往的醣蛋白合成法平均需要100多個合成步驟,很難簡單合成。
針對這些問題,上述研究團隊為發展合成結構均一的醣蛋白的高效方法,很早就開始利用從雞蛋中分離出來的糖鏈,研究擁有各種糖鏈結構的醣蛋白的化學合成。其中,在後期將糖鏈插入蛋白質分子的方法作為難度最大,效率最高的合成方法,一直在該團隊考慮之中。然而,由於蛋白質和糖鏈存在各種各樣的官能基,像低分子藥物那樣精確控制分子結構進行連接的方法在以前比較困難。因此需要開發精確控制蛋白質(肽)分子的化學選擇性反應。
研究團隊通過以硫代酸為關鍵物質,開發出了可通過化學選擇性連接糖基天冬醯胺酸硫代酸和蛋白質(肽)鏈的新型酰胺耦聯反應「二醯基二硫化物耦聯(DDC)」。
然後利用基於DDC的合成法,開發出了可將糖鏈自由插入蛋白質的任意位置的醣蛋白合成法。
由此可以將合成的糖鏈迅速嵌入醣蛋白,從原料開始大約隻需5步就能成功合成出高純度醣蛋白。
研究團隊還測量了IL3(擁有用此次開發的方法合成的糖鏈)的細胞增殖活性,評估了糖鏈的功能,由此發現了促進IL3與其接受者蛋白結合的新作用機制。
為了研究此類糖鏈作用影響的實驗,必須快速獲得具有均一糖鏈的高純度醣蛋白,這種合成法被認為將成為今後探究醣蛋白上的糖鏈功能的關鍵。
另外,利用這種合成法可以快速製備醣蛋白,還有望應用於醣蛋白製劑。
梶原教授表示:「醣蛋白的化學合成大約20年前就開始了。當時完全無法實用化,只是在實驗室中勉強能合成。此次的合成研究是2015年前後開始與野村、畢業生原口以及岡本講師和真木助教等人一起推進的,從意外發現的肽合成法中發展而來。雖然還需要進行改良,但隻需幾個步驟就能合成醣蛋白是一項超出預期的成果,今後還可以用於新藥研發。」
原文:《科學新聞》
翻譯編輯:JST客觀日本編輯部













