東京醫科齒科大學研究生院醫齒學綜合研究科的橫田隆德教授和永田哲也副教授通過與愛奧尼斯製藥公司和武田藥品工業公司開展聯合研究,開發出了突破常規核酸藥物無法有效通過的血腦障壁,可通過靜脈注射和皮下注射抑制中樞神經系統的基因表現的血腦障壁(BBB)通過型異源雙鏈核酸。雖然脊髓性肌萎縮症的核酸藥物已經獲批,難治性神經系統疾病的根治正逐漸變為可能,但由於必須終生持續向鞘内注射藥物,患者的負擔非常大,而此次開發的技術,患者可以自己進行皮下注射。橫田教授表示:「(該藥物)應用於已批准的幾種異源核酸藥物後確認,具有5倍至100倍(平均20倍左右)的超強基因抑制效果。另外,還考慮將該藥物應用於阿茲海默症等,目前正與多家製藥公司進行聯合研究」。相關成果已經發布在《Nature Biotechnology》上。
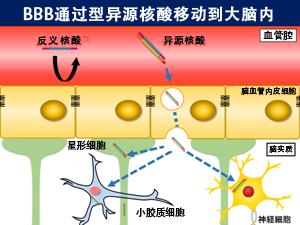
血腦障壁通過型異源核酸會穿過腦血管內皮,移動到大腦内,被神經細胞、小膠質細胞和星狀神經膠細胞吸收,發揮抑制基因表達的效果。而單鏈反義核酸不會穿過腦血管內皮。(圖片由東京醫科齒科大學提供)
核酸藥物是一種先進生物醫藥技術,可以選擇性控制以往的低分子化合物和抗體藥物難以控制的靶標RNA。近3年來,脊髓性肌萎縮症、家族性澱粉樣多發性神經病變及杜氏肌營養不良症等神經和肌肉疾病領域已經有15種核酸藥物通過審批。另外,肌萎縮側索硬化症、帕金森症和阿茲海默症等多種中樞神經系統疾病也在進行臨床試驗。
但是,治療中樞神經系統疾病時,需要進行腰部椎骨穿刺直接向鞘内注射藥物。因為以往的反義核酸和siRNA等核酸藥物全身給藥時無法通過血腦障壁,藥物無法到達大腦和脊髓等中樞神經。
鞘内給藥是從後背的腰部椎骨縫隙將一根長針插入脊髓周圍的脊液中給藥的方法,老年人中常見的接受抗凝治療的患者,以及難治性神經系統疾病中常見的脊柱側彎患者則很難通過這種方法給藥,偶爾也會發生感染和出血等。
東京醫科齒科大學的聯合研究團隊雖然已經獨立開發出了擁有與常規核酸藥物不同的分子結構和多樣化的遞送分子,以及憑藉獨特的細胞内作用機制而高度有效的DNA/RNA異源雙鏈核酸,但大腦的控制則比較難。因此,研究團隊嘗試使各種脂質傳遞分子(配體)與互補鏈結合,篩選了血腦障壁通過性藥物。由此發現,結合膽固醇注射到小鼠的靜脈中時,顯著抑制了中樞神經系統中的靶標RNA。這種效果通過多次給藥得以加強。
另一方面,以往的單鏈反義核酸無論單次給藥還是多次給藥都未能發現抑制中樞神經系統基因表現的效果。此外,研究團隊還利用在單鏈反義核酸中直接結合膽固醇的核酸進行了比較,確認這種方法效果較弱,且具有高毒性。
研究團隊利用新開發的血腦障壁通過型異源雙鏈核酸進行靜脈注射後確認,藥物被遞送到中樞神經系統中,並抑制了各種靶標RNA在中樞神經系統中的基因表現。詳細調查在神經細胞和各種膠質細胞中的基因表現的抑制效果後發現,在神經細胞和小膠質細胞中發現了強烈的基因表現抑制效果。共聚焦雷射顯微鏡的即時圖像顯示,只有血腦障壁通過型異源雙鏈核酸明顯移動到了大腦中。
除靜脈注射外,皮下注射也觀察到了中樞神經系統的基因表現抑制效果,這樣患者就無需每次都去醫療機構,可以自己進行皮下注射,存在大幅提高患者便利性的可能。
原文:《科學新聞》
翻譯編輯:JST客觀日本編輯部













