千葉大學研究生院理學研究院的板倉英祐副教授等人組成的研究團隊開發出了利用螢光蛋白使缺陷粒線體實現視覺化的缺陷粒線體感測器(Mito-Pain)。Mito-Pain解析與篩選可能傷害粒線體的化合物相結合後,除了此前已知的巴金森氏症致病基因的行為外,還發現了粒線體會根據壓力類型表現出不同行為的現象。相關成果已發布在《Journal of Biological Chemistry》上。
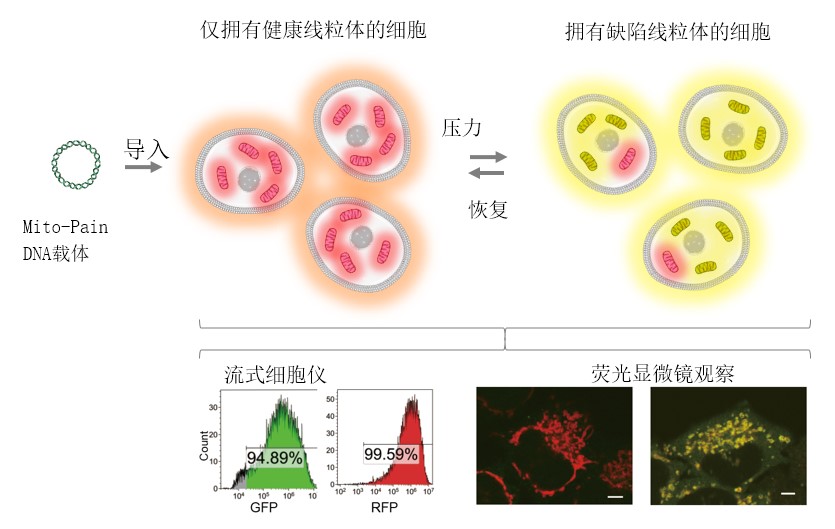
粒線體的壓力水平量化和局部動態分析成為可能(供圖:千葉大學)
粒線體容易因活性氧等壓力而受損,受損成為缺陷粒線體後,缺陷粒線體的積累會對細胞產生不良影響,從而誘發巴金森氏症或癌症等多種疾病。因此,調查何種情況下會出現缺陷粒線體至關重要,但此前由於方法有限,只能檢測特定的壓力。
PINK1基因是巴金森氏症的致病基因之一,以往的研究表明,PINK1蛋白在健康細胞中會迅速分解,但在有缺陷粒線體外膜上則保持穩定。利用這一特性,可將PINK1作為缺陷粒線體的標誌物使用,研究團隊製備了由PINK1、GFP(綠色螢光蛋白)、T2A(自切割序列)、RFP(紅色螢光蛋白)和Omp25(粒線體外膜蛋白)構成的Mito-Pain(DNA載體)。
當Mito-Pain被導入細胞後,一個mRNA會產生等量的PINK1-GFP和RFP-Omp25蛋白。RFP-Omp25局部存在於所有粒線體的膜上,而PINK1-GFP隻穩定存在於缺陷粒線體的膜上。也就是說,健康的粒線體上只有RFP,而缺陷粒線體上既有RFP也有GFP,因此可將黃色(紅色與綠色的混合色)比例的增加情況作為缺陷粒線體增加的指標進行定量分析。另外,通過利用螢光顯微鏡觀察細胞内的缺陷粒線體,還可以分析局部的粒線體壓力。
研究發現,粒線體受到壓力變成缺陷粒線體後,PINK1與巴金森氏症的致病基因產物Parkin蛋白會共同發揮作用,通過自噬分解並去除(粒線體自噬)缺陷粒線體。研究團隊通過Mito-Pain調查了引起粒線體壓力的各種化合物,發現有些化合物僅利用PINK1就會對粒線體壓力產生反應,這表明不僅是粒線體自噬,PINK1還具有獨立修復粒線體的功能。
板倉副教授表示:「粒線體壓力被認為會引起巴金森氏症、癌症及老化等。通過利用Mito-Pain詳細分析粒線體壓力,有望闡明各種疾病的發病機製。」
原文:《科學新聞》
翻譯編輯:JST客觀日本編輯部













