核心要點:
1. 免疫檢查點蛋白PD-L1是免疫治療的重要靶點,癌症組織中PD-L1的表達量與免疫治療的效果顯示臨床相關。
2. 本研究開發了一種新型的D型多肽核藥,該藥物可以獨特性檢測腫瘤組織中的PD-L1的表達量,從而為免疫治療提供指導。
3. 該核藥通過釋放β射線,可以選擇性殺死腫瘤組織中的PD-L1高表達的癌細胞,是一種潛在的癌症治療藥物。
4. 該研究表明D型多肽是理想的靶向核素遞送分子,為多肽核藥開發提供了新的研究方向。
國立研究開發法人量子科學技術研究開發機構量子生命・醫學部門量子醫科學研究所先進核醫學基礎研究部胡寬研究員,張明榮部長等人開發了一種新型的多肽核藥用於癌細胞中PD-L1的顯像,並證明了該核藥具有一定的腫瘤治療效果。該成果於近日發表在重要的藥學期刊《Acta Pharmaceutica Sinica B》。該研究的合作者包括來自中國南京市第一醫院、北京大學深圳研究生院以及深圳灣實驗室的研究人員。
研究背景
近年來,免疫治療成為了繼化學治療、放射性治療、靶向治療後,最重要的癌症治療手段之一。過去五年,基於免疫檢查點抑制劑的免疫治療取得了巨大的成功。目前,多種針對免疫檢查點蛋白PD-1/PD-L1/CTLA-4的單源抗體藥物已經進入市場,為患者提供了更多的治療選擇。但是,免疫檢查點治療也表現出一些不足。比如:只有部分病人對免疫檢查點治療顯示臨床受益。因此,如何篩選出潛在的受益人群,從而避免無效治療,是仍舊存在的醫學難題。
基於臨床數據分析,研究人員發現腫瘤組織中PD-L1的表達量與免疫檢查點治療效果呈現密切的相關:高表達PD-L1蛋白的病人在接受免疫檢查點抑制劑治療後,表現出更佳的臨床受益。因此,非侵入性檢測腫瘤組織中的PD-L1表達量,可以篩選出適合免疫檢查點治療的病人,從而提高治療的有效性和準確性。
截至目前,來自美國、中國等國家的科學家相繼開發了可以獨特性顯像PD-L1的核醫學診斷試劑。日前,多個診斷藥物已經在美、中分別進入臨床試驗階段。與美、中相比,日本尚未有免疫檢查點顯像藥物進入臨床。儘管本庶佑教授因為對免疫治療領域的巨大貢獻獲得了諾貝爾獎,但是,日本在免疫檢查點顯像藥物的開發方面投入明顯不夠。
日本國立量研機構張明榮教授團隊於2018年開始啟動了免疫檢查點顯像藥物的開發項目,在過去三年,相繼發表了多篇重要論文,公開了該團隊在免疫檢查點顯像藥物開發方面的系列進展。該團隊從藥物分子創製出發,旨在開發出可以用於臨床的免疫檢查點顯像藥物。
研究内容
在該研究中,研究者將目光投向了一類新型的多肽分子—D型多肽。D型多肽是一類全部由D型胺基酸組成的多肽。D型多肽的研究始於上個世紀70年代,經過接近半個世紀的發展,人們對於D型多肽的結構、活性、活體代謝情況有了深刻的認識。D型多肽不僅保留了L型多肽的優點,如:優良的藥代動力學性質、優異的靶點獨特性以及低毒性。而且,與L型多肽不同,D型多肽難以被天然的水解酶識別降解,從而在活體內具有極強的穩定性。研究表明D型多肽較L型多肽具有更長的胃腸道、血漿以及細胞内的半壽命。此外,一些包含有D型氨基酸的多肽已被批准用於臨床,如Vasopressin,Desmopressin,DOTATATE等,這些結果表明D型多肽具有良好的生物安全性。鑑於以上優點,研究人員推斷D型多肽是潛在的核素顯像藥物的靶向載體。
研究者選擇了一條由十二個胺基酸組成的D多肽—DPA作為研究對象。DPA由噬菌體展示篩選得到,其具有獨特性結合PD-L1的能力。作者首先研究了DPA在活體小鼠内的分佈、吸收和代謝情況。研究者使用正電子核素64Cu對DPA進行了標記,接下來在正常C57BL/6J老鼠體內追蹤了[64Cu]DPA的運動情況。結果表明,[64Cu]DPA被快速的從血漿中清除,並主要經由腎臟排出體內(圖1)。通過尿液分析表明,[64Cu]DPA在體內未發生降解,直接以完整的分子形態從尿液排出。
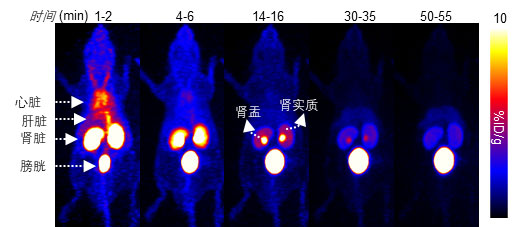
圖1. [64Cu]DPA在小鼠體內隨著時間的分佈變化動態圖。
隨後,研究人員分別在荷有B16F10和U87MG腫瘤的小鼠中進行了[64Cu]DPA成像,結果顯示,在尾靜脈注射後的80分鐘以内,[64Cu]DPA在瘤内有明顯的富集,這些結果表明[64Cu]DPA在活體內可以有效的結合PD-L1,從而進行PD-L1表達量的檢測。但是,考慮到64Cu的物理可用能半衰期為12.7h,與DPA的靶點作用時間不配對分組,隨後研究人員使用68Ga對DPA進行了標記。68Ga是一種短壽命的正電子發射核素,其半衰期為68min。在荷U87MG腫瘤的小鼠體內的顯像結果表明[68Ga]DPA是一種具有臨床轉化潛力的PD-L1的顯像分子(圖2)。
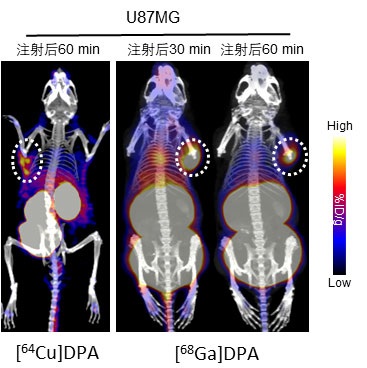
圖2. [64Cu]DPA和[68Ga]DPA在U87MG異種移植小鼠中的分佈圖。
最後研究人員進一步研究了[64Cu]DPA作為一種靶向PD-L1的核素治療分子對U87MG腫瘤生長的抑制情況。由於64Cu可以發射β負電子以及鄂惹電子,單次尾靜脈注射74MBq的[64Cu]DPA,即顯示出對U87MG腫瘤的生長抑制效果(圖3)。此外,[64Cu]DPA也表現出良好的生物安全性,在治療期間,除了由於放射性引起的白血球先減少後增多現象,未觀察到其他明顯的毒副作用。這些結果表明[64Cu]DPA是一種潛在的靶向核素治療藥物分子。
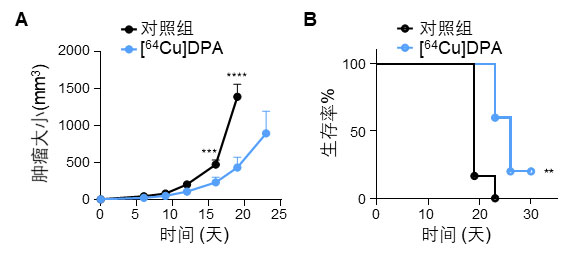
圖3. 腫瘤變化曲線(A)和小鼠存活曲線(B)。
研究結論
該論文開發了一種新型的PD-L1的診斷核藥物,該藥物由獨特性識別PD-L1的D型多肽和正電子核素組成。在黑色素瘤和腦膠質瘤模型中,該藥物成功對PD-L1的表達進行了檢測。此外,當與64Cu結合時,該藥物還顯示出一定的治療效果。未來,通過對該藥物的進一步最適化,有可能得到一種可臨床轉化的集診斷和治療功能一體的新型核藥。
論文資訊:
論文題目: Whole-body PET tracking of a D-dodecapeptide and its radiotheranostic potential for PD-L1 overexpressing tumors
刊載期刊 Acta Pharmaceutica Sinica B
論文鏈結:doi.org/10.1016/j.apsb.2021.09.016
文 胡寬
編輯修改 JST客觀日本













