東京醫科齒科大學綜合研究機構腦綜合功能研究中心的味岡逸樹副教授和東京農工大學研究生院工學研究科的村岡貴博教授等人組成的研究團隊宣佈,與北里大學、臺灣國立陽明交通大學和名古屋市立大學等共同開發了可形成在體內給藥部位緩慢釋放蛋白質的超分子肽凝膠的肽「JigSAP」。研究團隊把利用這種凝膠緩慢釋放具有血管再生的VEGF蛋白的超分子肽凝膠用於腦梗塞發病1周後的模型小鼠,確認行走功能得到改善。該成果有望實現針對亞急性期腦梗塞的無細胞再生治療。相關内容已發布在國際科學期刊《Nature Communications》的11月19日號上。
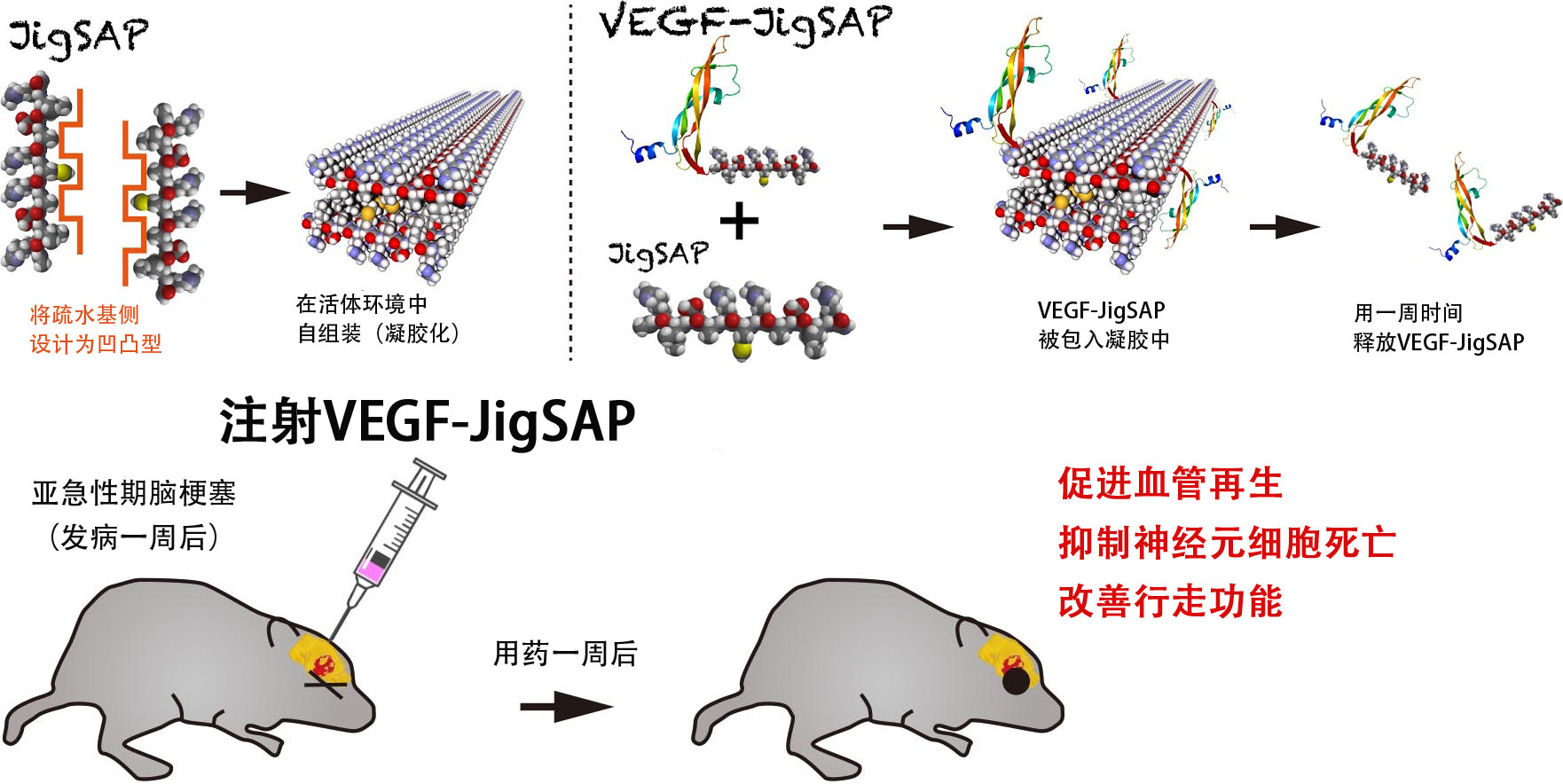
JigSAP肽凝膠吸收和緩慢釋放蛋白質,注射VEGF-JigSAP後改善了亞急性期腦梗塞小鼠的行走功能(圖片:東京醫科齒科大學)
在日本,每年有20萬人發生腦梗塞,其中約5%的患者在發病4.5~8小時内的早期階段接受溶栓和取栓治療後復健。其餘約95%的患者會留下護理需求為1~5級的後遺症,為減少就醫費用以及國家的醫療和護理費用,需要儘量讓腦梗塞患者復健。但另一方面,對於發病一週後的亞急性期重症患者,目前尚不存在有效的治療方法。
利用大腦的潛在再生能力的自體幹細胞移植和通過肽凝膠緩慢釋放細胞生長因子的技術備受期待,但幹細胞移植方法比較複雜,目前還沒有能納入細胞生長因子並在體內緩慢釋放的肽凝膠。
此次,研究團隊開發出了可用於臨床、安全性高、能在給藥後的大腦内緩慢釋放所含的細胞生長因子的新型超分子肽凝膠「JigSAP」。
在開發過程中發現,兩親分子肽會通過自組裝變成凝膠,氨基酸側鏈的疎水基側呈平面狀,這種疎水性相輔作用具有很強的凝聚力,使帶有兩親分子標記的蛋白質更容易被吸收,但很難在體內有效地緩慢釋放。
因此,研究團隊將兩親分子肽的疎水基側設計成像拼圖一樣的凹凸形狀,合成了由11個氨基酸構成的在活體環境中會變成凝膠的肽「JigSAP」。JigSAP在中性條件下變成凝膠,並隨著時間的推移變硬,經確認,作為細胞支架使用時,與天然的細胞支架纖連蛋白等具有相同的性能。
研究團隊還驗證了蛋白質的緩釋效果。使c端帶有JigSAP標記的EGFP(綠色螢光蛋白)-JigSAP與過量的JigSAP混合後確認,EGFP-JigSAP會吸收JigSAP並進行自組裝。通過在與活體相同的環境中試驗,確認EGFP-JigSAP在一週内以約40%的高效率緩慢釋放。
研究團隊根據過去的報告將血管內皮細胞生長因子(VEGF)設定為緩釋對象。製備了帶JigSAP標記的VEGF(VEDF-JigSAP)並與JigSAP混合,然後注射到腦梗塞模型小鼠的梗塞部位驗證了效果。
具體來說,研究團隊使小鼠發生腦梗塞並在第七天分析其步態,然後在不同條件下注射凝膠,7天后進行步態分析和組織學分析。給藥條件分別設定了注射磷酸鹽環域分析生理食鹽水(PBS:對照組)、僅注射JigSAP、僅注射VEDF-JigSAP、注射VEGF和VEDF-JigSAP、混合注射VEDF-JigSAP和JigSAP五種條件,然後進行了比較。
結果顯示,只有混合注射VEDF-JigSAP和JigSAP的小鼠改善了行走功能。通過組織學分析確認,只有這個條件促進了受損部位周邊的血管新生並抑制了神經元細胞死亡。這些效果被認為對改善腦梗塞模型小鼠的行走功能做出了貢獻。
研究團隊已開始著手推進醫療應用和商業化。今年4月在神奈川縣立產業技術綜合研究所啟動了「採用超分子肽的腦梗塞再生項目」,目前正在推進之中。
味岡副教授表示:「此次開發了使大腦發揮潛在再生能力的技術,這項成果還有望發展成明確大腦潛在再生能力的研究。實際上,我們也獲得了很多有趣的數據,希望能為神經再生學的發展做出貢獻。」
原文:《科學新聞》
翻譯編輯:JST客觀日本編輯部













