大阪大學研究生院醫學系研究科的谷内田真一教授宣佈,與東北大學、東京大學醫科學研究所和慶應大學等共同明確了罕見的難治性癌症——廣泛發生於消化系統的消化系統神經內分泌腫瘤(NEC)的發病機理。研究團隊通過收集日美歐的大量樣本,並全面進行基因體分析,發現發病機理引起的基因異常存在差異。NEC高度表達控制向神經內分泌系統分化的轉錄因子SOX2和ASCL1,研究發現,這與正常情況相反,是由啟動子區域的甲基化引起的。該成果有助於實現早期診斷和開發治療藥物。相關内容已經於12月9日發布在美國癌症學會的期刊上。
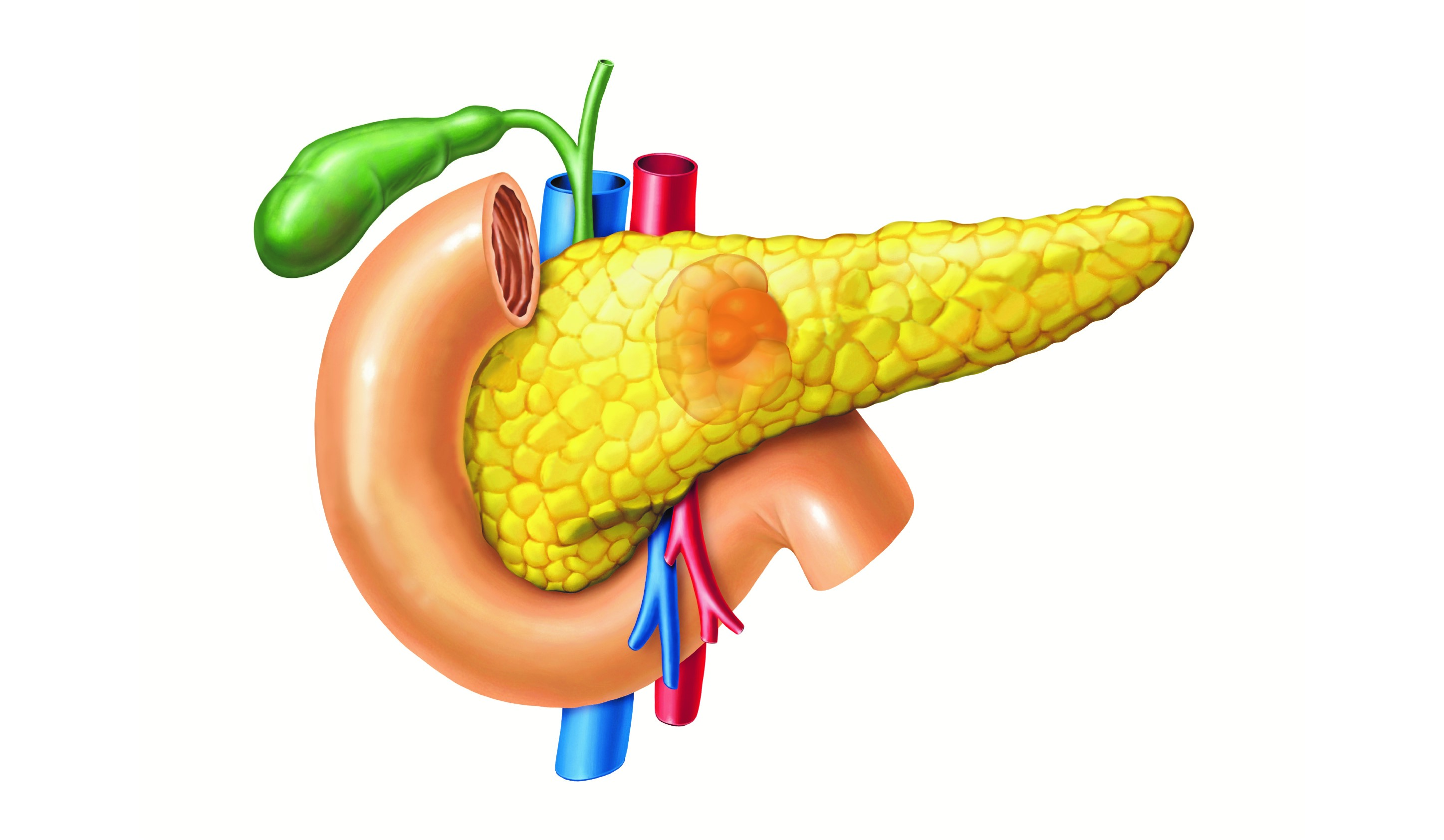
消化系統神經內分泌腫瘤發病機理(供圖:大阪大學)
眾所周知,NEC是比胰腺癌惡性程度更高、預後也更差的癌症。WHO根據病理組織圖像將消化系統的神經內分泌腫瘤(NENs)分為高分化神經內分泌腫瘤(NET)和低分化神經內分泌腫瘤(NEC)。NET很多都能通過手術根治,病理相對比較清楚。另一方面,NEC根據病理組織圖像分為小細胞型和大細胞型,但由於比較罕見且診斷時往往已經轉移,很難診斷和獲得研究樣本,因此一直沒有實施基因體分析。
研究團隊此次從各種消化系統癌症發病頻率較高的日本、美國和荷蘭收集了55例NET和60例NEC,全面實施了基因體分析(全基因體分析、全外顯子分析、全轉錄成分析、甲基化分析、ATAC-seq分析)。
首先按器官將NEC分為預後最差的胰腺來源和非胰腺來源進行了分析,發現基因體異常存在差異。確認胰腺源NEC可以分為發生KRAS基因突變,胰腺的導管細胞標記基因(SPP1和CFRT)表達增加的「Ductal-Type」,以及未發生KRAS基因突變,胰腺的導管細胞標記基因(PTF1A)高度表達的「Acinar-type」。
另外發現,在非胰腺消化系統源NEC中,「TP53和RB1基因異常」與「TP53和CCNE1或者MYC基因異常」相互排斥發生,二者都具有結構多態性。此外,胃NEC和大腸NEC各有一例是由病毒感染引起的,這兩個病例未發現TP53和RB1基因異常。
消化系統NEC的特徵是轉錄因子SOX2和ASCL高度表達,研究發現,這是由各基因的啟動子區域的甲基化引起的,尤其是SOX2高度表達的NEC,促進了基因轉錄。
以往的報告認為可能存在由胰腺NET轉成胰腺NEC的情況,但此次首次確認二者明顯不同。NET中不存在NEC常見的RB1基因異常,基因突變也不同,另外還發現,雖然不是全部,但胰腺NET會高頻率發生染色體水平的缺失、全基因體重複,以及參與維持染色體結構的MEN1基因突變。
今後有望以此次明確的相關基因為靶標,推進新藥開發。
原文:《科學新聞》
翻譯編輯:JST客觀日本編輯部













