肝臟一直是奮戰在針對各種抗原的免疫最前線,但也容易因外部的刺激而發生急性肝傷害或肝耗竭。對此,近年來除了肝移植外,使用可以分化為骨骼或脂肪等多種組織的「間充質幹細胞(MSC)」的治療方法也備受關注。MSC能抑制肝臟的發炎,並通過細胞分泌的細胞外囊泡(EVs)促進抗炎作用,但需要開發一種更簡單的方法。
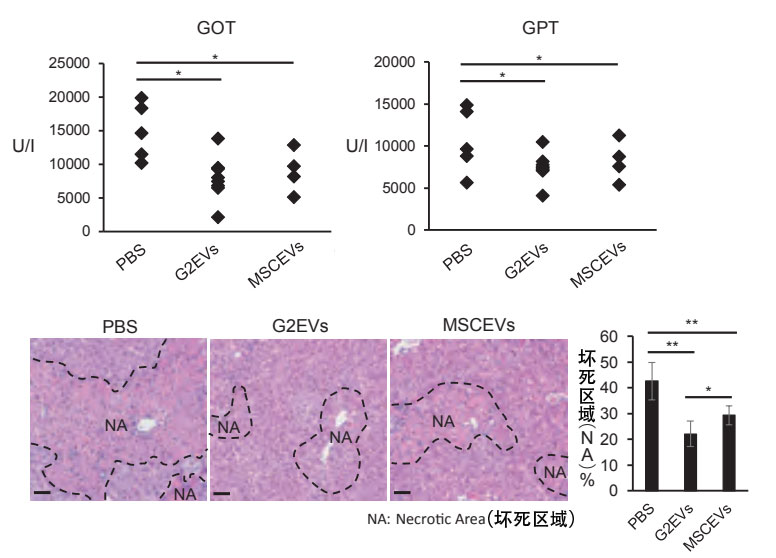
誘導小鼠發生急性肝傷害並測量表示肝臟傷害情況的指標GOT和GPT,通過染色評估了組織壞死區域。由此發現,施用EVs可抑制GOT和GPT升高,組織的肝細胞壞死區域也大幅減少。(PBS:未施用EVs,G2EVs:施用源自肝細胞的EVs,MSCEVs:施用源自MSC的EVs)
因此,日本東海大學的幸谷愛教授等人組成的研究團隊驗證了肝細胞分泌的EVs是否也會像MSC一樣發揮抗炎效果,以及脂肪酸是否在該機制中起到了作用。具體來說,為提前培養的肝傷害模型小鼠施用了源自肝細胞的EVs和源自MSC的EVs。結果顯示,源自肝細胞的EVs與源自MSC的EVs相比,顯示出了相同或更高的抗炎效果,顯著降低了作為肝傷害指標的血清酶(GOT和GPT)的值。
另外,為分析這些抗炎效果源自EVs的哪部分,研究團隊還調查了EVs表面覆蓋的磷脂。由此發現,富含脂肪酸二十二碳六烯酸(DHA)的EVs會作用於肝臟和骨髓,抑制發炎。此外,研究團隊還自主開發了增強EVs的生物學效應的新修飾法(SPREDs),並申請了專利。今後預定將SPREDs應用於源自肝細胞的EVs,並開發針對新冠病毒(COVID-19)引起的細胞介素風暴的蠻力抗炎和組織保護治療法。
文:JSTnews 2022年1月號
翻譯編輯:JST客觀日本編輯部














