治療阿茲海默症等癡呆症的「新方法」正在加速開發之中。一種向頭部照射超音波的治療方法年内將在日本啟動最終臨床試驗。另外還有研究表明,利用幹細胞進行神經再生的可能性也已得到證實。無論哪種方法,作用原理都不同於2021年在美國有條件批准的美國渤健和衛材的治療藥物,目標是實現根本性的治療。
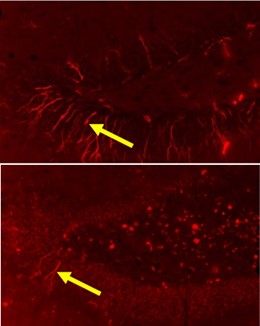
小鼠的海馬體。年輕個體(上)可以看到神經細胞。高齡個體施加幹細胞後神經細胞出現增加(下)(供圖:神戶醫療產業城市推進機構田口明彥部長)
開發利用超音波治療癡呆症的方法的,是東北大學的校辦初創企業Sound Wave Innovation(SWI,東京中央區)。該方法是在患者頭部佩戴專用裝置,並照射1個小時的超音波。每週照射3次為一個療程,每3個月重複一個療程。
該方法的安全性已在2018~2019年的臨床試驗中得到了確認。從2019年開始針對輕度阿爾茨海默型癡呆症患者和輕度認知障礙(MCI)患者等約20人實施了臨床試驗。初步分析顯示,癡呆症的症狀發展有減緩的趨勢。計劃年内增加人數,啟動最終階段的臨床試驗。如果能證明治療效果,預計2026年可通過藥事審批。
SWI是國際醫療福祉大學的副院長下川宏明於2020年創辦的企業。下川通過動物實驗確認,超音波會增加腦内名為「eNOS」的物質。eNOS被認為能擴張血管,抑制引起阿茲海默症的蛋白質「β澱粉樣蛋白」前段物質的產生。下川認為,這種物質有助於抑制認知功能的下降。
治療時向頭部照射32個特定頻率的超音波。使用16個或48個同樣頻率的超音波照射時未能獲得有效物質的明顯增加,目前還不清楚其原因。澄清詳細機制將是實用化和提高治療效果的一個課題。
2021年美國有條件批准的渤健和衛材的治療藥物「ADUHELM」可減少腦内的β澱粉樣蛋白,但在部分臨床試驗中未能顯示出其有效性,銷售一直比較低迷。在日本還未獲得審批。
β澱粉樣蛋白的減少與抑制症狀進展的效果之間的關係尚不明確,這使得癡呆症治療藥物的開發變得困難。靶向β澱粉樣蛋白的其他治療藥物也在推進臨床試驗,但還不清楚能否取得足夠的治療效果。
此外,還有研究人員在挑戰完全不同的方法。神戶醫療產業都市推進機構的田口明彥部長等人已證實,為動物施用產生紅血球等的造血幹細胞後,負責短期記憶的海馬體的神經細胞會增加。短期記憶失落,也即遺忘近期發生的事,是阿茲海默症的症狀之一。
另一項動物實驗證實,通過施用幹細胞可以改善記憶、學習和運動能力等。田口部長等人認為,造血幹細胞會促進血管再生,從而增加神經細胞。其詳細機制將在今後進行調查研究。
田口部長就常規的治療藥物開發存在的課題指出:「使用了即使不是高齡,β澱粉樣蛋白也不斷積聚的特殊模式小鼠」。他在實驗中使用了2歲左右的高齡小鼠,這可能更適合作為癡呆症的模型。
除β澱粉樣蛋白外,另一種被指出與阿茲海默症有關的蛋白質是「Tau」。衛材等正在開發靶向Tau的治療藥物。
東京大學的岩坪威教授等人明確了從大腦中去除Tau的機制。神經細胞内形成的Tau可通過腦脊髓液從大腦中去除。此時參與Tau去除的是腦血管附近的「水通道蛋白4」。增強這種蛋白質的功能可能會有助於治療。
根據世界衛生組織(WHO)的預測,癡呆症患者今後會繼續增加。亟需開發出高效的治療方法。
日文:尾崎達也、《日經產業新聞》,2022/04/13
中文:JST客觀日本編輯部













