京都大學的竹内理教授等人組成的研究團隊開發出了有助於開發抑制免疫失控的核酸藥物的方法。該團隊開發出了增強免疫抑制酶功能的核酸,並在小鼠身上確認了有效性。今後將研究核酸的種類和給藥方法,以盡快在自體免疫性疾病和難治性發炎性疾病等領域實用化。

利用了給免疫「剎車」的酶(供圖:京都大學竹内理教授)
通常負責保護身體免受外敵攻擊的免疫系統,由於某種原因開始攻擊自身的疾病被稱為自體免疫性疾病。常見的自體免疫性疾病包括伴有肢體麻痹和視力異常等的多發性硬化症等,並且尚未確立有效的治療方法。
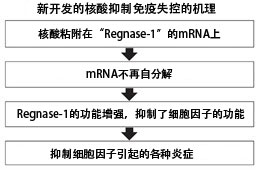
人體內有控制免疫系統失控的機制,竹内教授的研究團隊著眼於其中的一種酶「Regnase-1」。Regnase-1能夠分解在體內傳遞引起各種發炎反應的細胞介素的傳訊RNA(mRNA)。研究團隊認為,增強Regnase-1的功能,就能減少細胞介素,從而抑制過度免疫。換句話說就是免疫製動功能,已知Regnase-1的作用與潰瘍性大腸炎等很多疾病有關。
不僅是細胞介素,Regnase-1還會通過分解自身的mRNA來調節功能。研究團隊認為,抑制mRNA的自分解可以增加Regnase-1。Regnase-1通過識別自身mRNA的獨特髮夾狀結構來分解mRNA。因此,研究團隊設計了核酸的鹼基序列,使其可以粘附在髮夾結構上,以抑制mRNA的自分解。
研究團隊利用小鼠驗證了是否真的有抑制發炎性疾病和自體免疫性疾病症狀的效果。在人為引起小鼠肺纖維化前後使用這種核酸發現,抑制了肺部的發炎。肺纖維化是一種肺部組織變硬,病人無法正常呼吸的疾病,目前尚無有效的治療方法。另外,還抑制了因免疫失控,肺部積水而發生重度呼吸耗竭的「急性呼吸窘迫症候群」的症狀。
研究團隊還調查了對自體免疫性疾病之一的多發性硬化症的效果。多發性硬化症是神經周圍的組織受到破壞,從而引起麻痹症狀等的難治性疾病。當為小鼠施用會引起多發性硬化症的藥物並在發病前向小鼠大腦施用新開發的核酸發現,麻痹等症狀得到了抑制。
竹内教授表示,此次確認了利用核酸增強Regnase-1的功能從而抑制發炎的「新治療概念實現的可能性」,強調了該成果的意義。現已開始與核酸藥物專家和企業推進聯合研究,將研究人用核酸的設計和給藥方法,以及針對的疾病等。雖然還存在很多課題,但對難治性疾病的效果值得期待,因此「希望能盡快實現實用化」(竹内教授)。
日文:藤井寬子、《日經產業新聞》,2022/5/18
中文:JST客觀日本編輯部













