北海道大學研究生院藥學研究院的鍛代悠一助教和松田正教授等人組成的研究團隊發現,抗癌藥物拓撲替康通過抑制新的靶蛋白RPL15,會促進癌症免疫的激活。相關内容已經發布在Journal of Immunology上。
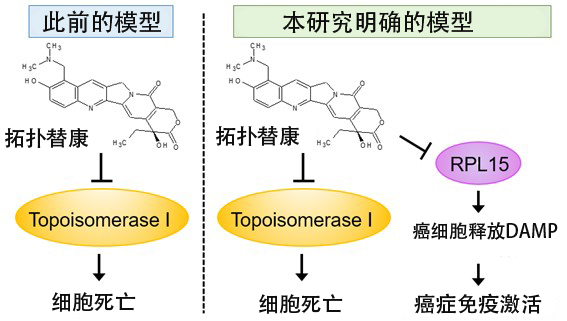
圖:研究團隊發現,拓撲替康通過與新靶點RPL15結合,會抑制60S核糖體次單元前驅體的形成,並誘導癌細胞釋放DAMP。另外,抑制癌細胞中的RPL15會誘導DAMP介導的癌症免疫激活,荷瘤小鼠模型通過抗PD-1抗體增強了抗腫瘤效果。本研究表明,RPL15有望成為提高癌症免疫療法治療效果的新藥物靶點。(供圖:北海道大學)
已知細胞在受到化學物質、輻射和溫度壓力等傷害時會釋放名為DAMP的免疫激活分子。癌細胞釋放DAMP會促進癌症免疫的激活和相關癌細胞的消除,因此被認為會影響癌症治療的效果。
研究團隊此前曾報告,用拓撲替康處理過的癌細胞會釋放激活免疫的DAMP,促進癌症免疫。然而,一直不清楚是什麼樣的機制誘導了這種現象。
為此,為了探索拓撲替康的新靶蛋白,研究團隊製作了結合拓撲替康的珠粒,通過與癌細胞的細胞提取液混合後使珠粒沉澱,回收了拓撲替康結合蛋白。通過全面分析回收的蛋白質,確定RPL15為新的拓撲替康結合蛋白。接下來,為驗證RPL15與癌細胞釋放DAMP的關係,把通過敲低減少了RPL15生成的皮膚癌(黑色素瘤)細胞移植到小鼠體內,評估了腫瘤内浸潤的免疫細胞的成分和活化狀態。
結果顯示,敲低了RPL15的腫瘤與對照組相比腫瘤的生長速度明顯下降。另外,對照組的腫瘤未發現抗PD1抗體的腫瘤抑制效果,而在敲低了RPL15的腫瘤中,抗PD1抗體顯著降低了腫瘤生長速度。此外,通過流式細胞術分析腫瘤内浸潤的免疫細胞發現,在敲低了RPL15的腫瘤中,細胞毒性T細胞顯著增加,而抑制癌症免疫的調節性T細胞減少。這些結果表明,抑制RPL15可以將腫瘤微環境變成容易通過細胞毒性T細胞誘導細胞毒性的環境,同時還會通過抗PD1抗體增強抗腫瘤效果。
今後如果能開發出不作用於拓撲異構酶I的RPL15獨特性抑制劑,將有望為抗PD1抗體等癌症免疫療法的改良做貢獻。
原文:《科學新聞》
翻譯編輯:JST客觀日本編輯部
【論文資訊】
期刊:Journal of Immunology
論文:Identification of RPL15 60S ribosomal protein as a novel topotecan target protein that correlates with DAMP secretion and antitumor immune activation
URL:jimmunol.org/content/209/1/171













