由日本原子能研究開發機構原子能基礎工學研究中心放射線行為解析研究團隊的骨幹研究員古田琢哉和日本量子科學技術研究開發機構(QST)量子生命和醫學部門放射線醫學研究所放射線管理科學研究部主任研究員古場裕介等人組成的研究團隊,於8月25日宣佈開發出了對接受重粒子射線治療後患者全身輻射量進行評估的「RT-PHITS for CIRT」系統,以闡明重粒子射線治療後發生繼發性癌症的機制。該系統可以根據過去臨床治療數據,在計算機上重現每位患者各不相同的複雜的輻射體系,通過模擬試驗,對患者全身輻射量進行高精度評估。由此希望獲得以重粒子射線治療為首的風險更定的放療成果。該研究成果已經發表在國際科學雜誌《Physics in Medicine and Biology》上。
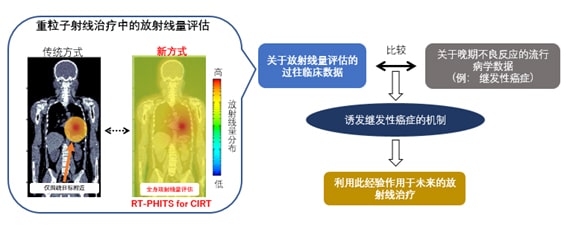
圖1:新開發的放射線量評估系統 (RT-PHITS for CIRT) 的作用(供圖:日本原子能研究開發機構)
放射線療法是通過對治療對象的癌等腫瘤靶點照射一定的放射線能,讓腫瘤細胞死亡的一種治療方法。儘管治療計劃中會儘可能地將射線集中在腫瘤部位,但由於不可能完全遮蔽射線,所放射線療法存在著誘發繼發性癌症的風險。繼發性癌症為放療後出現的腫瘤轉移和非腫瘤複發等所有新出現的癌症,有報告顯示,X線放療後出現繼發性癌症的機率有意義地高於手術等非放射線治療方法。
作為放射線療法中的一種,重粒子射線療法與X線療法相比,線量可以更加集中於病竈,已有報告顯示,尤其是對前列腺癌而言,與X線放療相比,重粒子射線療法出現繼發性癌症的機率要低。另一方面,目前尚沒有能夠對發生繼發性癌症的照射部位以外的全身輻射量進行檢測的系統,無法做定量評估。對重粒子線療法的輻射量分佈評估還僅限於照射部位的周圍,用來觀察治療效果和避免周圍重要臟器發生急性功能障礙。
繼發性癌症發生的機率非常低,為了弄清原因,需要根據患者體內輻射劑量的詳細分佈,以不同臟器以及眾多患者為對象,調查輻射量水平、繼發性癌症的發生頻率等。
為此,研究團隊為了闡明重粒子射線治療導致繼發性癌症的機制、以及發生頻率較低的原因,決定開發一個能夠檢測全身輻射量的系統。
在重粒子線治療中,需要在碳離子組成的重粒子線束上放置多個防護罩,根據每個患者腫瘤形狀的不同,生成射線束,以腫瘤為靶點進行集中照射,這些資訊均記錄在治療方案中。由於碳離子是由錯離子構成的,在照射時與檢查裝置、防護罩碰撞以及在患者體內發生衝突產生二次粒子,離開照射部位的線量就是由這些二次粒子造成的。評估全身輻射量時,需要通過計算機重現重粒子線的複雜照射系統,並模擬二次粒子的產生。
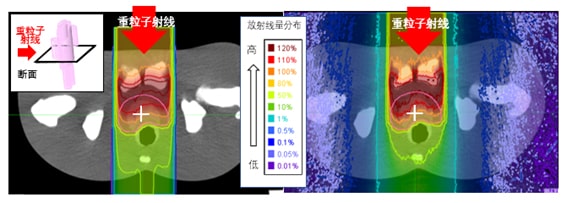
圖2. 在擬人化幻影中,傳統計算方式(左)與新開發系統(右)的放射線量分佈比較(供圖:日本原子能研究開發機構)
新開發出來的系統按照重粒子射線治療的治療方案數據,在計算機的虛擬空間中再現了治療時的照射體系。通過利用主要由該機構開發的蒙特卡洛輻射行為分析碼「PHITS」,準確模擬了照射系統中重粒子射線以及二次粒子的行為,從而實現了評估整個患者全身輻射量的詳細分佈情況。此外,通過將這些過程自動化,構築了一個能夠處理病人大量數據的系統。不但能夠評估治療部位的輻射量分佈,還可以評估離開治療部位的其他身體部位以及低於1%的低輻射量的分佈情況。
此外,該系統還能將輻射量分佈轉換為DICOM數據,並利用基於DICOM數據的圖像整合軟體,將輻射量疊加在患者的CT圖像上。
古田骨幹研究員表示:「今後將使用該系統,對量研(QST)保存的重粒子射線治療病例重新進行評估。QST擁有世界最多的病例數據。通過對每個患者的治療輻射量進行評估和跟蹤調查,可以對病人是否發生了繼發性癌症、以及是否發生了副作用等進行比較,以明確在什麼條件下會發生繼發性癌症,以及為什麼重粒子射線治療不容易引起繼發性癌症。首先將對接受X射線治療後的約200個前列腺癌病例進行分析。通過闡明機制,相信在未來將有助於提高放射治療的安全性。」
古場主任研究員表示:「今後,將會在重新分析QST積累的治療數據的同時,與其他研究機構合作,共同評估接受X射線治療患者的輻射量並與重粒子射線治療進行比較分析,明確發生繼發性癌症的原因。」
原文:《科學新聞》
翻譯:JST客觀日本編輯部
【論文資訊】
雜誌:Physics in Medicine and Biology
論文:Development of the DICOM-based Monte Carlo dose reconstruction system for a retrospective study on the secondary cancer risk in carbon ion radiotherapy
DOI:https://doi.org/10.1088/1361-6560/ac7998













