東京大學和大阪大學正在挑戰因事故等原因失去的手足的再生。該方法並非在試管中培養肢體,而是使用「直接重程式設計(DR)」技術促進在人體內部的再生。通過靈活應用在新型冠狀病毒疫苗中廣泛使用的傳訊RNA(mRNA)技術,在防止再生細胞癌變的問題上也開始迎來了曙光。
該項研究已被納入2021年政府大型科研項目「登月型研發事業」。項目成員由東京大學醫學部、工學部、大阪大學工學部的研究人員組成,擔任項目總監的東京大學慄田昌和講師幹勁十足地表示:「我們的目標是在2040年達到臨床應用的水平,2050年在一定程度上普及這種治療方法」。
再生醫療技術較為人熟知的是使用能分化為神經、肌肉等各種組織細胞的富潛能幹細胞(萬能細胞)的方法。例如,京都大學的山中伸彌教授開發的iPS細胞就是通過在皮膚等纖維母細胞的細胞中導入特定基因製作而成的。與此相對,DR是一種不通過萬能細胞而將纖維母細胞等細胞直接轉化為目標細胞的方法。
與iPS細胞在培養上耗費時間和成本相比,DR可以降低成本。此外,慄田講師指出「DR更適合用於生成再生手足」。將試管培養的細胞移植到體內時,形狀越複雜的組織血流越不通暢,越難以生成。採用DR可以像蜥蜴的尾巴那樣在體內再生組織。
DR的研究從1990年代開始,主要圍繞以皮膚細胞轉化成肌肉細胞的技術展開。隨著2006年山中教授發表iPS細胞的相關論文,把將細胞根據目的轉化的基因搜尋方法應用於DR的研究開始推廣。在日本,相關研究以筑波大學和九州大學等為主進行。
慄田講師原本的專業研究是「褥瘡」,這是因長期臥牀不起的患者背部和腰部長期受壓而導致的皮膚循環障礙。為了快速治癒通常需要經過數月治療的褥瘡,他開始研究DR。褥瘡癒合一般是從傷口邊緣逐漸再生皮膚細胞, DR則可以在整個創傷表面同時全面再生皮膚細胞,所以能夠加速癒合。
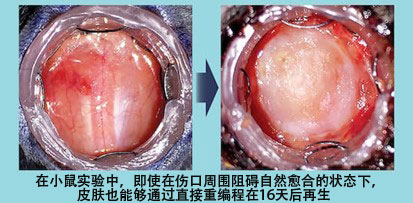
通過歷時15年的研究,慄田講師從86種候選基因中發現了4種能夠再生皮膚的基因體合。在小鼠實驗中,即使在傷口周圍安裝圓筒阻礙自然治癒的條件下,傷口仍能在2周後癒合。慄田講師又花費3年時間,成功再現了皮膚所具備的功能。通過發現能夠使細胞回到接近胎兒的狀態,具有高度再生能力狀態的基因體合,再生出了滋潤皮膚的「脂腺」和生長毛髮的「毛囊」。
應用這種組織胎兒化研究,慄田講師從2021年開始挑戰小鼠的前後肢再生實驗。目前已經確認到可以通過DR從缺損面生長出骨骼和軟骨。今後將尋找能夠同時再生肌肉和神經的基因體合。
為防癌方法帶來光明

慄田講師等人推進的DR研究,在疫情防控方面被廣泛應用的技術意外地起到了推進作用。
儘管動物實驗已經獲得成功,但皮膚再生治療仍未能夠投入實用的原因之一是副作用方面的擔憂。該技術中使用病毒載體分子攜帶細胞轉化基因。這種載體雖然能夠用於各種基因療法,但仍有極個別的情況會出現細胞遺傳資訊被改寫導致癌變的風險。慄田講師表示:「有人指出這種皮膚再生方法帶來的風險與獲益不相配對分組」。
作為代替病毒載體分子候選的便是mRNA。由於導入的是轉錄基因的RNA(核糖核酸)而非基因本身,所以可以避免癌變的擔心。
新冠疫情發生之前,幾乎沒有能夠設計與生產mRNA的設備以供研究,研究人員也很難確保高額的研究委託費用。在新冠防治中,伴隨著mRNA疫苗開發的推進,mRNA的設計生產設備在製藥業界迅速普及。由此將mRNA應用於DR研究也有了眉目。
日文:寺岡篤志、《日經產業新聞》、2022/10/14
中文:JST客觀日本編輯部













