新一代癌症治療藥物「靶向蛋白降解藥」的研發勢頭正盛。因能針對性攻擊引起疾病的蛋白質(病原蛋白)有望獲得較高療效而頗受期待。安斯泰來製藥表示將正式投入經營資源,率先在日本企業中首次開展臨床試驗。引領該公司研發的是蛋白降解藥部門長早川昌彥。

安斯泰來製藥蛋白降解藥部門長早川昌彥
——靶向蛋白降解藥是一種怎樣的藥物?
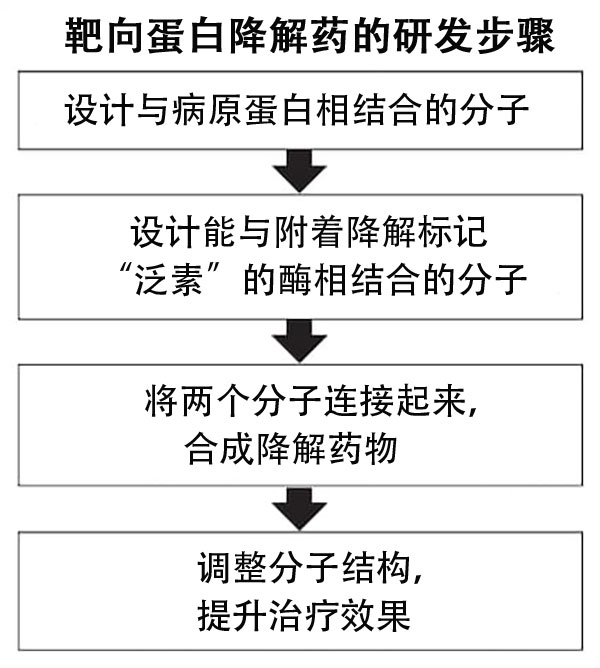
早川:是一種促進病原蛋白分解的低分子藥物(低分子化合物類藥物)。它利用了細胞原本就具備的能夠分解非需要蛋白質的機制。讓作為分解標記的泛素分子與病原蛋白、以及附著在病原蛋白上的酶相結合,就可以將兩者聯在一起促進分解。
以往的癌症治療藥物主要是抑制劑型,它與癌細胞增殖相關的蛋白質相結合以阻礙其功能。然而,能與治療藥物緊密結合的「深口袋」病原蛋白僅約兩成左右,對於除此之外的癌細胞則難以開發治療藥物。降解藥物即便口袋很淺也能發揮作用,理論上可以把所有病原蛋白作為攻擊目標。
——2022年美國已開始了臨床試驗。
早川:臨床試驗的對象是特定基因變異導致的大腸癌。這種基因變異引發的腫瘤中,名為KRAS蛋白質的第12個氨基酸從甘胺酸更換成了天冬醯胺酸。由於結合口袋淺,治療藥物開發較為困難。能進入臨床試驗正好是因為降解藥物才得以實現的成果,希望最早在2023年内就能得出結果。
——藥物開發有可能發生怎樣的改變?
早川:這關係到一些已放棄研發藥物的重生。美國臨床試驗中的候選新藥,將作為抑制劑效果不佳的藥物改為降解藥物的「零件」,使其重生。換句話說就是把過去的失敗變成了寶庫。
此外靶向蛋白降解還有利於提高藥物開發效率。通常藥物的合成需要幾年時間,但此次降解藥物的合成僅用了5個月,這一速度是空前的。此前也有合成數千種以上藥物的情況,但此次在合成第38種藥物時就得到了能夠進入臨床試驗的候選藥物。除了對可用於降解藥物使的各種成分(分子)進行高效搜尋外,藥物設計還使用了人工智慧(AI)和機器人技術。
——對安全性等方面有顧慮嗎?
早川:我認為可以開發出僅對體內的針對性部位起作用的降解藥物。可在病原蛋白上附著泛素的酶約有600種,有的會在特定的癌部和器官中發揮作用。所以可以根據藥物設計的不同來使用適當的酶。
目前針對其它病原蛋白的降解藥物也在開發中。希望將來也能應用於免疫疾病等。雖然有人說(經過多年推進的)低分子藥物的研發已經到了極限,但降解藥物的出現讓人們切實感受到低分子藥物還大有可為。
利用研究的積累來改變落後局面
國外的企業在開發靶向蛋白降解藥方面處於領先地位。美國初創企業Arvinas正與美國大型製藥公司輝瑞共同以乳房癌患者為對象開展臨床試驗。2022年宣佈其研發的藥物在第二階段臨床試驗中對38%的患者有效,最快2023年内將開始最終階段的臨床試驗。
雖然目前還沒有成功將靶向降解藥物用於實際治療的案例,但近年來的研究表明,用於治療多發性骨髓瘤的沙利度胺類抗癌藥的作用機制與降解藥物相同。沙利度胺類藥物的年銷售額超過1萬億日元,期待靶向降解藥物中也能出現優秀的癌症治療藥物。
日本從早期開始就為降解藥物的研發和機制闡明做出了貢獻。早川表示「日本有很多低分子藥物所需的化學合成專家」,如果能發揮這一優勢,日本還有充分的機會改變局面。
日文:遠藤智之、《日經產業新聞》、2023/1/30
中文:JST客觀日本編輯部













