京都大學整合細胞材料科學研究所(iCeMS)客座副教授龜井謙一郎(兼任紐約大學阿布扎比分校副教授)、研究生院工學研究科工學基礎教育研究中心的平井義和講師、微工程專業楊建東博士等人組成的研究團隊,使用微流路研發了可在體外模擬再現非酒精性脂肪性肝病(NAFLD)的腸肝臟器模式晶片。目前NAFLD尚未開發出有效的診斷及治療藥物,研究成果有望促進病狀的闡明和新治療藥物的開發。相關研究成果已發表在《Communications Biology》上。
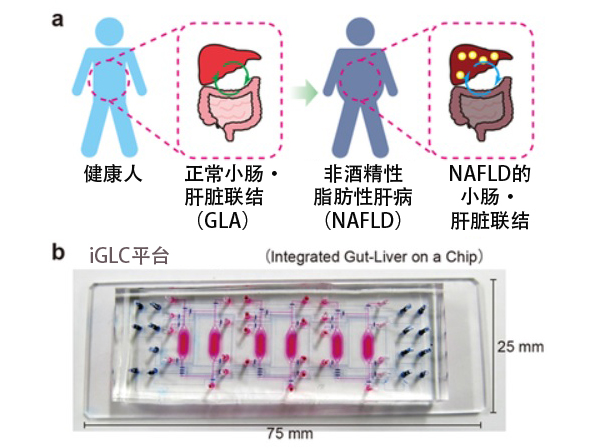
圖(a)非酒精性脂肪性肝病(NAFLD;Non-alcoholic fatty liver disease)的小腸·肝臟聯結(GLA)。(b)模擬GLA的iGLC平台(Integrated Gut-Liver on a Chip)(供圖:京都大學)
全球患者人數持續增加的NAFLD(Non-alcoholic fatty liver disease,非酒精性脂肪性肝病)是一種慢性肝病,可導致脂肪肝、肝硬化、癌症和心血管疾病。一旦演變為重症,肝移植是唯一的治療手段,但找到供體非常困難。由於NALFD發生在一個高度複雜的過程中,因此其疾病機制目前尚不明確。而藥物開發需要深入瞭解每個過程。
龜井客座副教授和平井講師一直以來都在共同致力於生物組織晶片的開發。此次開發的被稱為iGLC平台(Integrated Gut-Liver on a Chip)的腸肝臟器模式晶片就是其中之一。
iGLC平台在晶片内配備了可以精確控制細胞培養液流動的微閥和泵,實現了分別連接各個細胞培養室,以及連接小腸和肝細胞的培養液循環流動。
使用該平台共同培養腸和肝細胞,並投放已知可誘導NAFLD的遊離脂肪酸(FFA:Free Fatty Acid),能夠成功誘導出代表初期和進行性NAFLD的細胞狀態(細胞内脂質貯存等)。此外,結合mRNA測序和顯微成像進行單細胞分析,還可以研究NAFLD狀態下與獨特的細胞表同質多相變體化相關的基因網路。
在遊離脂肪酸處理的有無、單培養和共培養等共計4種條件下,研究團隊確定了存在基因表現差異的654個基因(小腸細胞)和1330個基因(肝細胞)。證實小腸細胞和肝細胞的共同培養降低了遊離脂肪酸對基因表現的調節。
與單獨培養的傳統細胞培養實驗法相比,通過使用該平台,新發現了小腸細胞和肝細胞對遊離脂肪酸能夠起到相互保護的作用。
龜井客座副教授表示,「目前,我們正在與製藥公司進行聯合研究,以確定可以在多大程度上模擬何種類型的病狀。使用組織模式晶片,即使在前臨床和疾病模型研究中不使用動物,也能更高效地研製藥物。」
原文:《科學新聞》
翻譯:JST客觀日本編輯部
【論文資訊】
雜誌:Communications Biology
文章:Integrated gut–liver-on-a-chip platform as an in vitro human model of non-alcoholic fatty liver disease
DOI:10.1038/s42003-023-04710-8













