將癌組織轉變為急性發炎組織,讓免疫細胞對其進行攻擊——日本九州大學研究生院工學研究院的新居輝樹助教、片山佳樹教授、一貫製博士課程4年級學生谷戶謙太等人組成的研究團隊在世界上首次開發出了用癌症引發發炎的細胞藥物「MacTrigger」。該細胞藥物採用了非直接攻擊癌細胞,轉而利用巨噬細胞激活人體排異功能的新概念。新居助教表示:「將努力在10年内開始臨床試驗」。相關研究成果已刊登在《Journal of Controlled Release》上。
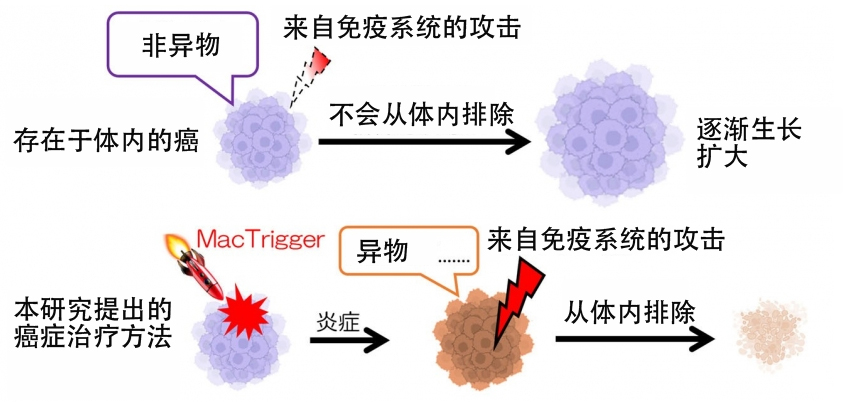
研究概念圖(供圖:九州大學)
癌細胞會通過釋放多種物質來躲避人體免疫細胞的攻擊。PD1抑制劑雖然可以防止這種免疫躲避,但其效果因患者不同存在很大差異。
此次研究團隊著眼於免疫細胞之一的巨噬細胞。已知巨噬細胞會積極聚集在癌細胞附近,這些聚集的巨噬細胞會從普通型(M0型)向抗發炎型(M2型)極化。研究團隊利用巨噬細胞的這一特性開發了轉基因巨噬細胞「MacTrigger」,在巨噬細胞極化為M2型時,能夠立即釋放發炎因子TNFα(腫瘤壞死因子α)。新居助教介紹說「TNFα是各種發炎因子中最好的。這是因為我們受傷時最先出現的就是TNFα。」
MacTrigger被程式設計為在到達癌症部位後大約4天内消失。將MacTrigger注射到大腸癌小鼠體內8天后確認了抗癌效果。具體效果為,腫瘤内NK細胞(自然殺手細胞)的比例從約1%增加至約5%,殺傷性T細胞從約6%增加至約15%。在給藥第16天的階段,與未治療組相比,給藥組的腫瘤體積縮小到了3分之1左右,存活率也上升到100%(未治療組約為20%)。
但是,如果這種引起發炎的物質作用於全身,將會十分危險,因此,為了使MacTrigger隻對癌症部分發揮作用,研究團隊加入了只要從癌細胞釋放的精胺酸酶-1不超過一定水平,TNFα就不會大量釋放的鎖定功能。在沒有鎖定功能的情況下,觀察到肝肥大和血液中AST(穀草轉氨酶)值升高現象,但通過導入鎖定功能,已確認可以避免這些問題。
迄今為止,巨噬細胞由於基因導入率低,作為細胞藥物並未受到太多關注。研究團隊研究了多種提高巨噬細胞轉基因導入效率的基因重組方法,通過藥物篩選選出基因導入細胞,成功獲得了可用於治療水平的細胞量(100萬個)。
新居助教表示:「為了應用於實際治療,必須減少細胞數,所以我們正在進行各種嘗試。另外,我們還在研究今後能否用血液單核球製作MacTrigger。將來的目標是實現利用採血製作MacTrigger,並用於癌症治療。」
原文:《科學新聞》
翻譯:JST客觀日本編輯部
【論文資訊】
雜誌:Journal of Controlled Release
論文:Engineered macrophages acting as a trigger to induce inflammation only in tumortissues based on arginase 1-responsive TNF-α accelerated release
DOI:10.1016/j.jconrel.2023.04.010













