隨著肥胖的增加,全球範圍內在因子膽固醇過度累積而患上非酒精性脂肪性肝病(nonalcoholic fatty liver disease,NAFLD)的患者數量不斷在增加,部分NAFLD會發展為以發炎和纖維化為主要特徵的非酒精性脂肪性肝炎(nonalcoholic steatohepatitis,NASH)。日本也是如此,隨著生活方式的西化,體檢診斷出NAFLD的患病率為9~30%,其中約10%被推定為NASH。10~20%的NASH患者會出現肝硬化和肝癌。然而,由於導致NASH形成的因素尚未完全闡明,因此除了飲食和運動療法外,尚無有效的治療方法。
京都大學研究生院醫學研究科循環器内科的尾野亙教授、堀江貴裕助教在對miRNA進行泛函分析的過程中發現,肝細胞的miRNA-33b(miR-33b)在NASH形成中發揮著重要作用。此外,還發現通過投餵獨特性抑制33b的合成核酸,可以抑制NASH小鼠模型的發炎、纖維化和肝傷害,表明這種核酸藥物可用於治療NASH。尾野教授表示:「今後將繼續開發以應用於實際治療」。該研究成果已發表在《Life Science Alliance》上。
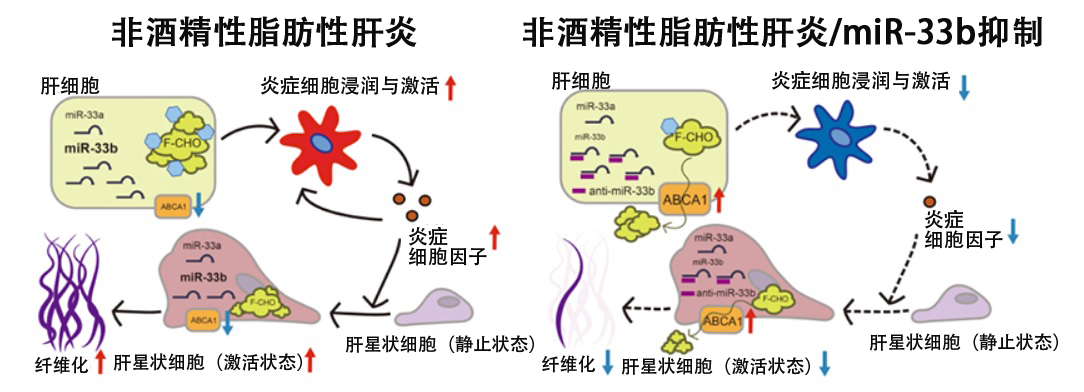
圖1 肝細胞和肝星狀細胞中miR-33b的表達高於miR-33a,通過投餵anti-miR-33b,肝細胞及肝星狀細胞的ABCA1表達上升,且通過減少這些細胞内遊離膽固醇和肝内膽固醇結晶,減輕了肝臟發炎反應和纖維化。因此,肝細胞和肝星狀細胞中的miR-33b對於NASH發病具有重要作用,抑制miR-33b有望成為新的NASH治療方法。(供圖:京都大學)
研究團隊此前已明確,小鼠的miRNA-33可抑制細胞内膽固醇轉運蛋白ABCA1的表達。ABCA1將膽固醇從細胞内輸送到細胞外,形成好膽固醇。因此,激活miRNA-33會抑制ABCA1並降低好膽固醇。實際也已確認缺失miRNA-33的小鼠的動脈硬化和主動脈瘤的形成受到了抑制。
小鼠體內的miRNA-33只有1種,而人體內則有2種,為此將與小鼠位於同一位置的命名為a,另一個命名為b。33b的作用尚不明確。
研究團隊製作了人源化基因敲入小鼠,並在與人類相同的位置插入了33b。這種小鼠中,33a和33b均有表達,且與野生型相比,動脈硬化加劇。
對小鼠肝臟的整體脂質分析表明,表達33a的小鼠脂質較多,而同時表達33a和33b的基因敲入小鼠具的脂質更多。
當給基因敲入小鼠投餵高脂肪食物後發現,脂肪在肝臟中累積,並伴有發炎和纖維化,以及表現出NASH症狀。此外,肝臟中的膽固醇和甘油三酯過度累積。相反,使肝細胞獨特性缺失33b後,NASH表達型得到改善,而使巨噬細胞獨特性缺乏33b也沒有改善表達型。堀江助教表示:「我們發現,給基因敲入小鼠投餵高脂肪飲食可使其成為NASH模型小鼠。」
接著,研究人員在生物體中製備了能單獨抑制33a/b的人工核酸,連續12周投餵NASH誘發食物,同時每2周1次向基因敲入小鼠皮下注射抑制33a的人工核酸、抑制33b的人工核酸,及抑制33a/b的人工核酸。
在21周齡時確認給藥效果後發現,在對照組中觀察到小鼠肝臟中膽固醇累積,發炎細胞浸潤,細胞介素增加,肝星狀細胞活化和纖維化進展,而與此相對照,皮下注射人工核酸的小鼠膽固醇累積受到抑制。特別是,對肝臟中高表達的33b顯示出明顯抑制效果,甚至與同時抑制a和b的情況相比,對發炎細胞介素和纖維化基因的抑制更多。
堀江助教表示:「通過此次的實驗,我們發現人源化miR-33b基因敲入小鼠表現出NASH,其中肝細胞的miR-33b尤為重要。」
原文:《科學新聞》
翻譯:JST客觀日本編輯部
【論文資訊】
雜誌:Life Science Alliance
論文:Inhibition of microRNA-33b in humanized mice ameliorates nonalcoholic steatohepatitis
DOI: 10.26508/lsa.202301902













