北海道大學遺傳病控制研究所癌症控制學領域的園下將大教授等人組成的研究團隊發布研究成果稱,製作了模仿胰腺癌患者中觀察到的4個基因突變的胰腺癌模型果蠅,並通過全面篩檢成功找到了新的治療靶點。研究人員還在果蠅(4-hit果蠅)中成功再現了4個基因突變,通過利用這種果蠅對所有激酶進行全面的基因篩檢,找到了新的治療靶點,並證實了這種抑制劑可以提高4-hit果蠅的存活率。這一發現有望促進胰腺癌治療藥物的開發。研究成果已發表在美國癌症協會雜誌《Cancer Research》6月28日號上。
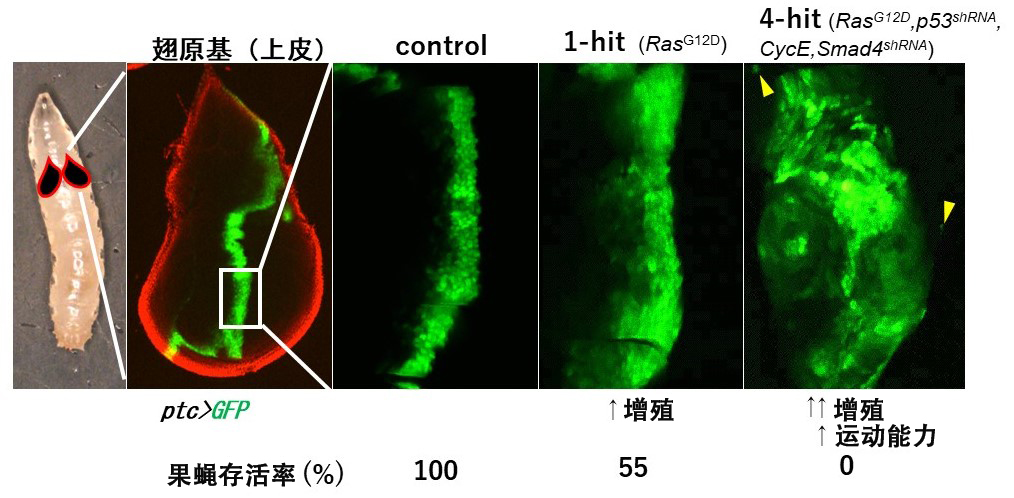
圖 胰腺癌基因型果蠅模型中的腫瘤發生。利用patched (ptc) 基因啟動子活性驅動GFP表達,標記幼蟲翅原基的單層上皮細胞。在「1-hit」果蠅中,Ras基因的激活誘導細胞增殖。此外,改變4個基因的「4-hit」果蠅表型惡化並產生遷移細胞(箭頭),出現致死現象。(供圖:北海道大學)
胰腺癌是治療選項極為有限的難治性癌症之一,癌基因KRAS的活化和抑瘤基因組TP53、CDKN2A和SMAD4的失活可單獨或組合出現。同時具有這4個基因突變的患者預後最差,但目前尚無再現該病況的模型小鼠,新模型動物的製作備受期待。
果蠅攜帶超過70%的人類疾病中觀察到的異常基因,與哺乳動物具有高度的遺傳保存性,以及對應功能的體內構造。
2019年,上述研究團隊利用將甲狀腺髓樣癌基因突變導入果蠅的模型蠅進行了基因篩檢和化合物篩檢,發現了可作為新治療靶點和候選治療藥物的激酶抑制劑。
此次,研究團隊在世界上首次成功製作出再現胰腺癌中出現的4個基因突變的模型果蠅(4-hit果蠅),並通過單獨或組合方式在幼蟲翅原基中再現了與人類各基因對應的果蠅基因的活化和功能減弱。
首先,研究人員製作了在幼蟲的翅原基上皮細胞中僅激活果蠅Ras基因(人類為KRAS基因)的1-hit蒼蠅,並分析了表現型。觀察到細胞增殖加速,約有一半的個體死亡。此外,進一步製作了4-hit果蠅,觀察到翅原基上皮細胞的增殖和遊走能力明顯增強,並且在未羽化之前全部死亡。這些結果證實,果蠅能夠毫無矛盾地反映臨床胰腺癌的病況。
其次,研究人員使用4-hit果蠅對所有激酶進行了全面的基因篩檢。大多數癌症中都發現了激酶的異常,並且被認為與癌症中異常細胞的增殖密切相關。在該分析中,針對4-hit果蠅,研究人員一一製作了缺乏果蠅激酶基因功能的系統,並分析了對病況帶來的變化。據稱,人類大約有500個激酶基因,而果蠅的數量大約是人類的一半。
結果發現,降低MEK和AURKB的活性後,可提高4-hit果蠅的存活率。
於是,研究人員進行了將MEK抑制劑(Trametinib,曲美替尼)和AURKB抑制劑(BI-831266)作為抑制激酶活性的化合物經口給予4-hit果蠅的實驗。
實驗結果表明,與單劑給藥相比,2劑的組合給藥更有助於恢復4-hit果蠅的存活率。並且確認,即使在植入人類胰腺癌細胞的模型小鼠中,2劑給藥也能明顯抑制腫瘤的生長。此外,對北海道大學醫院胰腺癌患者手術樣本的分析顯示,存在磷酸化組蛋白H3(AURKB活化指標)的患者組的預後比沒有磷酸化組蛋白H3的患者組更差。
據該研究團隊稱,已經發現了多個其它的候選新型治療靶點。
園下教授表示:「此次的研究成果揭示了基於果蠅表達系統篩選的藥物研發的可能性。在哺乳動物中很難實現的實驗,但可以在果蠅中有效地進行,相信這種方法也可以應用於胰腺癌以外的其他癌症。未來將在努力研發胰腺癌治療藥物的同時,還將嘗試掌握與胰腺癌發病相關的信號通路的整體情況。」
原文:《科學新聞》
翻譯:JST客觀日本編輯部
【論文資訊】
雜誌:Cancer Research
論文:Drosophila screening identifies dual inhibition of MEK and AURKB as an effective therapy for pancreatic ductal adenocarcinoma
DOI:doi.org/10.1158/0008-5472.CAN-22-3762













