京都大學開發了一種隻在目標細胞中使基因發揮作用的基礎技術。由於治療時基因隻作用於癌細胞等異常細胞,因此有望減輕治療的副作用。此外,還有望降低使用免疫細胞進行治療的成本。目標是在2050年代作為新一代基因療法普及應用。
京都大學iPS細胞研究所(CiRA)的齊藤博英教授等通過識別細胞内的分子,開發出了基因僅在特定細胞中發揮作用的特殊蛋白質。相關研究成果已發表在英國科學雜誌《自然通訊》上。
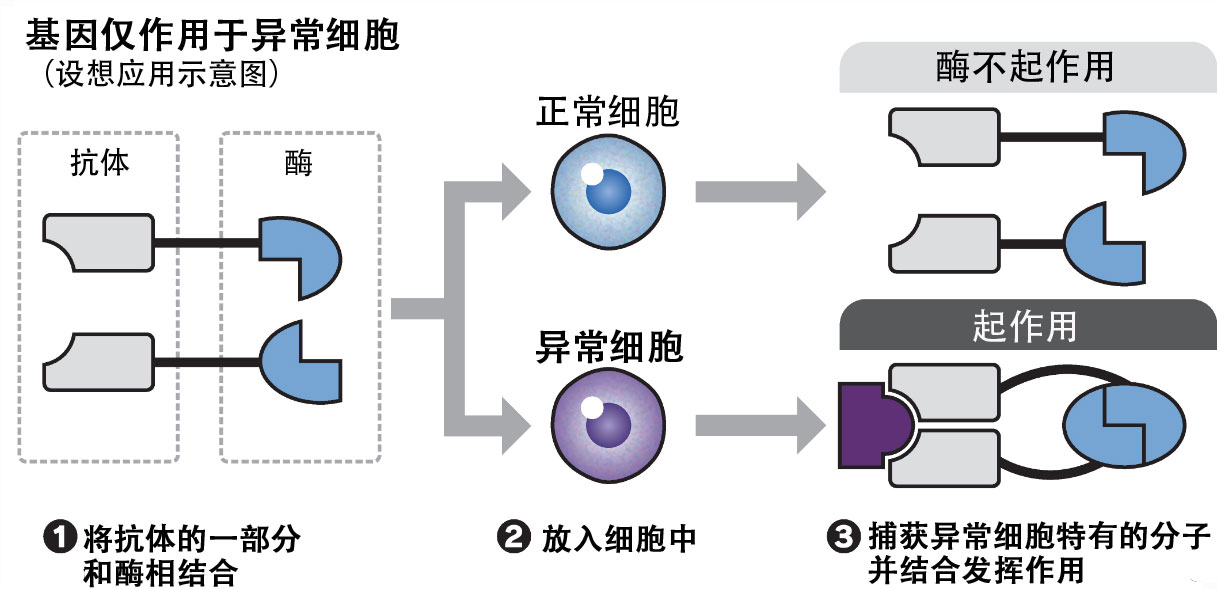
開發的蛋白質由從DNA合成RNA(核糖核酸)的名為「聚合酶」的酶和抗體的一部分結合後而成,共2對,只有結合在一起後,治療用基因才會表達。由於結合需要特定細胞内所含的分子,因此基因很難在正常細胞中發揮作用。理論上可以減少治療性蛋白質在健康臟器中的積累等副作用。
不同的細胞内部存在的分子也各有差異。所以,當細胞發生癌變時,就會隨之產生正常細胞中不存在的異常分子或蛋白質。目前通過檢測這些分子和蛋白質實現癌症早期診斷的研究正在推進之中。
本次研究通過利用生物體內的這一現象,設想隻用治療用基因攻擊癌細胞,從而抑制腫瘤生長的使用方法。傳統化學療法的抗癌藥物也作用於正常細胞,會給人體造成一定程度的傷害。如果能夠做到隻攻擊癌細胞,就可以減輕副作用。
此次開發的技術,只要改變與特定分子結合的抗體類型,就還可應用於癌症治療以外的領域。比如,利用抗體可以區分由多個氨基酸相連組成的肽、蛋白質和RNA等各種分子構造上的差異。
通過改變用於治療的基因類型,不僅可以產生蛋白質,還可以產生「基因編輯」修改細胞基因所必須的RNA。
研究團隊認為該技術可應用於將T細胞(一種免疫細胞)進行基因修改讓其攻擊癌細胞的「CAR-T細胞療法」。
「Kymriah」和「Yescarta」等獲得藥事批准的治療藥物價格均在3000萬日元以上,非常昂貴。因為這些目前的CAR-T細胞療法是從患者體內取出T細胞,進行基因修改後再返回體內的緣故。
而利用此次開發的技術,將有可能在患者體內僅對T細胞進行基因修改。由此可以減少體外管理細胞所需的時間和成本。
此次開發的技術用於臨床時,是否能夠真的發揮作用,以及是否存在安全問題等是今後必須解決的課題。
此外,該技術還有望應用於在由iPS細胞生產治療用細胞時從中僅選擇出高質量的細胞,或識別被病毒感染的細胞等。負責該項研究的研究生小松將大介紹說:「該技術的應用範圍非常廣泛」。
同時推進基礎研究

操作基因工作方式的基因表現控制技術有助於生命現象的闡明。其不僅可用於開發疾病治療方法等臨床應用,還有望推進基礎研究。
傳統研究很多都是採用人體擁有的控制系統來進行的。而此次開發的技術靈活應用帶有病毒的酶等,因此有望建立出對人體內部系統難以產生不良影響的靈活機制。
然而,要想成為可以自由操作子功能的便利工具,還有需要解決的課題,也即目前開發的蛋白質還相對較大。一般來說,抗體等大分子很難通過細胞表面的細胞膜。為此,研究人員正在考慮將抗體和酶包裹在脂質膜中,或將想要利用的基因加到無害的病毒上使其進入細胞内。
使用脂質和無害病毒的方法已經被用於製作新冠病毒疫苗。重要的要讓被吸收的蛋白質在細胞内有效地發揮作用。推進來自基礎研究的方法,也是擴大該技術應用範圍的關鍵。
日文:尾崎達也、《日經產業新聞》、2023/11/24
中文:JST客觀日本編輯部













