日本慶應義塾大學醫學部的市原元氣助教(研究當時)、佐野元昭副教授、該大學體育醫學綜合中心的勝俁良紀專任講師和京都大學研究生院醫學研究科的杉浦悠毅特定副教授的聯合研究團隊發表研究成果稱,發現了一種著眼於心肌梗塞的代謝變化的新治療方法。研究團隊利用疾病模型小鼠,通過「利用代謝分子的監測方法」詳細觀察了心肌缺血再灌注傷害的階段性進展過程,發現該疾病是由保護心肌的重要因子——麩胱甘肽(一種還原物質,多肽的一種)通過載體「MRP1」被釋放到細胞外而引起的。研究還證實,通過干預增強活性氧清除的代謝路徑,可以減少心肌缺血再灌注傷害後的心肌傷害。該成果有望推動心肌梗塞後的復健。相關成果已刊登在《Circulation Research》雜誌10月11日號上。
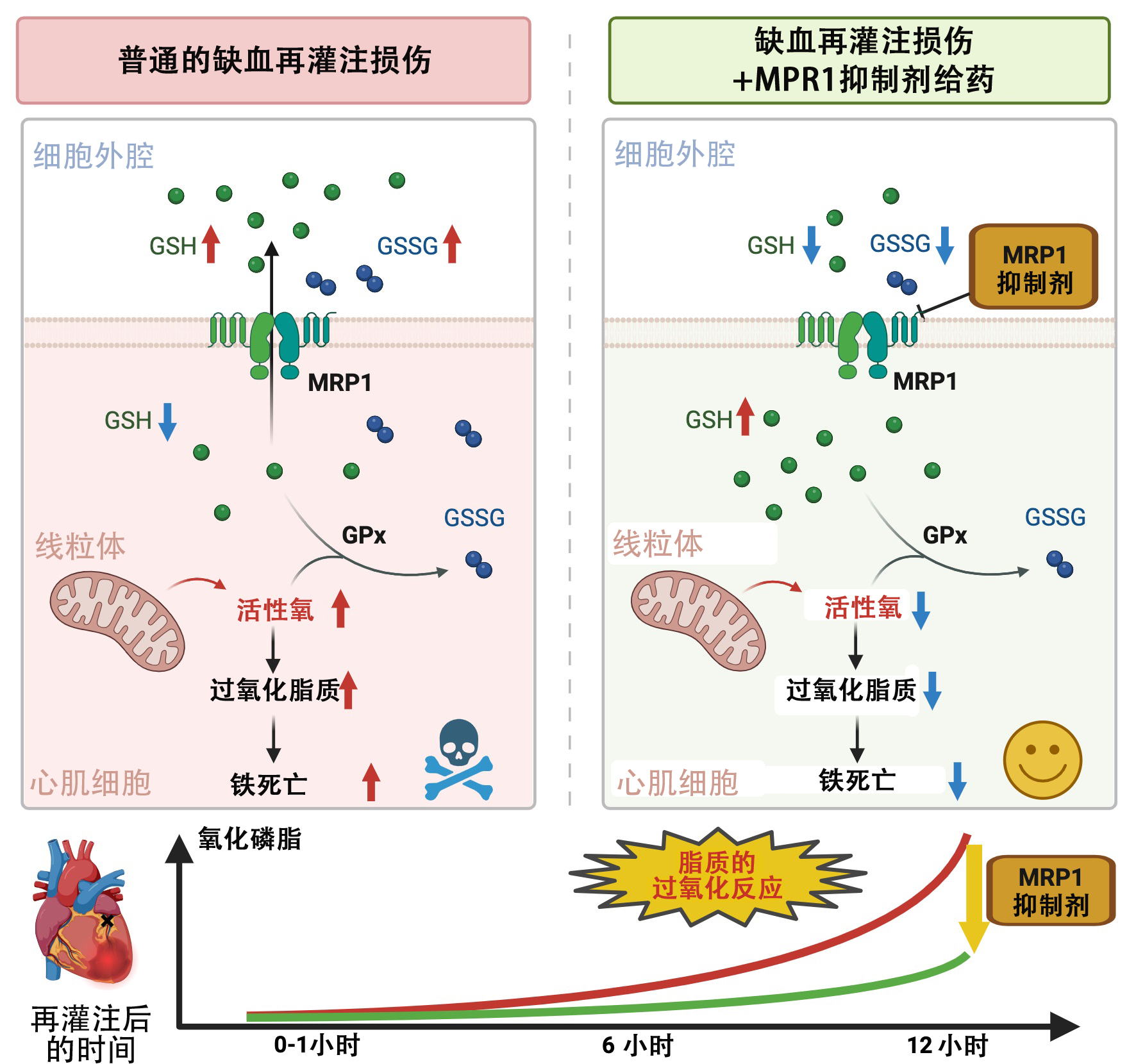
心肌缺血再灌注傷害的進展機制和MPR1抑制劑給藥的效果。(供圖:慶應義塾大學醫學部)
GSH:還原型麩胱甘肽
GSSG:氧化型麩胱甘肽
GPx:麩胱甘肽過氧化物酶
心肌梗塞(缺血性心臟病)是全球範圍内排名靠前的死亡疾病,近年來隨著治療技術的提高,搶救成功率已顯著提升。另一方面,由於心肌梗塞引起的缺血再灌注傷害,心臟泵血功能降低,許多患者在搶救後會出現心力耗竭,而目前尚未確立針對此的治療方法。缺血性再灌注傷害是由於缺血心肌在血流恢復後迅速再氧化,產生大量活性氧,使得細胞内各種蛋白質變性而引起的。
為此,研究團隊利用大鼠心臟再現了缺血再灌注傷害,並在活體狀態下持續分析了這一過程中產生的代謝物質變化。研究人員採用將筒狀半透膜植入心壁,連續收集並測量透過半透膜的心肌間質代謝物的方法(微透析法)。傳統方法通過收集同一傷害後的心肌細胞並分析代謝物等來尋找目標分子,但無法跟蹤隨時間快速變化的心肌代謝狀態。
結果,研究人員成功地在缺血前、缺血中和再灌注後的3個階段,分別連續收集到了同一活體心肌間質中的代謝物。研究人員還發現,心肌保護的關鍵因數,同時也是蠻力還原性物質的「麩胱甘肽」在缺血和再灌注階段會被釋放到細胞外,從而變得無法清除細胞内的活性氧類。
細胞内麩胱甘肽的枯竭會使活性氧類增加,導致脂質過氧化和因細胞膜脂質過度氧化而引發的細胞死亡(鐵死亡)。
此外,研究人員還發現這種細胞外釋放主要由一種被稱為MRP1的特殊載體介導。
於是,研究人員使用藥物抑制了MRP1的功能,結果發現麩胱甘肽保留在細胞内,不僅活性氧被清除,氧化脂質也減少了,由此可知麩胱甘肽可以支持心肌細胞的存活。
此外,研究還證實,這種以鐵死亡為靶向的治療法即使在缺血再灌注後數小時開始也具有一定的效果。
針對心肌梗塞發病6小時後出現的氧化脂質增加的情況,有望通過治療藥物延緩給藥實現有效的治療。
勝俁專任講師介紹說,在這項研究中,通過採用新技術「利用代謝分子的監測」方法,成功地明確了由心肌梗塞引發的有害活性氧清除機能逐漸下降的機制。利用這一發現,我們揭示了對抗氧化壓力的重要防禦物質——麩胱甘肽在缺血和再灌流時會洩漏到細胞外的現象。我們期望這一發現能為開發新的心肌梗塞治療方法開闢道路。
原文:《科學新聞》
翻譯:JST客觀日本編輯部
【論文資訊】
雜誌:Circulation Research
論文:MRP1-dependent Extracellular Release of Glutathione Induces Cardiomyocyte Ferroptosis After Ischemia-Reperfusion
DOI:10.1161/CIRCRESAHA.123.323517













