秋田 英萬
日本東北大學 研究生院藥學研究科 教授
2017年起擔任 CREST 研究代表
新型冠狀病毒疫苗獲得了2023年諾貝爾生理學或醫學獎。其基礎技術 RNA藥物的開發正吸引著越來越多的關注。在助於臨床應用的藥學研究中,不僅藥物的發現很重要,將藥物有效輸送到靶細胞的「Drug Delivery System(DDS,藥物遞送系統)」也很重要。東北大學研究生院藥學研究科的秋田英萬教授開發出了能控制體內及細胞内分子動態的高通用性劃時代材料,正在推進加速日本RNA 藥物發現的研究。
關注細胞内的藥物動態
為傳統淋巴學帶來新活力
「藥物遞送」是指將藥物精準地輸送到身體的所需位置以達到治療效果。藥物遞送學的研究領域非常廣泛,包括口服藥物從消化道吸收和攝取的過程、將注入血液的藥物輸送到目標器官的途徑和手段,以及減輕藥物的毒性等多個方面。多年來一直致力於藥物遞送研究的正是東北大學研究生院藥學研究科的秋田英萬教授。
秋田教授的研究重點是在藥物遞送中尤其是在微觀環境中,藥物成分在細胞内的動態。一直以來,人們對在血液中的DDS進行了廣泛的研究,但在 JST 的CREST「淋巴系統内奈米粒動態與交流的綜合控制和藥物發現基礎開發」項目中,秋田教授把目光投向了另一個脈管系統——淋巴。由於淋巴管難以觀察和分析,因此過去研究一直未能取得進展。然而,考慮到癌症也會擴散到淋巴結,因此秋田教授認為淋巴是一個非常重要的靶點。秋田教授通過開發控制淋巴内部運動的DDS,給傳統淋巴學注入了新的活力(圖1)。
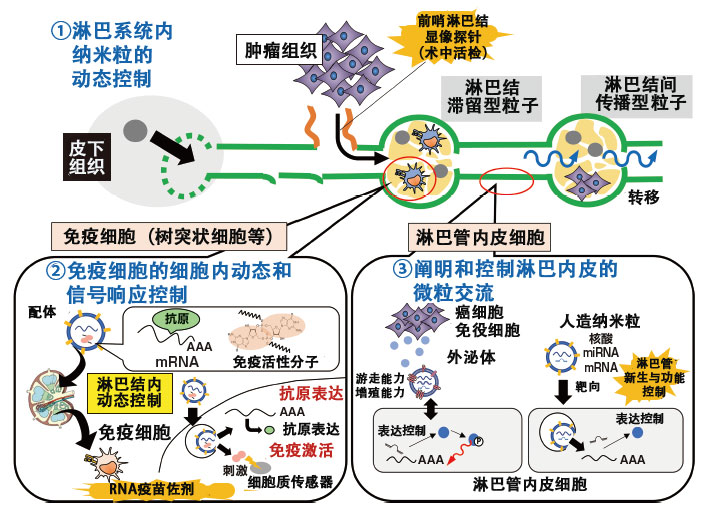
圖1 CREST項目的三大支柱
在通過淋巴體內微環境中的奈米粒動態、RNA疫苗的免疫控制機制、外泌體等内源性微粒、DDS製劑中的外源性微粒進行淋巴管內皮細胞的生物體內功能的解析和控制,其中奈米粒的解析和開發是關鍵。
在新冠疫情擴大的過程中,通過向體內注射信使核糖核酸(mRNA),以誘導出疫苗效果的RNA疫苗在全球範圍内獲得使用。2020年以後廣泛應用於臨床,美國賓夕法尼亞大學的卡塔琳·卡里科和德魯·魏斯曼因此獲得了諾貝爾生理學或醫學獎。秋田教授談到研究的意義時表示「DDS的開發是實現RNA藥物發現的一個非常重要的關鍵點」。
有助於基因療法的人造材料
可在細胞内自行破裂,遞送核酸
近年來,DDS的技術開發急劇加速。目前已開發出多種可應用於細胞療法的材料,分子改良的應用範圍也在不斷擴大。例如,作為癌細胞免疫療法的CAR-T療法,以前需要取出患者自身的T細胞,植入CAR基因後再將其送回患者體內。但隨著DDS的發展,可以直接將mRNA傳遞給體內的T細胞,使其表達CAR基因,就像用藥一樣進行治療的「In VivoCAR-T療法」已成為全球競相開發的題目。
DDS之所以能夠取得這樣突破性的進展,是因為奈米粒製造技術的不斷進步,全自動均質裝置取代了手工作業。新冠病毒疫苗也應用了這些技術。秋田教授與DDS醫藥用製劑原料企業日油(東京涉谷區)聯合開發出了在細胞内產生自我分解反應的新材料。這種材料可以形成脂質奈米粒,能夠根據細胞内部的環境有效地傳遞密封的藥物。
為了將mRNA人工導入到適當的臟器或細胞中,需要將在細胞外容易破裂的核酸分子封閉在由脂質或聚合體等材料形成的奈米粒中加以保護,然後再輸送到細胞内。但如果奈米粒過於穩定,被封裝的核酸就不能釋放從而無法發揮作用,因此,有待開發出兼具細胞外穩定性和細胞内破裂性的新型材料。
因此,秋田教授提出了用於奈米粒的人工材料「SS-Cleavable pH-Activated Lipid-Like Material(ssPalm)」。「ssPalm除了具有在細胞内還原化環境中容易被分解的雙硫键之外,還具有一種根據環境引發奈米粒子膜不穩定從而導致破裂的‘叔胺(三級胺)’結構。它被細胞吸收後,可以快速破裂並有效地進入細胞内部」。秋田教授通過在ssPalm分子中加入苯基酯鍵開發ssPalmO-Phe分子,引發粒子内有機反應,從而實現了在細胞内的自發性破裂(圖2、3)。
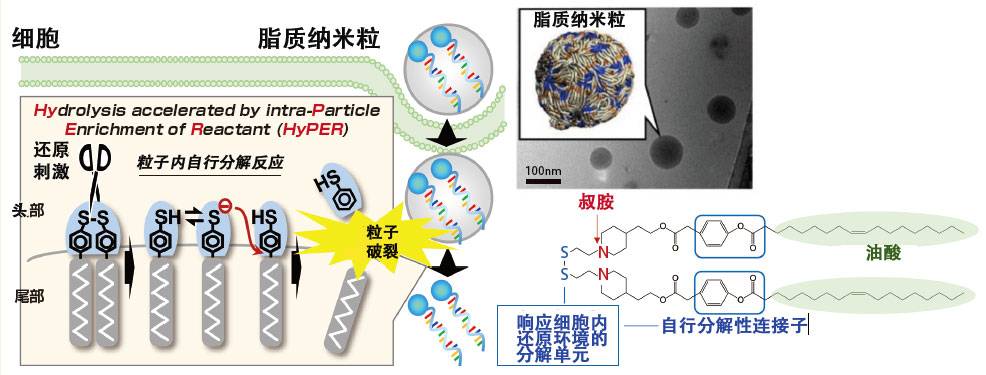
圖2 人造材料ssPalmO-Phe和脂質奈米粒
ssPalmO-Phe的化學式和電子顯微圖像,以及分子模擬計算得到的粒子模型。形成脂質奈米粒的ssPalmO-Phe可以内封mRNA和藥劑,並在細胞内的環境中自行分解,釋放出内封分子。
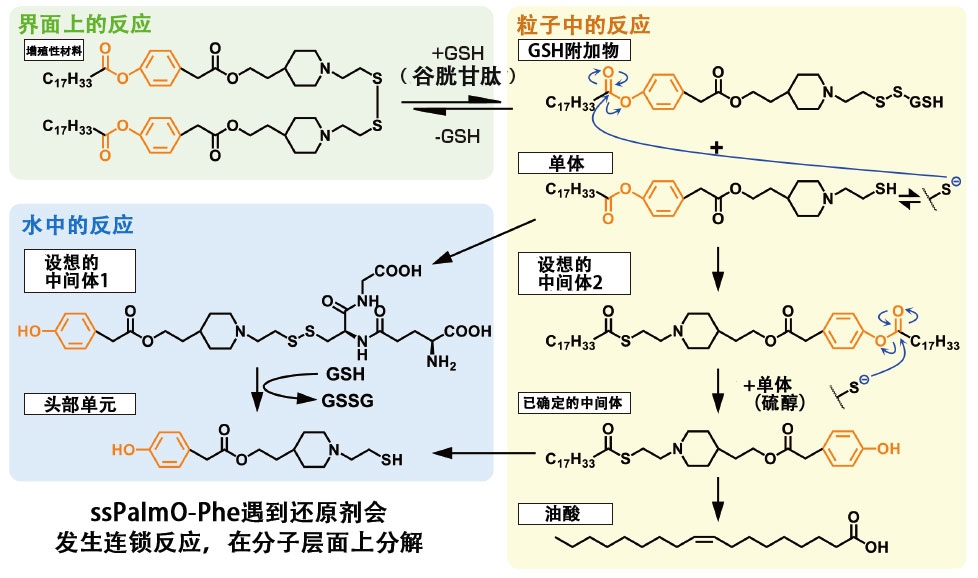
圖3 ssPalmO-Phe的結構和粒子内有機反應機制
通過小鼠的靜脈遞送mRNA時,在肝臟中出現了高蛋白表達。向血液中注射ssPalm 等脂質奈米粒時,血液中的蛋白會與其表面結合,被肝臟細胞的接受者識別。秋田教授還發現,通過加工ssPalmO-Phe形成的奈米粒表面,將其投放到皮膚表面後,淋巴内也出現了與血液中同樣的機制,實現了淋巴管內皮細胞的靶向化。
最近的研究表明,淋巴管內皮細胞不僅可形成淋巴管,還具有控制免疫細胞功能的作用。如果能將mRNA等核酸遞送給這些細胞,就有望實現免疫控制和治療淋巴水腫等疾病。高分解性ssPalmOPhe不容易在體內積累,具有極佳的安全性。希望通過應用該技術,大幅加速基因療法和根據患者的基因資訊選擇最佳療法的個性化醫療以及DNA/RNA疫苗的開發。
使用維生素的 RNA 疫苗
強效激活「殺傷性T細胞」
2023年9月秋田教授發表了題為《創造可激活殺傷性T細胞的RNA疫苗》的論文。這項研究成果表明,利用含有維生素E結構的ssPalm 製成的脂質奈米粒具有強有力地誘導在癌症治療和傳染性疾病治療中具有重要殺傷性的T細胞的性質。秋田教授介紹說「為了增加ssPalm分子的變化,我們將重點放在了生物來源成分上,目前正在開發採用脂溶性維生素——維生素A和維生素E作為脂溶性支架結構的分子。此外,雖然還不清楚其機制,但我們偶然發現,具有維生素 E 支架結構的分子具有非常高的免疫活化能力」。
RNA疫苗將作為病原體標記的「抗原」作為遺傳基因資訊植入到mRNA中,生物體將其轉換為蛋白質,從而發揮出疫苗的作用。在使用維生素E的脂質奈米粒上搭載mRNA的RNA疫苗能強效激活「殺傷性T細胞」。這種細胞被激活後具有殺死癌症和病原體抗原的能力,但RNA疫苗激活殺傷性T細胞的過程中尚不清楚是哪些細胞起了作用。對此,秋田教授通過向生物體內接種RNA疫苗並表達抗原,成功確定了能激活殺傷性T細胞的免疫細胞(圖4)。
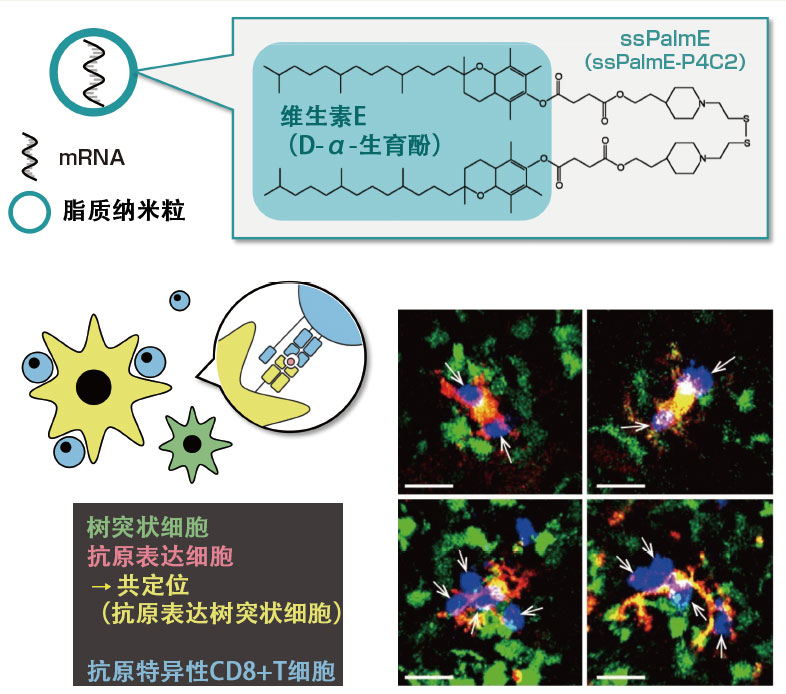
圖4 含有維生素E結構的由脂質奈米粒製成的RNA疫苗向殺傷性T細胞提供抗原
將由維生素E型離子化脂質構成的脂質奈米粒(上)中封入mRNA的RNA疫苗注入小鼠體內,通過顯微鏡觀察淋巴結内的抗原呈現情況,結果確認了表達疫苗抗原的樹突狀細胞與抗原獨特性殺傷性T細胞產生相輔作用的事實(下)。(圖中橫槓= 20μm)
RNA疫苗雖然通過SARS-CoV-2病毒的大流行得到了迅速發展,但副作用的問題也逐漸凸顯。秋田教授與理化學研究所的岡田峯陽組長進行聯合研究,發現了通過 RNA疫苗誘導細胞性免疫的部分機制。隨著脂情況下,為目標細胞補充蛋白質的mRNA藥物。
Ready-to-Use製劑的開發
誰都可以製備RNA搭載粒子
DDS的材料開發出來之後,就要想辦法讓大家都能使用它們。下一步要進行的是使用上述DDS材料促進RNA藥物發現的技術開發研究。當時提出聯合研究的申請也很多,研究室的工作人員製作了粒子並送往多個合作夥伴手裏。「但由於mRNA的分解性很高,所以必須按照實驗日程來製作。我們與研究室的工作人員一起,挑戰開發讓客戶隻需要添加 mRNA 溶液就能輕鬆製備内封 mRNA 的脂質奈米粒的技術」秋田教授回顧了開發的起因時說道。
這種隨時可以根據需要製備脂質奈米粒的Ready-to-Use製劑的開發技術,對 RNA 藥物發現的發展也具有非常重要的意義。雖然國内外都在進行 RNA 藥物發現,但並不是所有人都能輕易參與其中。其中一個原因是,要找到一種具有潛在療效的蛋白質或mRNA,並驗證其是否可以用作mRNA藥物,這在技術上是很困難的。「所以我想,如果能夠事先製造出空粒子,然後讓使用者隻需要在其中加mRNA,就可以製備出無論是細胞層面還是動物實驗層面中都能使用的脂質奈米粒,那麼其通用性將會大大提高」。
經過4年左右的時間,對粒子的製造工藝和冷凍乾燥時的添加劑、濃度等條件的組合進行了反複試驗後,於2023年2月發表了日本首個冷凍乾燥型Ready-to-Use製劑(圖5)。因為不需要特別的設備和技術,只要有溫度控制設備誰都可以使用,所以可以簡單地驗證自己設計的mRNA在藥物發現方面的可行性。還可以同時搭載長mRNA 和分子量較低的核酸,通過導入兩者來實現基因編輯。
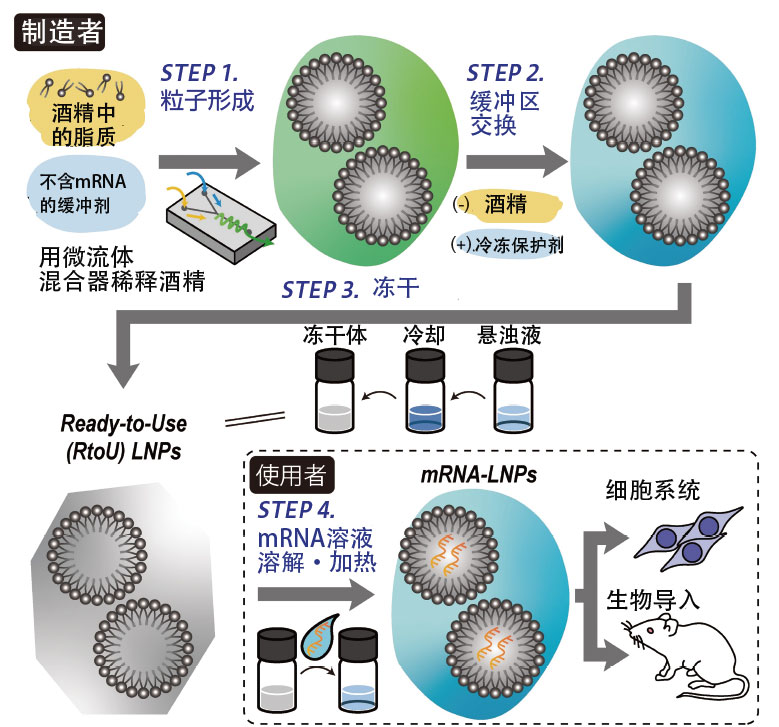
圖5 Ready-to-Use型LNP
蛋白質的設計圖mRNA和LNP在混合狀態下會互相粘附,但當施加熱能時,奈米粒的結構就會發生變化,形成mRNA自發地被包裹在其中的脂質奈米粒。經確認,製備的奈米粒與傳統方法製備的奈米粒具有相同的結構,即使注射到血液中也能發揮同等程度的活性。
開發有助於患者和研究人員的技術
在剩下的一年裏制定規畫圖
秋田教授一直都在追求「有利於人類的研究」。在研究過程中,不僅僅是直接幫助患者,通過DDS技術支持不同領域的研究人員也非常重要。Ready-to-Use 的開發就是一個例子,不只是一味的在RNA藥物發現領域開展競爭,而是公開對日本RNA藥物發現具有價值的資訊以及開發工具。如果企業和研究人員能利用此工具進行藥物發現研究,最終也會為患者帶來幫助。「我最近強烈地感受到了這一趨勢非常重要。我認為 DDS 是一個可以實現這一目標的領域,因此今後也會繼續努力」。
秋田教授在聽取實際使用Ready-to-Use製劑的研究人員的成果報告時,發現了問題,也由此產生了新的想法,使得更加容易提出新的使用方法,秋田教授自己的想法也發生了很大的變化。另一方面,對於目前DDS整體面臨的課題,秋田教授指出細胞和臟器的靶向化技術還不夠成熟。雖然想法已經由來已久,但使用奈米粒的 DDS技術尚未實際投入應用。血液注射型的脂質奈米粒,注射的大部分都收歛集到肝臟裏,所以新藥的臨床試驗也都是以肝臟為靶點。如果能以肝臟以外的器官和細胞為靶點,就能大幅擴大其用途。
不僅是 DDS 領域,當前的藥物發現研究是一個瞬息萬變的領域。因此,秋田教授還認識到除了中長期的研究之外,還有必要進行如何將自己的技術靈活運用到瞬息萬變的藥物發現技術種子的短期研究中。秋田教授對未來充滿熱情:「CREST的5年研究對我幫助很大。在還剩下一年的時間裏,我想整理出有關自體免疫性疾病的治療效果的研究結果,並整理CREST的成果和下一階段的規畫圖」。(TEXT:吉本直子、PHOTO:楠聖子)

原文:JSTnews 2023年12月號
翻譯:JST客觀日本編輯部














