東海大學醫學部綜合診療學系的渡邊伸央講師、豬口貞樹客座教授等的研究團隊發表研究成果稱,從約700萬個現有化合物中全球首次發現了能同時選擇性抑制人和小鼠的血小板平足蛋白(podoplanin)接受者(CLEC-2)和膠原蛋白接受者(GPVI)的化合物基本結構。該成果有望加速癌症相關血栓症、癌症轉移和動脈硬化相關血栓症等疾病的有效治療藥物的開發。相關成果已發表在《Thrombosis and Haemostasis》上。
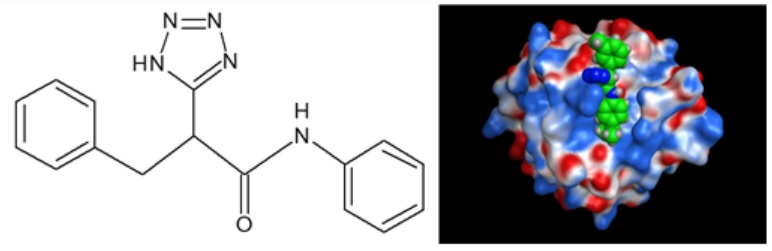
圖1:Diphenyl-tetrazol-propannamide衍生物與CLEC-2的結合(供圖:東海大學)
在In silico的結合試驗中,嵌入CLEC-2分子的平足蛋白結合位置上的化合物G1分子(diphenyl-tetrazol-propanamide衍生物之一)。CLEC-2分子顯示為靜電位雲,化合物G1顯示為空間填充模型。
血小板通過在血管傷害部位被激活並凝集來堵塞傷害部位,是負責止血的重要因素。然而,在癌症或動脈硬化等病理狀態下,血小板聚集會阻塞血管並引發血栓症。血小板表面有包括膠原蛋白接受者在内的十多種觸發血小板聚集反應的接受者,但目前使用的阿司匹靈和氯吡格雷等抗血小板藥物因各種接受者的活化,會抑制在下游通常會發生的次級反應。因此,一方面廣泛適用於有血栓症風險的患者的預防,另一方面,由於缺乏選擇性,同時伴隨出血的風險。鑑於此,有必要開發對各種接受者具有選擇性的抗血小板藥物。
在血小板上的接受者中,CLEC-2由平足蛋白激活,GPVI由膠原蛋白激活。
研究團隊通過使用獨有計算機程序進行化合物結合評估,從約700萬的現有化合物中篩選出抗CLEC-2候選化合物,並應用其中的約100種化合物進行了實驗驗證。驗證結果表明,12種具有diphenyl-tetrazol-propanamide骨架的化合物同時符合CLEC-2的平足蛋白結合位置和GPVI的膠原蛋白結合位置,並且實際上分別阻礙了與平足蛋白和膠原蛋白之間的相輔作用,並因此抑制了人和小鼠的血小板聚集反應。
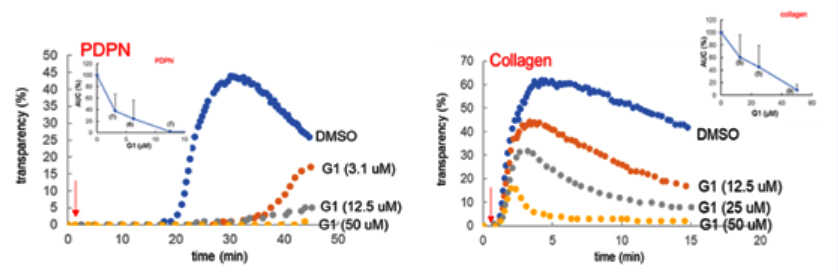
圖2化合物G1對人洗滌血小板的平足蛋白和膠原蛋白誘導的聚集的抑制作用(供圖:東海大學)
化合物G1可以抑制平足蛋白誘導聚集的IC50=3μM,膠原蛋白誘導聚集的IC50=15μM左右。
然而,研究發現該藥物的療效在小鼠血栓模型中下降。造成該現象的原因是與血液中白蛋白的結合太強,此發現指明瞭今後實際應用所需的基本骨架結構的修改方向。
靜脈血栓症約佔癌症患者死亡原因的20%,其中一部分被認為與平足蛋白激活血小板CLEC-2導致聚集引發靜脈血栓有關。另一方面,動脈硬化症中,動脈粥樣硬化斑塊塌陷,基底膜的膠原蛋白通過與血小板的GPVI結合,誘導聚集,導致動脈血栓形成,從而引發心肌梗塞和腦梗塞。
目前,無論是在臨床實務還是在臨床試驗中,都沒有針對CLEC-2和GPVI的小分子抑制劑。通過對本次研究團隊發現的diphenyl-tetrazol-propanamide基本骨架進行修改和最適化,將有望加速針對癌症相關血栓症、癌症轉移、動脈硬化相關血栓症的有效治療和預防藥物的研發。
原文:《科學新聞》
翻譯:JST客觀日本編輯部
【論文資訊】
雜誌:hrombosis and Haemostasis
論文:Diphenyl-tetrazol-propanamide derivatives act as dual-specific antagonists of platelet CLEC-2 and GPVI.
DOI:10.1055/a-2211-5202













