日本東北大學加齡醫學研究所(Institute of Development, Aging and Cancer, Tohoku University)腫瘤生物學領域的吉野優樹助教、千葉奈津子教授等與該大學研究生院醫學系研究科的研究生本成登貴和、石田孝宣教授等人合作,開發出了一種測量來自小鼠腫瘤組織及血液的淋巴母細胞樣細胞的同源性重組修復活性的方法。利用該方法可以預測癌症治療藥物的效果和診斷遺傳性乳房癌/卵巢癌症候群。相關研究成果發表在期刊《Scientific Reports》上。
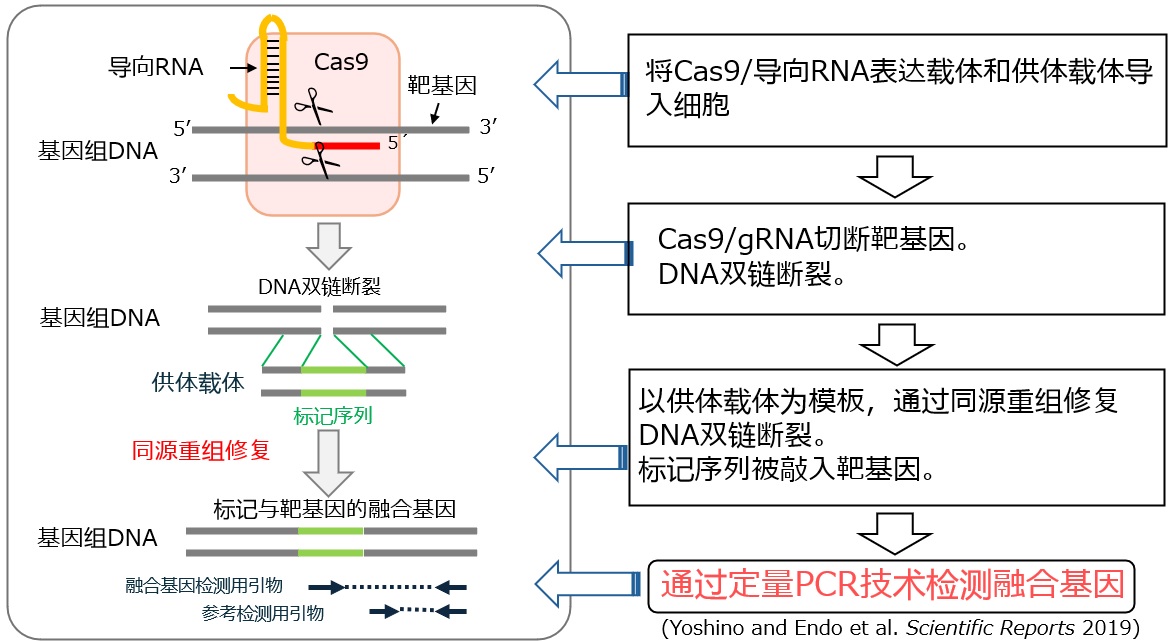
圖1 ASHRA的概述(供圖:東北大學)
對於同源性重組修復DNA雙鏈斷裂機制存在異常腫瘤,PARP抑制劑和鉑類抗癌藥物等被認為有效,而同源性重組修復所需要的分子如出現基因異常,則會導致遺傳性乳房癌/卵巢癌症候群。因此,研究人員認為,評估同源性重組修復活性將有助於預測癌症治療的有效性和診斷遺傳性乳房癌·卵巢癌症候群。
此前,臨床上評估同源性重組修復活性一般使用的是對BRCA1和BRCA2等在同源性重組修復中發揮作用的因子進行基因檢測的。然而,基因檢測不可能檢測出所有能引起同源性重組修復異常的致病基因,而且發現的基因變化有時無法判斷是否為異常。
研究團隊利用千葉教授等人開發的同源性重組修復活性測量方法ASHRA(Assay for Site-specific HR Activity),成功地直接測定了來自腫瘤組織及血液細胞的同源性重組修復活性。
在實施ASHRA時,研究人員向待測細胞中導入測定用載體,其中包括導致基因體DNA斷裂的Cas9/gRNA表達載體,以及具備與斷裂位點相同序列和檢測所需標記序列的供體載體。當基因體DNA上發生的DNA雙鏈斷裂利用供體載體進行同源性重組修復後,標記序列便被敲入了DNA雙鏈斷裂處,從而產生了標記序列與内源性基因的融合基因,此時便可運用定量PCR技術對融合基因進行檢測。
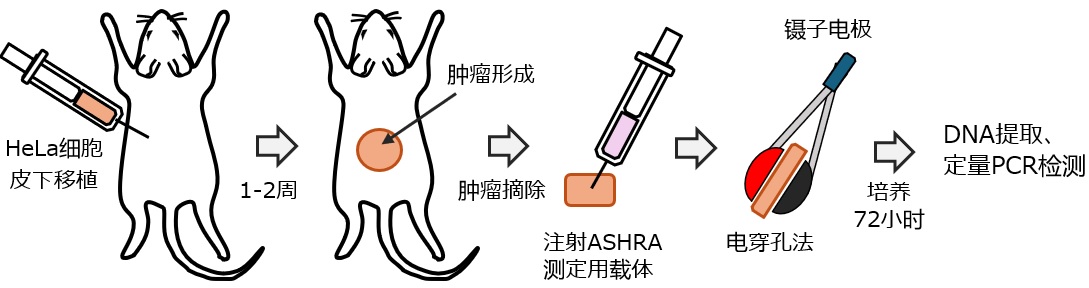
圖2 小鼠腫瘤組織中的同源性重組修復活性測定(供圖:東北大學)
研究人員將人癌細胞移植到小鼠體內以形成腫瘤後摘除,然後向腫瘤中注射測定用載體,利用電穿孔法將載體導入腫瘤細胞,即可檢測到經過同源性重組修復產生的融合基因。該方法測定的同源性重組修復活性與向小鼠投用PARP抑制劑「奧拉帕利」時的腫瘤縮小效果表現出高度相關。
此外,針對血液來源的淋巴母細胞樣細胞,通過電穿孔法將測定用載體導入其中後,也可檢測同源性重組修復活性。並且,在具有單等位基因BRCA1突變的遺傳性乳房癌/卵巢癌症候群的淋巴母細胞樣細胞中,檢測到同源性重組修復活性出現統計學意義上的顯著降低。這些結果表明,通過ASHRA進行的遺傳性乳房癌/卵巢癌症候群患者正常細胞——血液來源細胞的同源性重組修復活性評估,在診斷中具有應用潛力。
ASHRA可以直接檢測出同源性重組修復活性的變化,因此研究人員認為,即便是在未知的同源性重組修復因子存在異常,或是已知的同源性重組修復因子的基因變化異常與否無法判斷的情況下,它也能檢測出異常。該方法的臨床應用有望更有效地診斷癌症治療和遺傳性乳房癌/卵巢癌症候群。
原文:《科學新聞》
翻譯:JST客觀日本編輯部
【論文資訊】
雜誌:Scientific Reports
論文:Evaluating homologous recombination activity in tissues to predict the risk of hereditary breast and ovarian cancer and olaparib sensitivity
DOI:org/10.1038/s41598-024-57367-6













